Clear Sky Science · nl
Experimentele en theoretische evaluatie van geometrie-afhankelijke doxorubucine-belading op ceriumoxide-nanodeeltjes via modellering van van der Waals-interacties
Waarom de vorm van piepkleine dragers voor medicijnen ertoe doet
Kankergeneesmiddelen zoals doxorubucine zijn krachtig maar kunnen ook gezond weefsel beschadigen. Een strategie om ze veiliger te maken is ze te bevestigen aan nanodeeltjes die het middel rechtstreeks naar tumoren vervoeren. Deze studie stelt een verrassend eenvoudige vraag met grote implicaties: verandert de vorm van het nanodeeltje — of het nu op een bol, een staaf of een plaatje lijkt — hoeveel geneesmiddel het kan dragen en hoe goed het werkt?
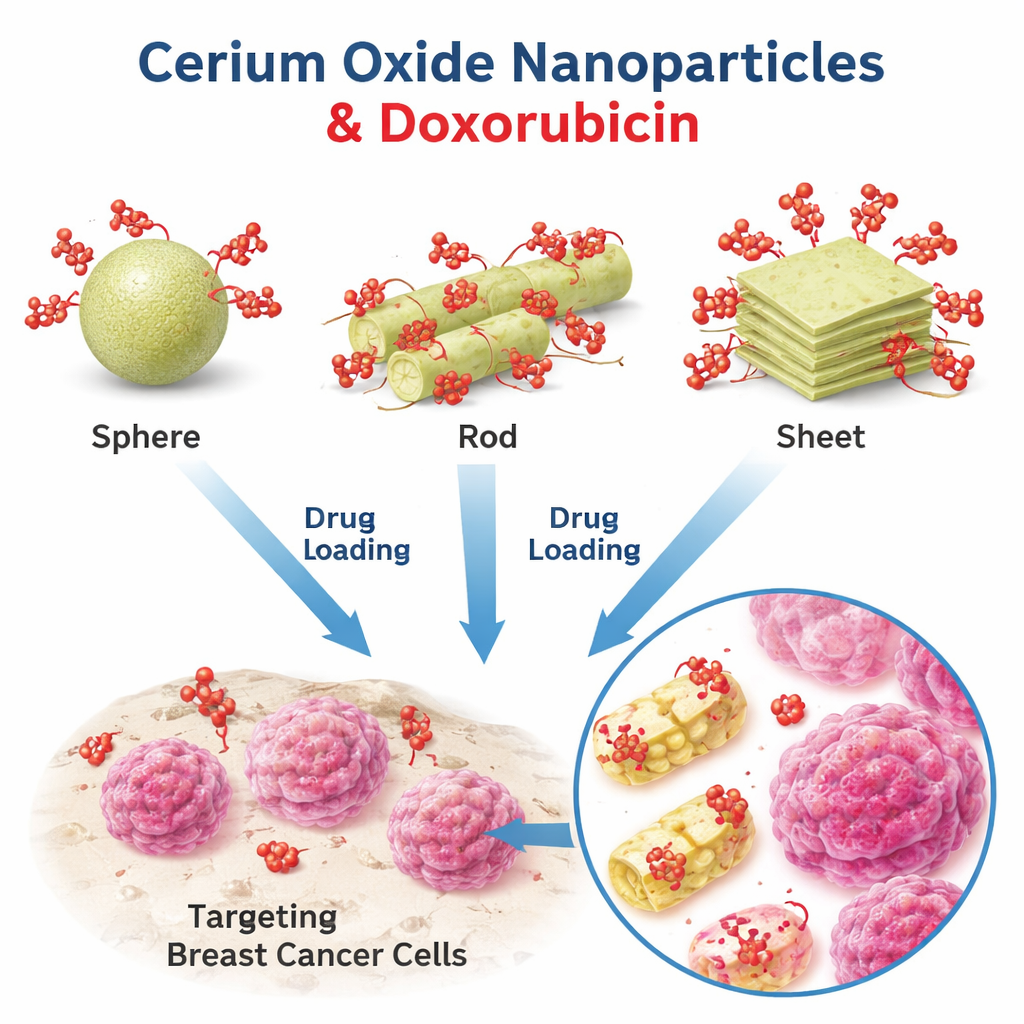
Drie piepkleine vormen, één kankergeneesmiddel
De onderzoekers richtten zich op nanodeeltjes van ceriumoxide, een materiaal dat al bekendstaat om zijn antioxidante, antibacteriële en wondgenezende eigenschappen, en onderzochten het potentieel als drager voor doxorubucine, een veelgebruikt chemotherapeuticum. Ze bereidden drie verschillende vormen van ceriumoxide: vrijwel perfecte bolletjes, staafvormige cilinders en dunne plaatachtige vlokken. Met elektronenmicroscopie en lichtverstrooiingsmetingen bevestigden ze de afmetingen en vormen van de deeltjes: bollen vormden compacte kralen, cilinders verschenen als slanke stokjes en platen als brede, platte lagen. Deze gecontroleerde set vormen stelde hen in staat om te onderzoeken hoe louter de geometrie het gedrag van het geneesmiddel verandert, terwijl het materiaal zelf hetzelfde bleef.
Meten hoeveel geneesmiddel elke vorm kan vasthouden
Om te bepalen hoe effectief elke vorm doxorubucine kon dragen, mengde het team de nanodeeltjes met een oplossing van het geneesmiddel en meette daarna hoeveel geneesmiddel in de vloeistof overbleef. Minder restanten betekenden dat meer op de deeltjes was geladen. Met precieze lichtgebaseerde methoden (UV–vis en fluorescentiespectroscopie) vonden ze dat bolvormige nanodeeltjes de meeste doxorubucine opvingen, met ongeveer 86% van het geneesmiddel dat op of in de bollen terechtkwam. Cilinders kwamen op ongeveer 79%, en platen bleven rond circa 67%. Toen deze belastte deeltjes werden getest tegen een agressieve borstkankercellijn, was de bolgebaseerde formulering opnieuw het meest effectief in het doden van kankercellen, gevolgd door de cilinders en vervolgens de platen. Interessant genoeg gaven de bollen ook het langzaamst het geneesmiddel vrij over tijd, wat suggereert dat een hoge belading gecombineerd met trage afgifte het effect van het geneesmiddel binnen cellen kan versterken.
Wiskunde toepassen op de nanowereld
Naar aanleiding van het labwerk bouwden de onderzoekers een analytisch model — een soort vereenvoudigde wiskundige microscoop — om te berekenen hoe sterk een enkele, min of meer bolvormige doxorubucinemolecule aan elk type nanodeeltje zou blijven kleven. Ze concentreerden zich op van der Waals-krachten, de zwakke maar alomtegenwoordige aantrekking die helpt dat moleculen aan elkaar hechten. Door het geneesmiddel te behandelen als een kleine bol nabij een sferische, cilindrische of plaatachtige ceriumoxide-oppervlakte, deriveerden ze exacte formules voor de interactie-energie terwijl het geneesmiddel naderde of zich verwijderde. Deze berekeningen stelden hen in staat te voorspellen welke vorm de meest stabiele binding zou geven, zowel wanneer het geneesmiddel in het deeltje begraven zit als wanneer het op het oppervlak ligt, zonder grootschalige computersimulaties te hoeven draaien.
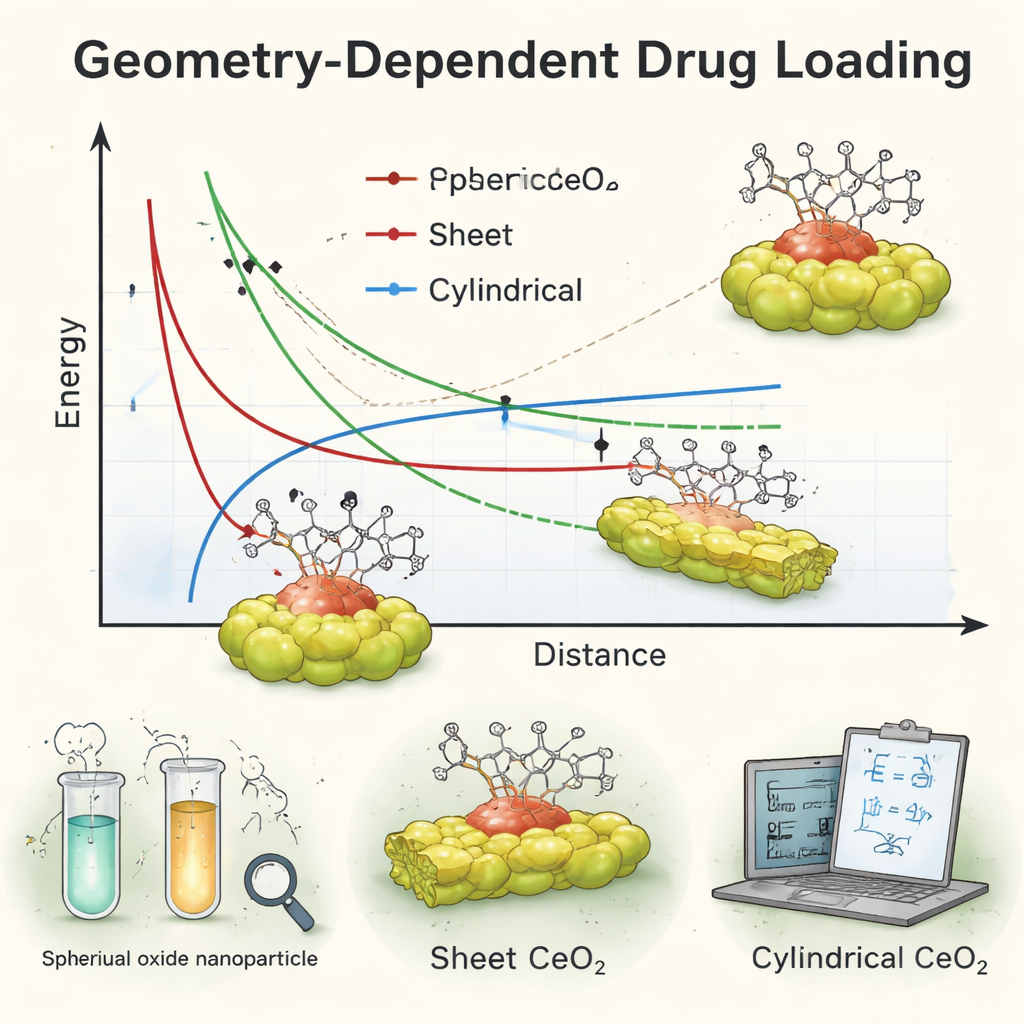
Waar theorie overeenkomt — en waar ze faalt
Toen het team hun vergelijkingen vergeleek met de experimentele gegevens, vonden ze een opvallende gedeeltelijke overeenkomst. De wiskunde suggereerde dat bol- en plaatachtige nanodeeltjes doxorubucine met zeer vergelijkbare bindingssterktes zouden vasthouden, wat goed aansloot bij de over het algemeen hoge belading die voor die twee vormen werd waargenomen. Bovendien kwamen bollen, wanneer het geneesmiddel werd verondersteld in de deeltjes opgesloten te zitten, naar voren als iets stabieler dan de andere vormen, wat de sterke prestaties van de sferische dragers in het lab weerspiegelde. Maar er was een puzzel: het model voorspelde relatief zwakkere binding voor cilinders, terwijl experimenten toonden dat staafvormige deeltjes het geneesmiddel nog steeds behoorlijk efficiënt laadden — bijna even goed als de bollen. Deze mismatch, met name voor de cilindrische vorm, toonde aan dat een eenvoudig model dat de omgeving als lege ruimte behandelt en oppervlakte-details gemiddeldeert, het echte gedrag van geneesmiddel–nanodeeltje-systemen die in vloeistof zijn ondergedompeld en met cellen interageren, niet volledig kan vatten.
Wat dit betekent voor toekomstige kankerbehandelingen
Voor niet-specialisten is de boodschap tweeledig. Ten eerste is de vorm van een nanodeeltje geen cosmetisch detail; het beïnvloedt direct hoeveel kankergeneesmiddel het kan dragen, hoe snel dat geneesmiddel wordt vrijgegeven en hoe krachtig het tumorcellen kan aanvallen. Sferische ceriumoxide-deeltjes kwamen in deze studie naar voren als bijzonder veelbelovende dragers voor doxorubucine, door hoge belading, sterke kankerceldoding en trage lekkage van het geneesmiddel te combineren. Ten tweede toont de studie de grenzen van zelfs elegante wiskundige modellen wanneer ze de rommelige realiteit van de biologie te veel vereenvoudigen. Om echt betrouwbare nanogeneesmiddelen te ontwerpen, zal toekomstig werk gedetailleerde experimenten moeten combineren met geavanceerdere theorieën die de waterige omgeving, complexe deeltjesoppervlakken en clustering van deeltjes omvatten. Gezamenlijk kunnen deze ontwikkelingen leiden tot slimmere nanodeeltje-ontwerpen die krachtige geneesmiddelen veiliger en effectiever afleveren.
Bronvermelding: Sripaturad, P., Keo, S., Wongpan, A. et al. Experimental and theoretical evaluation of geometry-dependent doxorubicin loading onto cerium oxide nanoparticles via van der Waals interaction modeling. Sci Rep 16, 6169 (2026). https://doi.org/10.1038/s41598-026-36893-5
Trefwoorden: nanogeneeskunde, ceriumoxide-nanodeeltjes, doxorubucine-afgifte, nanodeeltje-geometrie, borstkankertherapie