Clear Sky Science · nl
Synthese en antikankerevaluatie van nieuwe thioimidazoolderivaten met een trimethoxyfenylgroep
Nieuwe chemische instrumenten in de strijd tegen kanker
Chemotherapie beschadigt vaak gezonde cellen naast de tumor, wat leidt tot zware bijwerkingen. Deze studie onderzoekt een nieuwe familie laboratoriumgemaakte moleculen die erop gericht zijn kankercellen veel sterker te treffen dan normaal weefsel. Door op slimme wijze twee chemische bouwstenen te combineren die al bekendstaan uit geneesmiddelen, creëerden de onderzoekers verbindingen die in reageerbuis- en 3D-tummodellen sterke, gerichte killing van kankercellen laten zien, terwijl gezonde cellen grotendeels gespaard blijven.
Slimmere kankerdodende moleculen bouwen
Het team richtte zich op twee “geprivilegieerde” chemische structuren die steeds terugkeren in succesvolle geneesmiddelen. De ene is imidazool, een klein ringetje dat goed in veel biologische doelwitten past. De andere is een trimethoxyfenyl (TMP)-groep, een patroon van drie zuurstofhoudende zijketens op een aromatische ring dat centraal staat in diverse antikankerstoffen die de celdeling verstoren. Door een zwavelatoom in de imidazoolkern op te nemen (waardoor een thioimidazool ontstaat) en deze te koppelen aan een TMP-groep, hoopten de chemici het gedrag van de moleculen in het lichaam en hun bindingssterkte aan kankergerelateerde eiwitten te verfijnen. Met een stapsgewijze syntheseroute bouwden ze een bibliotheek van verwante verbindingen, elk subtiel aangepast om te onderzoeken welke eigenschappen het belangrijkst zijn voor antikankeractiviteit. 
Kankercellen testen terwijl gezond weefsel gespaard blijft
De nieuwe moleculen werden getest op vier menselijke kankercellijnen — osteosarcoom (bot), cervicaal, colorectaal en longkanker — en op niet-kankerachtige longfibroblasten. Veel van de verbindingen remden of stopten de kankercelgroei, maar één viel in het bijzonder op: aangeduid als 13b. Het doodde bot- en cervicaalcellen bij zeer lage concentraties, maar bleek geen detecteerbare toxiciteit te hebben voor normale fibroblasten, zelfs niet bij doses meer dan 60 keer hoger. Meerdere andere verbindingen waren matig krachtig maar minder selectief, wat benadrukt hoe kleine structurele veranderingen — zoals het toevoegen van een chlooratoom of een nitrogroep op specifieke posities — het evenwicht tussen brede toxiciteit en kankerspecifieke werking kunnen doen omslaan.
Hoe het leidende verbinding kankercellen zelfvernietiging laat ondergaan
Om te begrijpen wat 13b precies in cellen doet, zochten de onderzoekers naar kenmerken van geprogrammeerde celdood, of apoptose. Kankercellen behandeld met 13b werden positief voor Annexine V en activeerden de enzymen caspase-3 en -7, klassieke markers dat een cel in een ordelijk suïcideprogramma is geduwd in plaats van simpelweg te barsten. Microscopie toonde heldere vlekken van γH2AX, een signaal van gebroken DNA-strengen, in de kernen van behandelde cellen. In de loop van de tijd begon het interne geraamte van de cellen zich te reorganiseren en af te breken, vooral in cervicaalcellen die rond werden en losraakten — visuele aanwijzingen dat apoptose goed op gang was. Gezamenlijk tonen deze bevindingen aan dat 13b het DNA van kankercellen beschadigt en de cellen vervolgens een gecontroleerd doodspad induwt.
Van vlakke cellaagjes naar 3D-mini-tumoren
De meeste laboratoriumtests kweken kankercellen in dunne lagen, die niet volledig de dichte, gelaagde structuur van echte tumoren nabootsen. Om dit aan te pakken, lieten de onderzoekers de kankercellen uitgroeien tot driedimensionale sferoïden — kleine, bolvormige clusters die beter lijken op de architectuur van een tumor en de uitdagingen van geneesmiddelpenetratie. Wanneer deze sferoïden werden behandeld met 13b, krimpten ze in een dosisafhankelijke mate. Botsferoïden waren bijzonder gevoelig en werden klein, los en gefragmenteerd bij hogere medicijnniveaus. Fluorescente kleuring toonde golven van apoptose die van buiten naar binnen door het sferoïde trokken naarmate de concentratie steeg, wat bewijst dat 13b kan doordringen en cellen door het hele compacte weefsel kan doden. 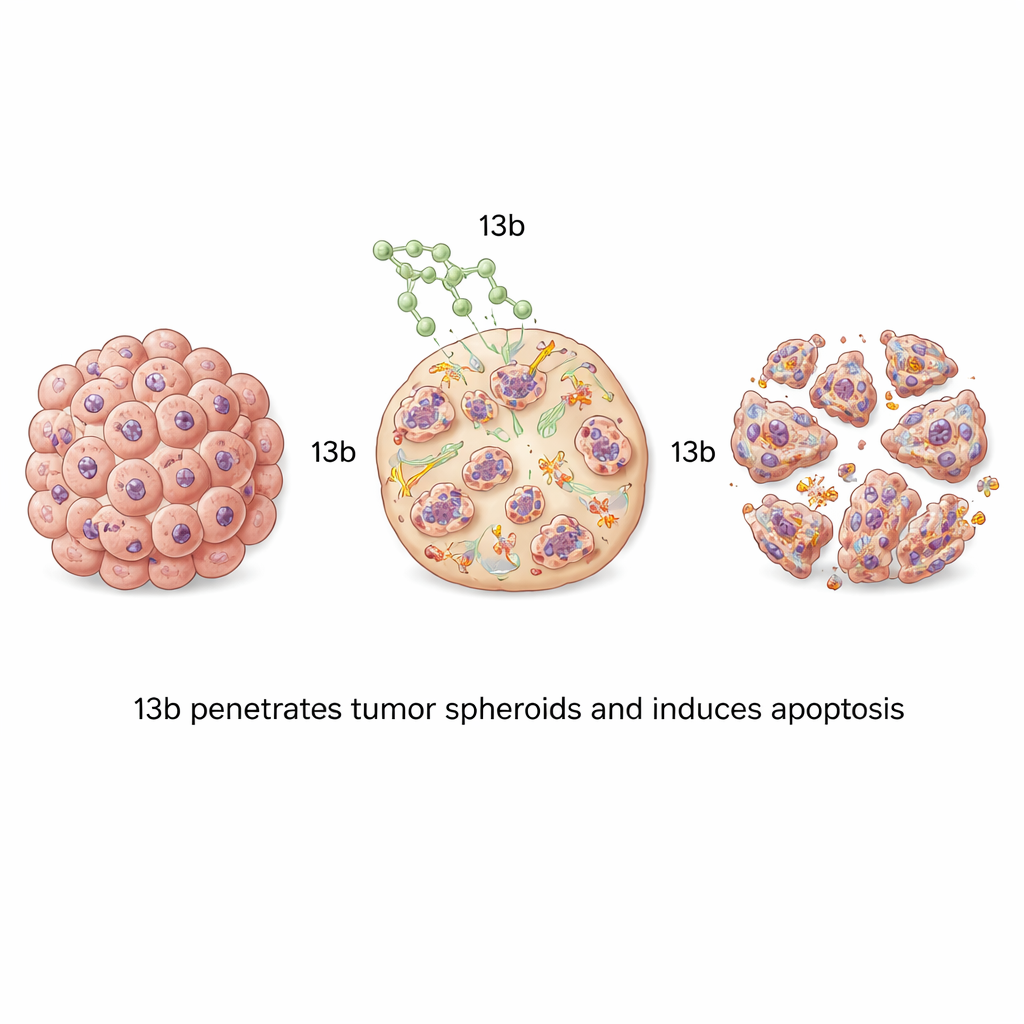
Waarom dit werk ertoe doet voor toekomstige kankerbehandelingen
Voor niet-specialisten is de kernboodschap dat de onderzoekers een nieuwe klasse kleine moleculen hebben gemaakt die de beste eigenschappen van twee bewezen medicinale componenten in één hybride ontwerp combineren. Hun leidende verbinding, 13b, kan kankercellen efficiënt herkennen en vernietigen terwijl gezonde cellen in laboratoriumtests grotendeels gespaard blijven, en blijft effectief zelfs in meer realistische 3D-tummodellen. Hoewel er nog veel werk te doen is — zoals het exact vaststellen van de moleculaire doelen, het verbeteren van de oplosbaarheid en dierproeven — toont deze studie aan dat het combineren van thioimidazool- en TMP-kaders een veelbelovende strategie is om meer selectieve en krachtige antikankermiddelen te ontwerpen.
Bronvermelding: Maciejewska, N., Grybaitė, B., Anusevičius, K. et al. Synthesis and anticancer evaluation of novel thioimidazole derivatives bearing a trimethoxyphenyl moiety. Sci Rep 16, 6271 (2026). https://doi.org/10.1038/s41598-026-36890-8
Trefwoorden: antitumorale middelen, imidazoolderivaten, trimethoxyfenyl, apoptose, 3D-tumorsfèroïden