Clear Sky Science · nl
Interpreteerbare machine learning onthult niet-lineaire ontstekingsdrempels en synergetische interacties bij hypertrofische littekens na brandwonden: ontwikkeling van een intelligent klinisch besluitvormingssysteem
Waarom littekens na brandwonden ertoe doen
Voor mensen die zware brandwonden overleven eindigt de strijd niet zodra de huid gesloten is. Velen ontwikkelen dikke, verheven littekens die kunnen jeuken, pijn doen en zelfs gewrichten vastzetten, waardoor alledaagse activiteiten moeilijk worden. Artsen weten dat sommige patiënten veel vatbaarder zijn voor deze hypertrofische littekens dan anderen, maar de huidige voorspellingsinstrumenten zijn grof. Deze studie onderzoekt hoe een "intelligent" maar transparant computersysteem artsen kan helpen voorspellen wie waarschijnlijk ernstige littekens ontwikkelt en vroegtijdig kan ingrijpen om dit te voorkomen.
Voorbij eenvoudige checklisten
Traditionele medische voorspellingsinstrumenten werken vaak als gewogen checklisten: elke risicofactor voegt in een rechte lijn wat toe aan de eindscore. De biologie van slechte littekenvorming na brandwonden is echter allesbehalve eenvoudig. Het omvat een storm van ontsteking, grote weefselschade en het herstelmechanisme van het lichaam dat soms in overdrive raakt. De auteurs volgden 520 volwassenen met ernstige brandwonden die in één ziekenhuis werden behandeld. Van elke patiënt verzamelden zij bij opname 15 gegevens, waaronder brandwondgrootte en -diepte, vroege bloedtests, infectiestatus en hoe lang het duurde voordat ze de operatiekamer bereikten. In plaats van te veronderstellen dat elke factor onafhankelijk werkt, gebruikten ze een moderne patroonzoekmethode om de gegevens complexere relaties te laten onthullen.
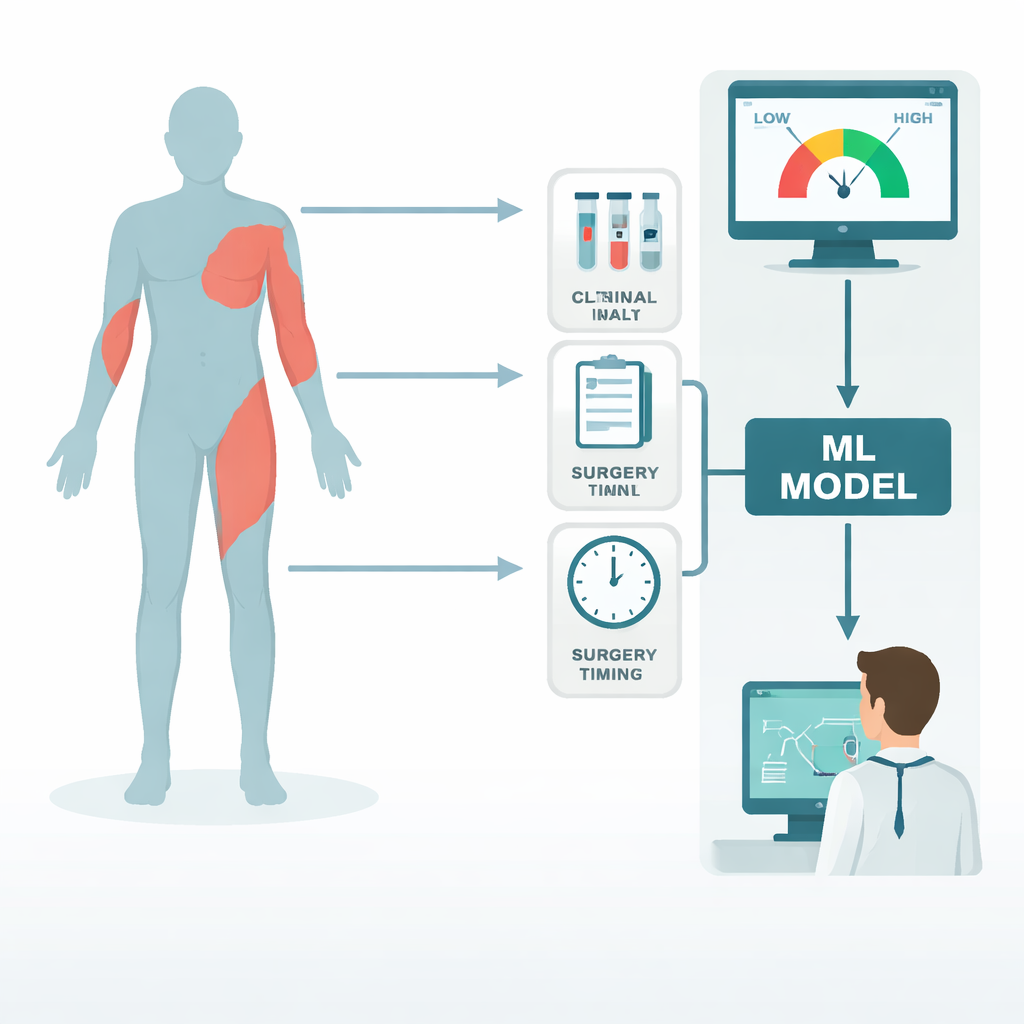
Een intelligente risicocalculator waar je in kunt kijken
Het team vergeleek verschillende typen computermodellen en ontdekte dat een methode bekend als gradient boosting het beste onderscheid maakte tussen patiënten die later dikke littekens ontwikkelden en degenen die dat niet deden. Belangrijk is dat ze niet bij nauwkeurigheid stopten. Ze koppelden het model aan een verklaringsinstrument genaamd SHAP dat voor elke voorspelling laat zien hoeveel elke invoer het risico omhoog of omlaag duwde. In tests op niet eerder geziene patiënten onderscheidde het systeem in de meeste gevallen correct hoge van lage risico’s en was het beter gekalibreerd dan klassieke statistische modellen, wat betekent dat de voorspelde kansen goed overeenkwamen met wat daadwerkelijk gebeurde. Besluitanalyses suggereerden dat het gebruik van dit systeem om preventiestrategieën te sturen meer patiënten zou helpen dan iedereen behandelen of alleen op brandwondgrootte vertrouwen.
Verborgen kantelpunten in ontsteking
Toen de auteurs het "black box"-model openden, verscheen een opmerkelijk patroon: een ontstekingsbloedtest genaamd C-reactief proteïne (CRP) was de sterkste enkele voorspeller van littekenvorming. Maar het effect was niet lineair. Bij matige waarden veranderden schommelingen in CRP het risico nauwelijks. Zodra CRP ongeveer in het bereik van 80–120 mg/L kwam, schoot het door het model geschatte risico omhoog en vormde een S-vormige kromme in plaats van een rechte lijn. Andere markers van systemische stress, zoals grote volledige-dikte brandwondgebieden, hoge leukocytaantallen en laag bloedalbumine, verhoogden ook het risico, terwijl een betere voedingstoestand beschermend leek te werken. Deze bevindingen suggereren dat er praktische ontstekingsdrempels kunnen bestaan waarboven het herstelproces van het lichaam waarschijnlijker blijvende, stijve littekens achterlaat.
Wanneer risicofactoren samenwerken
De studie laat ook zien dat risicofactoren zich niet eenvoudig opstapelen; ze kunnen elkaar versterken. Jonge volwassenen met dezelfde brandwondgrootte als oudere patiënten werden vaker als hoogrisico bestempeld, wat suggereert dat sterkere immuun- en groeiresponsen bij jongeren agressievere littekenvorming kunnen stimuleren. Grote brandwondgebieden en hoge CRP-waarden samen gaven een veel hoger risico dan elk van beide op zichzelf, waarmee het gevaar van een grote brandwond gecombineerd met intense ontsteking wordt onderstreept. Infectie en timing van chirurgie vormden een ander cruciaal paar: bij patiënten zonder wondinfectie veroorzaakte een bescheiden vertraging naar de operatiekamer weinig extra risico, maar bij geïnfecteerde wonden waren vertragingen gekoppeld aan sterk hogere voorspelde risico’s. Deze patronen benadrukken de noodzaak om combinaties van factoren in overweging te nemen, niet alleen losse cijfers in isolatie.
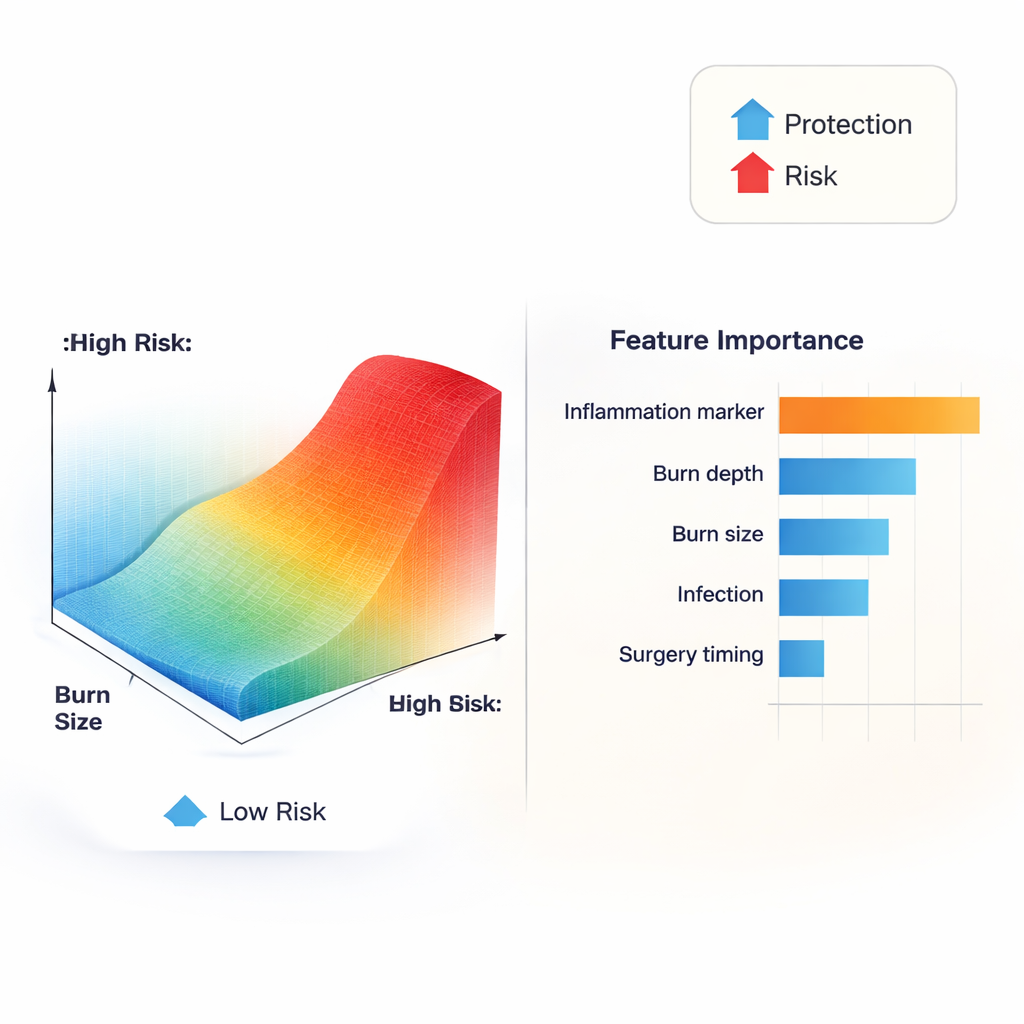
Van complexe data naar beslissingen bij het bed
Om hun werk bruikbaar te maken bouwden de onderzoekers een prototype van een webgebaseerd besluitondersteuningssysteem. Een behandelaar kan routinematige klinische gegevens invoeren en onmiddellijk een geïndividualiseerde schatrisk voor littekenvorming ontvangen. Het systeem toont vervolgens een eenvoudige visuele uitsplitsing die laat zien welke factoren het risico van die patiënt verhogen en welke bescherming bieden. Eén voorbeeldpatiënt had een matige brandwondgrootte maar extreem hoge CRP en een infectie; het hulpmiddel benadrukte duidelijk ontsteking als de belangrijkste boosdoener. Bij een andere patiënt werd het lage risico voornamelijk toegeschreven aan zeer vroege chirurgie. Hoewel het systeem nog getest moet worden in andere ziekenhuizen en over langere follow-upperioden, laat het zien hoe complexe wiskunde kan worden omgezet in duidelijke, patiëntspecifieke richtlijnen.
Wat dit betekent voor patiënten en artsen
Alledaags gesproken suggereert dit onderzoek dat artsen binnenkort een slimmer middel kunnen hebben om vroeg te zien welke overlevenden van brandwonden een aanrijding met ernstige littekenvorming tegemoet gaan. Door verborgen kantelpunten in ontsteking te onthullen en te laten zien hoe leeftijd, brandwondomvang, infectie en behandeltiming elkaar beïnvloeden, gaat het systeem verder dan vuistregels naar gerichte preventie. Als het breder gevalideerd wordt, kan zo’n interpreteerbaar hulpmiddel teams helpen ontstekingsremmende zorg te intensiveren, infectiebeheersing te verscherpen en tijdige chirurgie te prioriteren voor degenen die het het meest nodig hebben, wat uiteindelijk de functie en de kwaliteit van leven na verwoestende brandwonden kan verbeteren.
Bronvermelding: Tian, T., Liu, S. & Ji, G. Interpretable machine learning unveils non-linear inflammatory thresholds and synergistic interactions in post-burn hypertrophic scarring: development of an intelligent clinical decision support system. Sci Rep 16, 6908 (2026). https://doi.org/10.1038/s41598-026-36868-6
Trefwoorden: brandwondenlittekens, ontsteking, machine learning, klinische besluitvorming, precisiegeneeskunde