Clear Sky Science · nl
Farmacokinetiek, pathologie en werkzaamheid van SARS-CoV-2 hoofdproteaseremmer VPC285785 in een muismodel van coronavirusinfectie
Waarom we nog steeds betere COVID-pillen nodig hebben
De eerste antivirale pillen tegen COVID-19, zoals Paxlovid, waren een keerpunt in de pandemie. Maar ze zijn niet perfect: ze moeten zeer vroeg worden ingenomen, vereisen meerdere tabletten per dag en kunnen gevaarlijk interfereren met andere medicijnen. Deze studie onderzoekt nieuwe geneesmiddelkandidaten die het coronavirus op meer dan één manier blokkeren, goed werken als afzonderlijke orale tabletten en minder geneesmiddel‑interacties veroorzaken, met gebruik van een muismodel van coronavirusinfectie.
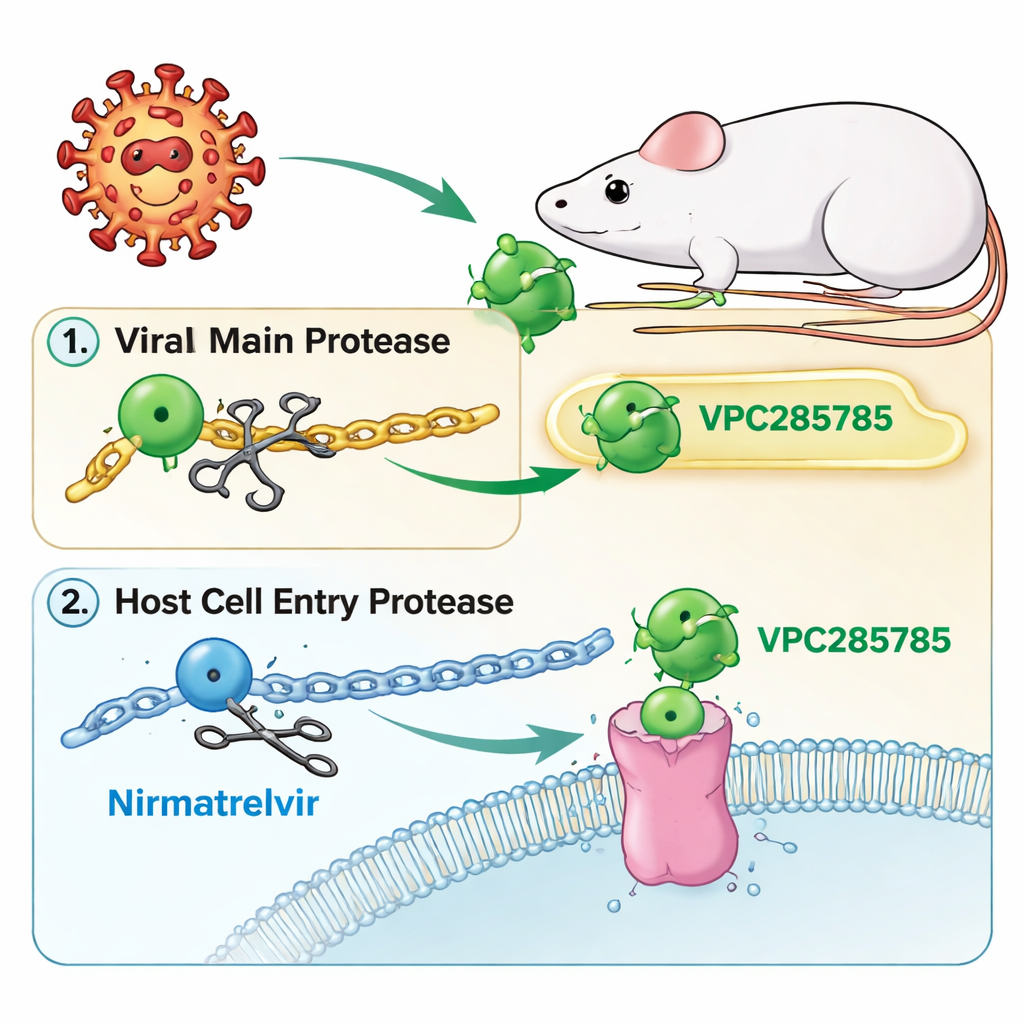
Een nieuwe draai aan het COVID-19 protease‑doelwit
Net als Paxlovid richten de nieuwe verbindingen — VPC285785 en VPC285786 genoemd — zich op het virus’ “hoofdprotease,” een moleculaire schaar die lange virale eiwitten in werkende onderdelen knipt. Als deze schaar vastloopt, kan het virus zichzelf niet afmaken en stokt het proces. De onderzoekers ontwierpen de moleculen ook om een tweede eiwit in onze eigen cellen te remmen, cathepsine L, dat sommige coronavirussen helpt binnen te dringen. Door zowel het virale schaarmechanisme als een gastheercel‑toegangshulp te richten, hoopte het team een dubbelwerkende pil te creëren die moeilijker door het virus te omzeilen is en geen booster‑middel nodig heeft.
Ontworpen voor blijvende werking, niet voor een booster
Paxlovid combineert nirmatrelvir met een ander middel, ritonavir, waarvan de taak niet is het virus te bestrijden maar de afbraak van nirmatrelvir in de lever te vertragen. Ritonavir interfereert echter met veel enzymen die veelvoorkomende medicijnen verwerken, wat leidt tot complexe en soms gevaarlijke interacties. VPC285785 en VPC285786 werden chemisch zo aangepast dat ze zelf minder snel worden afgebroken, met kenmerken zoals fluoratomen en ring‑“versteviging” die ze minder aantrekkelijk maken voor leverenzymen. In laboratoriumtesten met menselijke en muizenleverpreparaten bleken beide nieuwe verbindingen minstens zo stabiel als nirmatrelvir, en VPC285786 was op sommige punten zelfs nog robuuster, zonder dat ritonavir aanwezig was.
Hoe de middelen zich gedragen en bewegen in muizen
Vervolgens onderzochten de onderzoekers hoe de verbindingen door het lichaam van muizen reizen, door te meten hoe snel ze uit het bloed verdwijnen en hoe goed ze via de mond worden opgenomen. Na injectie bleven VPC285785 en VPC285786 ongeveer even lang in de bloedbaan als nirmatrelvir en bereikten ze een hogere totale blootstelling. Bij orale toediening splitsten hun paden zich echter: VPC285785 behaalde een matige maar bruikbare opname (ongeveer 15% van de ingeslikte dosis bereikte de circulatie), terwijl VPC285786 nauwelijks in het bloed terechtkwam (ongeveer 3%). Omdat pillen de darmwand moeten passeren om praktische behandelingen te zijn, werd alleen VPC285785 meegenomen naar de infectie‑experimenten.
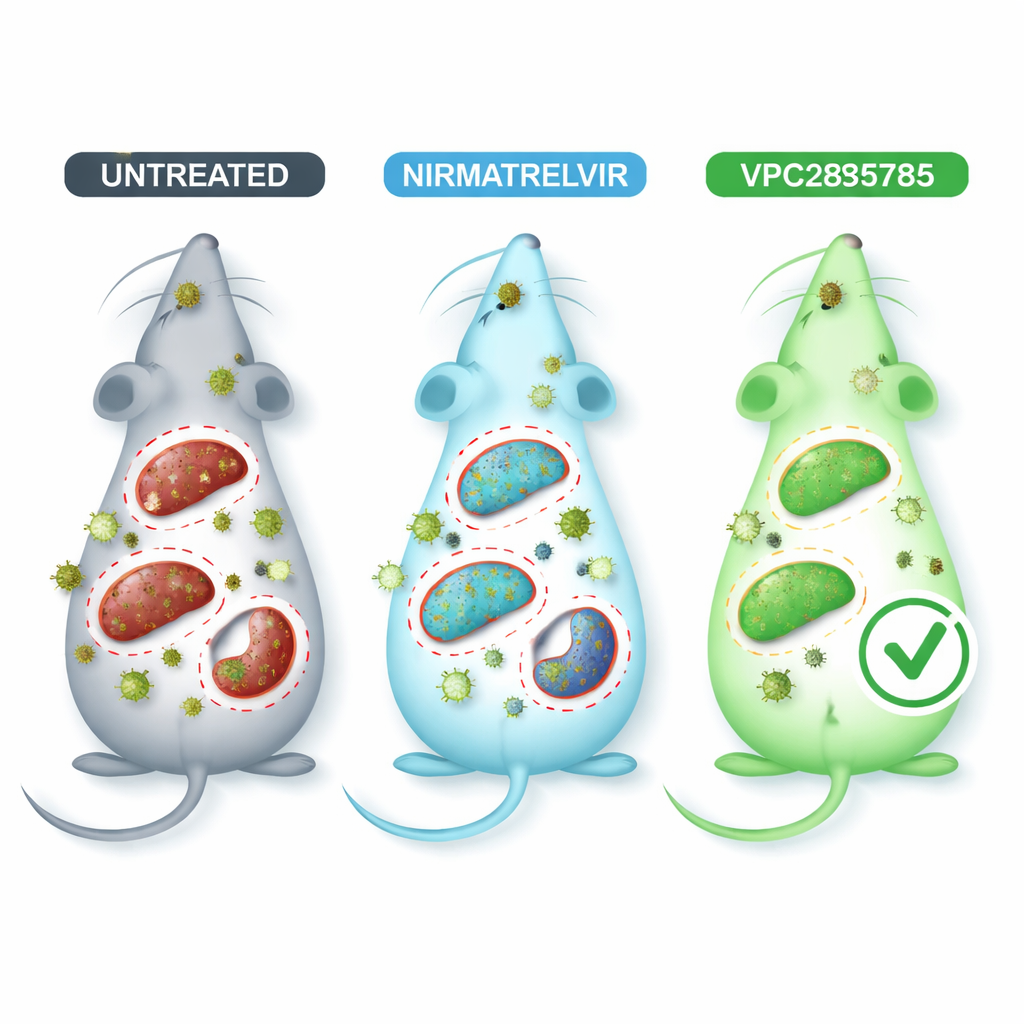
De nieuwe pil testen in geïnfecteerde muizen
Om coronavirusziekte in een veiligere omgeving na te bootsen, gebruikten de onderzoekers een muizencoronavirus genaamd MHV‑A59, dat meerdere organen binnendringt en long‑ en leverbeschadiging veroorzaakt die op veel manieren lijkt op menselijke infectie. Geïnfecteerde muizen werden oraal behandeld met VPC285785, met nirmatrelvir als vergelijking, of met een inactief voertuig. Bloedtesten toonden aan dat de infectie de lever en nieren belastte, maar dieren die VPC285785 of nirmatrelvir kregen, hadden over het algemeen gezondere leverenzym‑ en nierwaarden dan onbehandelde muizen. Het meest opvallend verlaagde VPC285785 sterk de hoeveelheid viraal genetisch materiaal in lever, hersenen en milt, terwijl nirmatrelvir een duidelijke daling alleen in de hersenen liet zien. In de longen, het hart en de nieren maakte geen van beide behandelingen onder de geteste condities een groot verschil.
Wat dit zou kunnen betekenen voor toekomstige COVID‑behandelingen
Hoewel VPC285785 in het reageerbuisje minder krachtig is tegen het virale protease dan nirmatrelvir, presteert het goed in levende dieren, vermindert het virusniveaus in meerdere belangrijke organen aanzienlijk en behoudt het orgaanfunctie — allemaal zonder ritonavir‑booster. Haar zusterverbinding, VPC285786, toont aan dat nog sterkere dubbele targeting van het virale protease en cathepsine L mogelijk is, maar de slechte opname daarvan moet worden verholpen. Gezamenlijk suggereren deze resultaten dat volgende‑generatie COVID‑pillen als enkelvoudige, oraal beschikbare middelen kunnen worden ontworpen die zowel virale als gastheerdoelen raken, minder gevaarlijke interacties met andere medicijnen bieden en toch sterke bescherming in vitale weefsels leveren.
Bronvermelding: Smith, J.R., Toro, A., Sabater, A. et al. Pharmacokinetics, pathology and efficacy of SARS-CoV-2 main protease inhibitor VPC285785 in a murine model of coronavirus infection. Sci Rep 16, 6905 (2026). https://doi.org/10.1038/s41598-026-36842-2
Trefwoorden: SARS-CoV-2 antiviralia, hoofdproteaseremmers, Paxlovid-alternatieven, muizen coronavirusmodel, orale COVID-behandeling