Clear Sky Science · nl
YTHDC1 moduleert het kwaadaardige fenotype van retinoblastoom via SQSTM1-gemedieerde autofagie
Waarom dit belangrijk is voor oogkanker bij kinderen
Retinoblastoom is de meest voorkomende oogkanker bij jonge kinderen. Artsen kunnen het vaak genezen als het vroeg wordt ontdekt, maar zodra de tumor omliggende weefsels binnendringt of richting de hersenen uitzaait, wordt het veel moeilijker zowel het leven als het gezichtsvermogen van het kind te bewaren. Deze studie onderzoekt een moleculaire "rem" in tumorcellen — twee moleculen genaamd YTHDC1 en SQSTM1 — die lijken te helpen retinoblastoom minder agressief te houden. Inzicht in hoe deze rem werkt kan nieuwe wegen openen voor mildere, meer gerichte behandelingen.
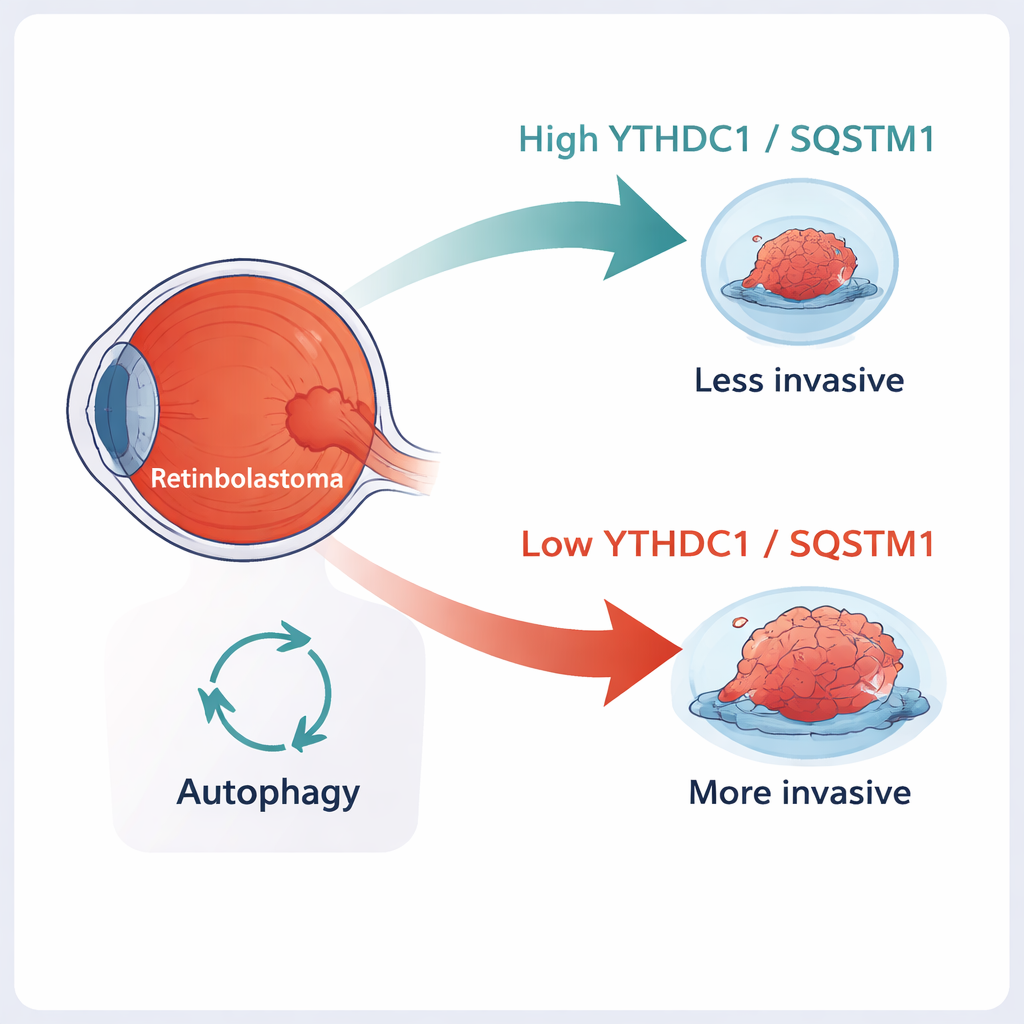
Een nadere blik op oogtumoren bij kinderen
Retinoblastoom ontstaat in de lichtgevoelige laag van het oog, het netvlies, meestal bij kinderen jonger dan vijf jaar. Klassiek begint de ziekte wanneer beide kopieën van een waakzaamheidsgen, RB1, verloren gaan. Maar het verlies van RB1 alleen verklaart niet volledig waarom sommige tumoren in het oog blijven terwijl andere zich in nabijgelegen weefsels ingraven of langs de oogzenuw uitzaaien. Onderzoekers realiseren zich steeds meer dat chemische labels op RNA — de tijdelijke boodschappen die cellen vertellen welke eiwitten ze moeten maken — sterk kunnen beïnvloeden hoe kankers zich gedragen. Een van de meest voorkomende labels, m6A genoemd, kan veranderen hoe stabiel die boodschappen zijn en hoe lang ze in de cel blijven bestaan.
Het ontdekken van een ontbrekende moleculaire rem
De auteurs begonnen met het vergelijken van genetische activiteit in tumoren die binnen het oog bleven met tumoren die al invasief waren geworden. Met een openbaar RNA-sequencing-dataset van retinoblastoommonsters identificeerden ze duizenden genen met verschillende activiteit tussen de twee groepen en concentreerden zich vervolgens op belangrijke m6A-"regulatoren." Dit omvat enzymen die m6A toevoegen of verwijderen en "lezer"-eiwitten die het label interpreteren. Van de tien belangrijkste regulatoren bleek één lezer, YTHDC1, consequent lager te zijn in invasieve tumoren. Toen ze monsters van 50 kinderen onderzochten en laboratoriumtesten op tumormateriaal uitvoerden, bevestigden ze dat de YTHDC1-niveaus — zowel het RNA als het eiwit — verminderd waren in agressievere kankers.
YTHDC1 aan de tand voelen
Om te zien wat YTHDC1 daadwerkelijk doet, manipuleerde het team de niveaus ervan in twee menselijke retinoblastoomcelijnen. Wanneer ze YTHDC1 met genetische hulpmiddelen verlaagden, vermenigvuldigden de cellen zich sneller en konden ze beter door kunstmatige membranen bewegen die weefselbarrières nabootsen — tekenen van een meer invasieve tumor. In muizen vormden cellen zonder YTHDC1 grotere, zwaardere tumoren. Het omgekeerde bleek ook waar: het dwingen van cellen om extra YTHDC1 te produceren vertraagde hun groei en verminderde hun vermogen om te migreren en te infiltreren. Deze experimenten suggereren dat YTHDC1 fungeert als een tumorsuppressor die helpt de gevaarlijkste eigenschappen van retinoblastoom te begrenzen.
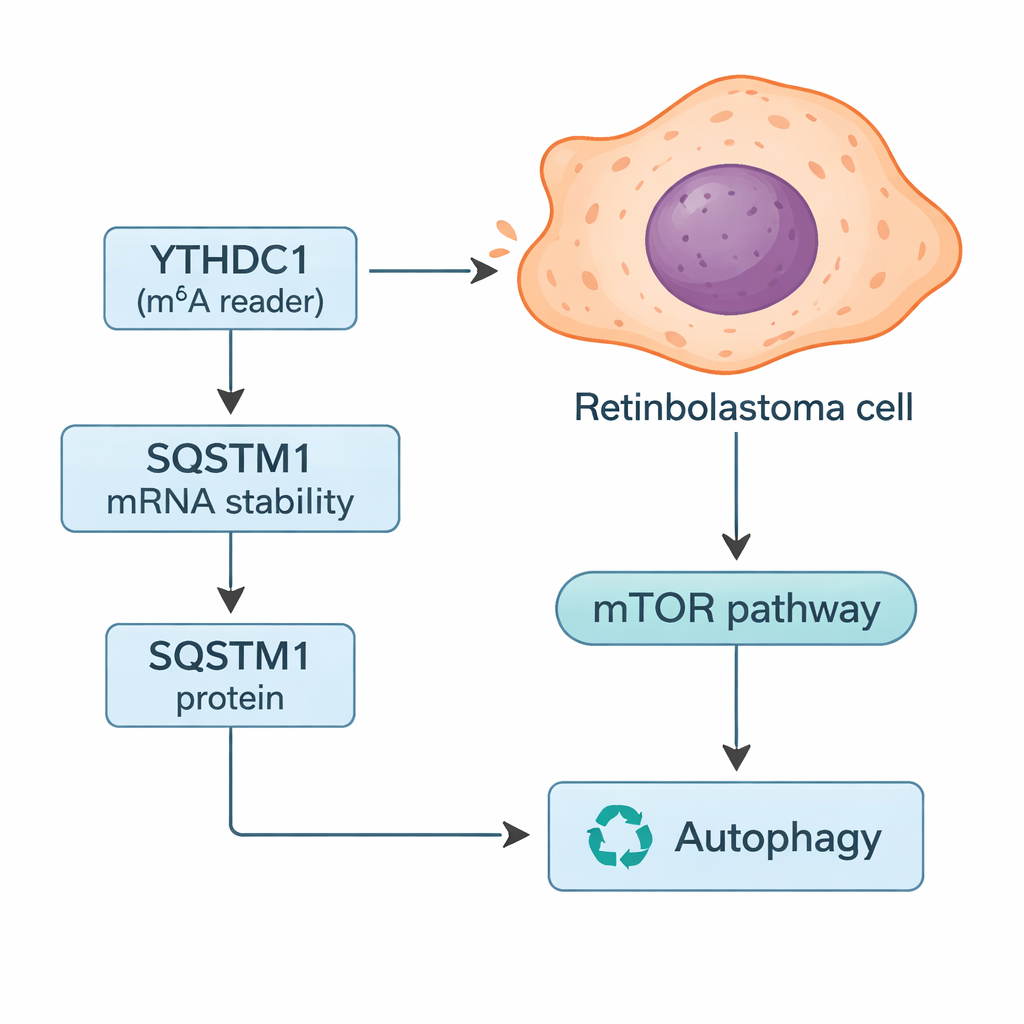
Hoe YTHDC1 het recyclingmechanisme van de cel reguleert
Dieper gravend zochten de onderzoekers naar specifieke genen waarvan de boodschappen mogelijk door YTHDC1 worden gecontroleerd. Door databankzoeken te combineren met hun tumorgegevens, richtten ze zich op SQSTM1, een eiwit dat beter bekend is als p62. SQSTM1 helpt bij het beheren van autofagie, het recyclingmechanisme van de cel dat beschadigde componenten afbreekt en brandstof kan leveren wanneer bronnen schaars zijn. De studie toonde aan dat YTHDC1 fysiek bindt aan het RNA van SQSTM1 en het stabiliseert, waardoor er meer SQSTM1-eiwit kan worden geproduceerd. Wanneer YTHDC1 werd verminderd, daalden de SQSTM1-niveaus en degradeerde het RNA sneller. Het uitschakelen van SQSTM1 alleen zorgde ervoor dat retinoblastoomcellen meer groeiden en invasiever werden, en het veegde gedeeltelijk de beschermende effecten weg die werden gezien wanneer YTHDC1 werd overgeproduceerd, waarmee SQSTM1 als een belangrijke tussenpersoon in deze route werd geplaatst.
Autofagie, energie en tumoragressiviteit
Aangezien SQSTM1 centraal staat in autofagie, testte het team hoe het veranderen van YTHDC1 en SQSTM1 dit recyclingproces beïnvloedde. Met een combinatie van fluorescente markers en eiwitmetingen vonden ze dat het verlagen van YTHDC1 of SQSTM1 de autofagische "flux" verhoogde — er werd meer cellulair materiaal in en door het recyclingsysteem geleid. Ze observeerden ook veranderingen in de mTOR-route, een belangrijke voedingssensor die normaal gesproken autofagie onderdrukt. Met minder SQSTM1 daalde de mTOR-activiteit, wat consistent is met het verhogen van autofagie. In invasief retinoblastoom stellen de auteurs voor dat verlaagde YTHDC1 leidt tot zwakkere SQSTM1-signalen, verminderde mTOR-activiteit en verhoogde autofagie die tumorcellen helpt stress te overleven en zich te verspreiden.
Wat dit betekent voor toekomstige behandelingen
Voor niet-specialisten is de kernboodschap dat deze studie een keten van gebeurtenissen binnen retinoblastoomcellen identificeert — YTHDC1 die SQSTM1 reguleert, wat op zijn beurt het recyclingmachinerie van de cel vormt — die beïnvloedt hoe agressief de kanker wordt. Wanneer deze keten verzwakt is, groeien tumoren sneller en dringen ze meer naar buiten. Hoewel er nog veel werk nodig is voordat deze bevindingen de kliniek kunnen bereiken, biedt de route nieuwe ideeën voor therapie: het herstellen van YTHDC1-functie, het stabiliseren van SQSTM1 of het fijnregelen van autofagie en mTOR-activiteit zou op een dag bestaande chemotherapieën kunnen aanvullen. Voor kinderen met deze oogkanker zouden dergelijke gerichte strategieën kunnen helpen de tumorspreiding te beperken, meer gezichtsvermogen te behouden en de bijwerkingen van behandelingen te verminderen.
Bronvermelding: Ding, J., Sun, J., Wang, J. et al. YTHDC1 modulates the malignant phenotype of retinoblastoma via SQSTM1-mediated autophagy. Sci Rep 16, 6292 (2026). https://doi.org/10.1038/s41598-026-36833-3
Trefwoorden: retinoblastoom, YTHDC1, SQSTM1, autofagie, mTOR-route