Clear Sky Science · nl
Irisin reguleert lipidenmetabolisme en ferroptose in eierstokkankercellen door het ALOX5-5-HETE-PD-L1‑as te moduleren
Waarom dit plantmolecuul van belang is voor eierstokkanker
Eierstokkanker behoort tot de dodelijkste vormen van kanker bij vrouwen omdat het meestal laat wordt ontdekt en vaak terugkeert na behandeling. Deze studie onderzoekt of een natuurlijke verbinding genaamd tectorigenine, aangetroffen in de plant Belamcanda chinensis, eierstokkanker kan vertragen door tumorcellen van bepaalde vetten te beroven en ze te dwingen in een speciale vorm van ijzerafhankelijke celdood te vervallen. Daarnaast onderzoekt het hoe deze verbinding het ‘onzichtbaarheidsmantel’ waarmee tumoren zich tegen het immuunsysteem verbergen, kan verzwakken.
Een verborgen brandstofbron in tumorcellen
Net als veel andere kankers herprogrammeren eierstoktumoren hun vetstofwisseling. In plaats van vetten alleen als energiebron te gebruiken, slaan kankercellen ze op als bouwstenen voor nieuwe membranen en als buffer tegen schade. In in-vitro eierstokkankercellen leidde toevoeging van extra enkelvoudig onverzadigde vetzuren tot een ophoping van vrije vetzuren, triglyceriden en cholesterol — belangrijke vormen van opgeslagen vet. Deze vetoverschotten maakten dat de cellen makkelijker groeiden en invasief werden en hielpen hen weerstand te bieden tegen een destructief proces genaamd ferroptose, waarbij ijzer en geoxideerde vetten samenkomen en celmembranen doen scheuren. Met andere woorden, abnormaal vetmetabolisme gaf de kanker een groeivoordeel en een beschermingslaag.
Het dwingen van kankercellen tot zelfvernietiging
De onderzoekers testten vervolgens tectorigenine op zowel normale eierstokcellen als op meerdere eierstokkankercellijnen. Bij doseringen tot 200 microgram per liter schaadde de verbinding normale cellen niet, maar vertraagde duidelijk de groei van kankercellen, verminderde hun vermogen om door een membraan te invaseren en verhoogde hun snelheid van geprogrammeerde celdood. Toen kankercellen werden voorbehandeld met een ferroptose-blockerend middel, werden ze agressiever. Toediening van tectorigenine keerde deze effecten om: vetvoorraden daalden, niveaus van ijzer- en oxidatieschade-indicatoren stegen en meer cellen stierven. In muismodellen met humane eierstoktumoren krompen tumoren na injecties met tectorigenine, nam het vetgehalte in tumorweefsel af en namen chemische tekenen van ferroptose toe, wat opnieuw suggereert dat de verbinding kankercellen naar deze ijzerafhankelijke doodsroute duwt.
Een belangrijke moleculaire schakel tussen vetten en immuunontsnapping
Om te achterhalen hoe tectorigenine op moleculair niveau werkt, combineerde het team big-data-analyse met computermodellering van medicijn–eiwitinteracties. Ze richtten zich op een enzym genaamd ALOX5, dat een veelvoorkomend vetzuur omzet in een signaalmolecuul genaamd 5‑HETE. In eierstokkankercellen en tumormonsters waren de ALOX5-niveaus veel hoger dan in normaal weefsel. Computer docking en moleculaire dynamicasimulaties lieten zien dat tectorigenine stabiel kan binden aan ALOX5 en als een interne rem fungeert. Wanneer de onderzoekers ALOX5 kunstmatig verhoogden in kankercellen, namen vetvoorraden toe, daalden ferroptose‑markers en werden de cellen invasiever. Behandeling met tectorigenine keerde deze veranderingen om. Het onderdrukken van ALOX5 had het tegenovergestelde effect—minder vet, meer ferroptose en verminderde groei—waardoor dit enzym centraal kwam te staan in de werking van de verbinding.
Hoe tumoren hun schild tegen het immuunsysteem verliezen
De studie koppelde deze vetroute ook aan een belangrijk immuuncheckpointeiwit genaamd PD‑L1, dat tumoren gebruiken om aanvallende immuuncellen uit te schakelen. Het product van ALOX5, 5‑HETE, verhoogde PD‑L1-niveaus en versterkte dit schild. Toen ALOX5 werd uitgeschakeld, daalden zowel 5‑HETE als PD‑L1; bij herintroductie van 5‑HETE steeg PD‑L1 weer en herwonnen kankercellen een deel van hun bescherming tegen ferroptose. Tectorigenine verlaagde ALOX5, verminderde 5‑HETE en verlaagde daardoor PD‑L1 in celculturen en muizen tumoren. Dit suggereert dat door één enkel metabolisch enzym aan te spreken, de verbinding zowel de vetgebaseerde verdediging van de kanker kan verstoren als haar vermogen om zich aan immuunaanvallen te onttrekken kan verzwakken.
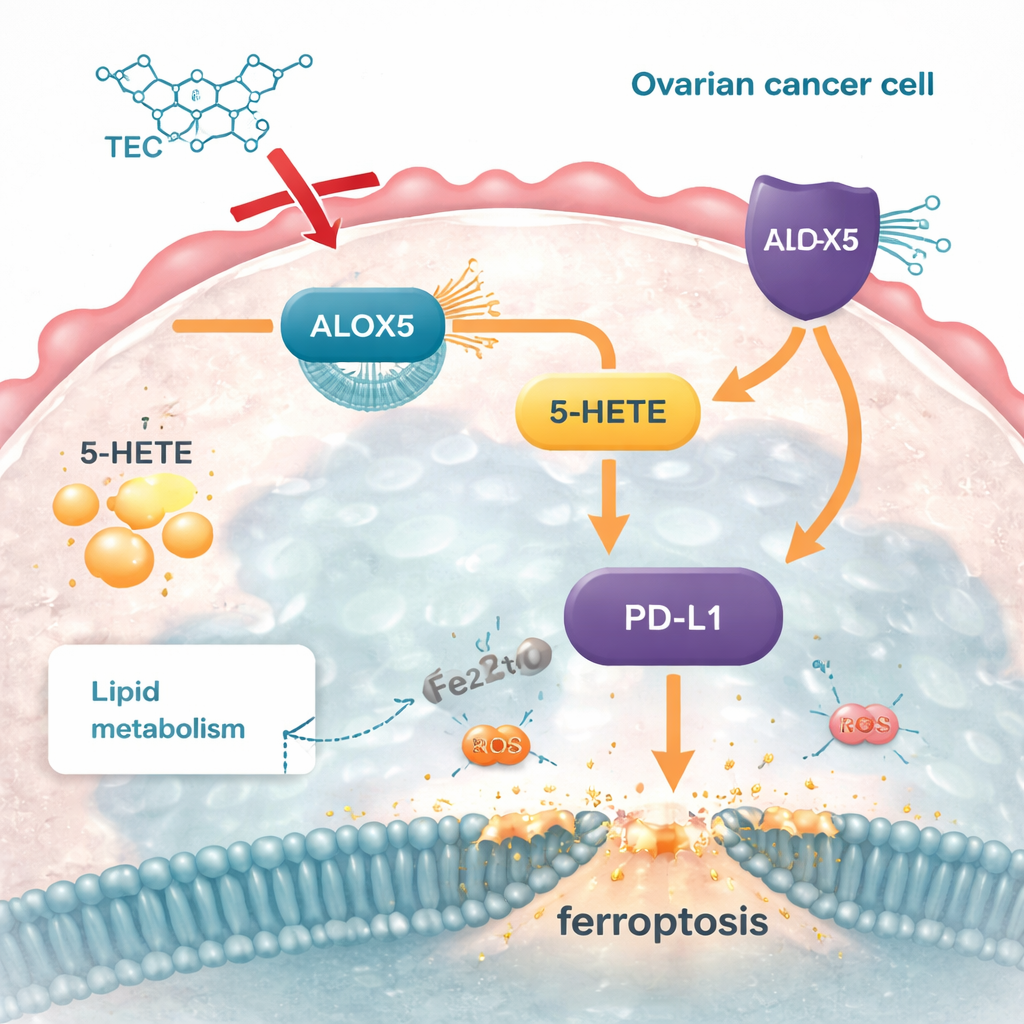
Wat dit kan betekenen voor toekomstige behandelingen
Kort gezegd toont dit werk aan dat tectorigenine fungeert als een precisiere sleutel die in de vetverwerkingsmachine van een kankercel wordt gegooid. Door ALOX5 te blokkeren, stopt het de productie van 5‑HETE, vermindert het overtollige vetvoorraden, maakt het cellen kwetsbaar voor ijzergedreven schade en ontdoet het hen van een deel van hun immuuncamouflage. Hoewel deze bevindingen afkomstig zijn uit cel- en muisonderzoek—en er veel moet worden getest bij mensen—wijzen ze op een veelbelovende strategie: het richten op de ALOX5–5‑HETE–PD‑L1‑as om zowel eierstoktumoren uit te hongeren als ze toegankelijker te maken voor het eigen immuunsysteem of toekomstige immunotherapieën.
Bronvermelding: Cai, H., Huang, C. & Zhang, Z. Irisin regulates lipid metabolism and ferroptosis in ovarian cancer cells by modulating the ALOX5-5-HETE-PD-L1 axis. Sci Rep 16, 7223 (2026). https://doi.org/10.1038/s41598-026-36816-4
Trefwoorden: eierstokkanker, lipidenmetabolisme, ferroptose, ALOX5, natuurlijke verbinding therapie