Clear Sky Science · nl
Experimentele karakterisering van proton-minibeamtherapie bij FLASH-dosisnelheidscondities
Snelere, zachtere stralingsbundels
Radiotherapie is een pijler van de kankerbehandeling, maar kan gezond weefsel naast tumoren beschadigen. Deze studie onderzoekt een nieuwe manier om protonstraling toe te dienen die erop gericht is tumoren hard aan te pakken terwijl de impact op normale organen wordt verzacht. Door twee opkomende ideeën te combineren — zeer fijn verdeelde “minibeams” en ultra-snelle FLASH-dosisniveaus — tonen de onderzoekers aan dat het technisch mogelijk is om zeer precieze behandelingen in slechts enkele seconden te geven met apparatuur die vergelijkbaar is met wat al in moderne ziekenhuizen aanwezig is.
Waarom straling in piepkleine bundels verdelen?
Traditionele bestralingsvelden lijken glad: de dosis is redelijk gelijkmatig verdeeld over het behandelde gebied. Ruimtelijk gefractioneerde radiotherapie doorbreekt dat principe bewust. Bij proton-minibeamradiotherapie wordt de straling opgesplitst in vele dunne, submillimeterbundels die door openingen van elkaar zijn gescheiden. Dicht bij het oppervlak ontstaat hierdoor een patroon van hoge dosis “pieken” en lage dosis “dalen”. Het gezonde weefsel tussen de pieken heeft een betere kans om zichzelf te herstellen, terwijl dieper in het lichaam de bundels uitwaaieren en overlappen, waardoor de tumor een meer uniforme en effectieve dosis ontvangt. Vroege laboratorium- en dierstudies suggereren dat dit patroon bijwerkingen kan verminderen en mogelijk zelfs nuttige immuunreacties tegen kanker kan opwekken.
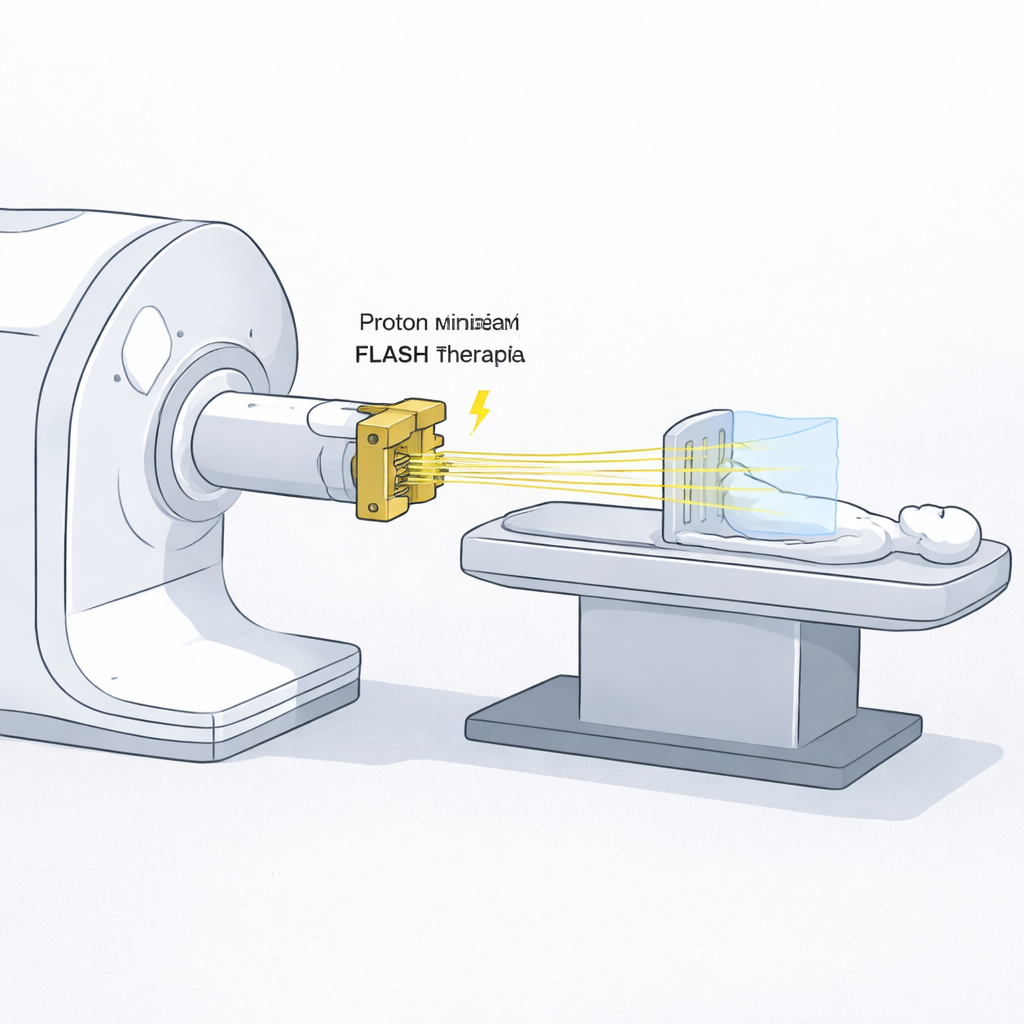
Wat is FLASH, en waarom doet snelheid ertoe?
FLASH-therapie is een nieuwe manier om naar de tijdsdimensie van stralingslevering te kijken. In plaats van een dosis langzaam over tientallen seconden of minuten toe te dienen, levert FLASH dezelfde dosis in een fractie van een seconde bij ultra-hoge dosisniveaus — tientallen tot honderden gray per seconde. Verrassend genoeg hebben veel experimenten aangetoond dat normaal weefsel onder deze extreme condities beter kan worden gespaard, terwijl tumoren even kwetsbaar blijven. Voor proton-minibeams bestond er echter een praktisch obstakel: de metalen multi-slitblokken die gebruikt worden om de bundel in dunne stralen te verdelen verspillen veel van de binnenkomende deeltjes, waardoor behandelingen enkele minuten kunnen duren. Als minibeams in FLASH-modus konden worden toegediend, zou de verloren tijd mogelijk kunnen worden teruggewonnen en zouden de biologische voordelen van beide methoden gecombineerd kunnen worden.
Minibeams en FLASH op een klinische machine toepassen
Het team werkte met een compact klinisch protonensysteem dat patiënten gewoonlijk behandelt met een glad, scannend protonenbundel. Ze bevestigden op maat gemaakte multi-slitcollimatoren van messing — elk met vijf smalle spleten van slechts 1 millimeter breed en 2,8 millimeter van elkaar — aan het uiteinde van de behandelmond. Door de bundelstroom te verhogen en de bundeloptica zorgvuldig af te regelen, lieten ze het systeem werken in een ultra-hoge-dosis-snelheidsmodus bij 228 MeV, terwijl ze nog steeds terug konden schakelen naar gewone klinische instellingen. Vervolgens maten ze hoe de dosis werd verdeeld in waterachtige kunststofblokken met speciale radiosensitieve films en vergeleken die metingen met gedetailleerde computersimulaties die individuele protoninteracties volgen.
Hoe presteerde de nieuwe bundel?
Onder FLASH-condities behield de protonenbundel een duidelijk minibeampatroon: scherpe pieken langs de spleetpaden en diepe dalen ertussen. De metingen en simulaties kwamen nauw overeen wat betreft hoe dit patroon zich met diepte ontwikkelde en hoe snel het vervaagde door verstrooiing van de bundels. Een dikkere collimator van 10 cm gaf een schonere scheiding tussen pieken en dalen dan een versie van 6,5 cm, vooral nabij het oppervlak, wat betekent dat de “dal”-gebieden beter werden beschermd. Cruciaal was dat het draaien van de machine in FLASH-modus de levertijd voor een typisch minibeamveld van 3 bij 3 centimeter reduceerde van ongeveer 3 minuten tot slechts 2,5 seconden. Berekeningen op basis van de timinglogs van de machine toonden aan dat de lokale dosissnelheden in de piekregio’s gemakkelijk de veelgebruikte FLASH-drempels overschreden, terwijl de fijne ruimtelijke structuur van de minibeams behouden bleef.
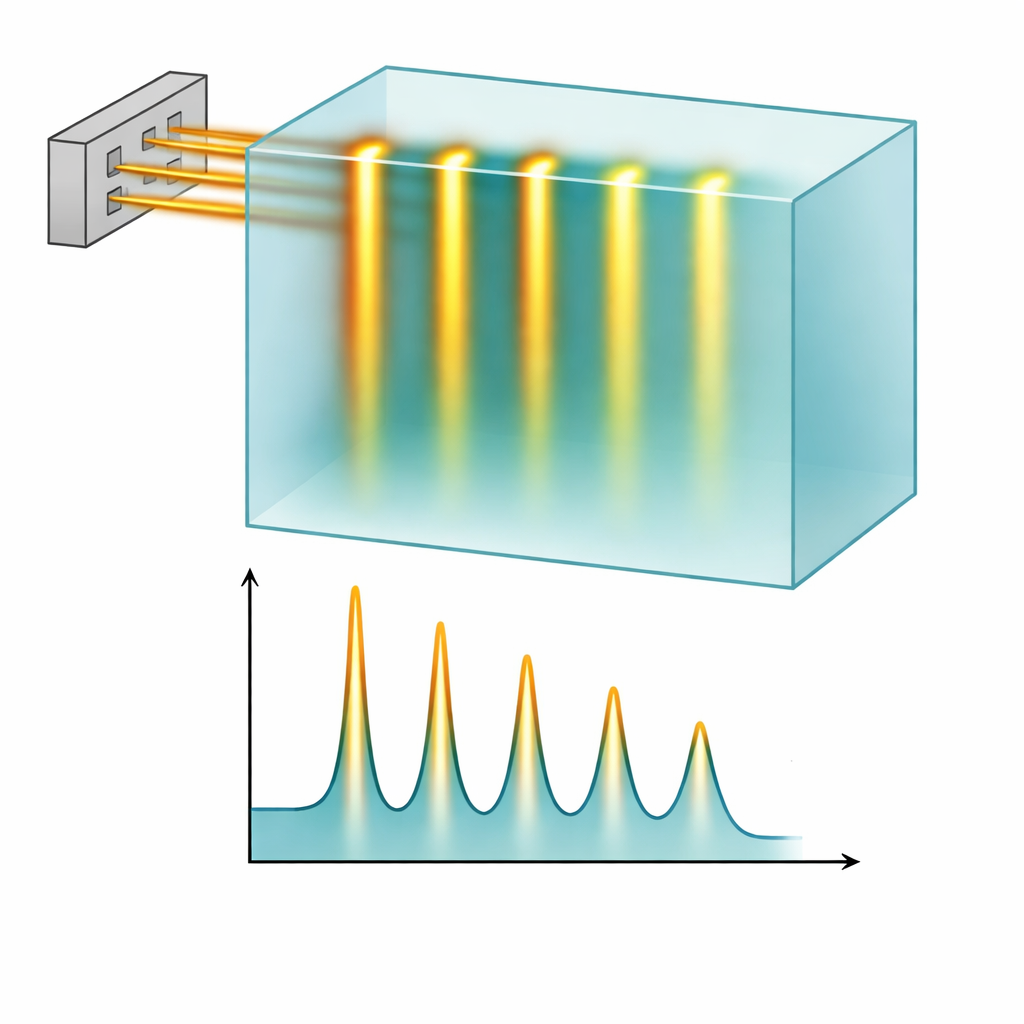
Wat dit kan betekenen voor toekomstige kankerzorg
Dit werk is een vroege maar belangrijke proof of principle. Het toont aan dat een standaard klinisch protonentherapiesysteem kan worden aangepast om proton-minibeams bij FLASH-dosisniveaus te leveren zonder in te boeten aan precisie of bundelkwaliteit. Patiënten worden nog niet op deze manier behandeld: de experimenten zijn gedaan in testopstellingen en er werd slechts één hoogenergetische bundel gebruikt, in plaats van de gelaagde energiemodi die echte tumoren vereisen. De biologische effecten van het combineren van ruimtelijke minibeampatronen met ultra-snelle FLASH-toediening moeten ook nog worden bewezen in diermodellen en uiteindelijk bij mensen. Toch legt de studie het technische fundament voor toekomstige behandelingen die tumoren mogelijk even effectief kunnen beheersen als de beste huidige methoden, terwijl ze door slim te doseren — zowel in ruimte als in tijd — de schade aan gezonde organen drastisch kunnen verminderen.
Bronvermelding: Lin, Y., Wu, W., Setianegara, J. et al. Experimental characterization of proton minibeam therapy delivery under FLASH dose-rate conditions. Sci Rep 16, 7803 (2026). https://doi.org/10.1038/s41598-026-36739-0
Trefwoorden: protontherapie, FLASH-radiotherapie, minibeamstraling, kankerbehandeling, stralingsdosissnelheid