Clear Sky Science · nl
Profaag-gecodeerd RexAB-achtig fage-afweersysteem in Pseudomonas putida
Verborgen lijfwachten die in bacteriën leven
Bacteriën worden voortdurend bejaagd door virussen die fagën worden genoemd en hele microbiële populaties kunnen uitroeien. Deze studie onderzoekt hoe “slapende” virussen die al in het DNA van een bacterie verborgen zitten, stiekem als lijfwachten kunnen optreden door geïnfecteerde cellen op te offeren om de rest te redden. Het begrijpen van deze natuurlijke verdedigingstrucs is van belang voor fagentherapieën, biotechnologie en voor het betrouwbaar laten functioneren van industriële microben.
Virussen die van vijanden bondgenoten worden
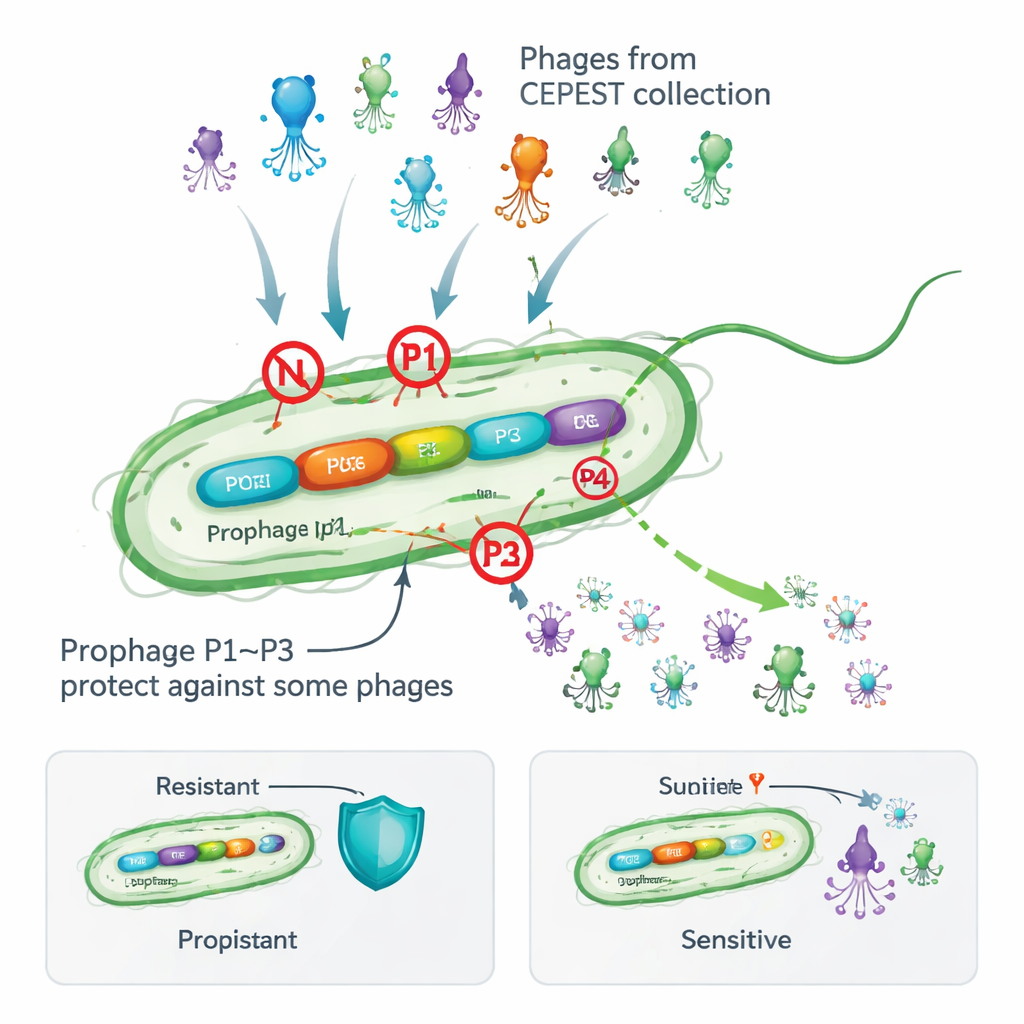
Veel bacteriën dragen temperente fagën in een slapende vorm die profaag wordt genoemd, ingebed in hun chromosomen. Op het eerste gezicht lijkt dat riskant: deze virale meerijders kunnen wakker worden en de gastheercel beschadigen, en ze maken het genoom omvangrijker. Toch tonen onderzoeken van duizenden bacteriële genomen dat de meeste soorten zulke profaagjes behouden, wat erop wijst dat ze voordelen bieden. Eerder werk aan de bodembacterie Pseudomonas putida toonde dat het verwijderen van haar vier cryptische (niet‑productieve) profaagjes de cellen kwetsbaarder maakte voor een experimentele verzameling fagën genaamd CEPEST. Dat suggereerde dat de profaagjes anti‑fagewapens dragen, maar de precieze genen en mechanismen waren onbekend.
Drie bewoners bieden gerichte bescherming
De auteurs ontwierpen systematisch welk aandeel elk profaag leverde door ze één voor één te verwijderen en te testen hoe goed 26 verschillende CEPEST‑fagën plaques konden vormen op bacteriële lawns. Ze vonden dat profaagjes genaamd P1, P2 en P3 elk bescherming bieden, maar alleen tegen specifieke groepen fagën, terwijl P4 neutraal lijkt. P1 alleen kan infectie door sommige fagën ruwweg duizendmaal verminderen, P2 biedt een gematigdere bescherming, en P3 is spectaculair effectief — maar alleen tegen bepaalde reusachtige “jumbo” fagën. In de meeste gevallen verklaart een enkel profaag het waargenomen resistentiepatroon, al lijken bij enkele fagën meerdere profaagjes samen te werken. Deze resultaten tonen dat zelfs “stille” profaagjes kunnen fungeren als een op maat gemaakt schild, afgestemd op specifieke virale bedreigingen.
Het opsporen van een moleculaire alarm van twee delen
Met de focus op de sterke en relatief brede bescherming die P1 biedt, verwijderde het team systematisch blokken van P1‑genen totdat de verdediging verdween. Door de zoektocht te verfijnen ontdekten ze dat het verlies van slechts twee aangrenzende genen, PP_5643 en PP_5644, de cellen even gevoelig maakte als wanneer de gehele P1‑profaag was verdwenen. Bioinformatica toonde aan dat PP_5643 lijkt op RexA, een DNA‑bindend eiwit uit klassieke lambda‑fagestudies, terwijl PP_5644 lijkt op een membraaneiwit met meerdere helixsegmenten die een porie zouden kunnen vormen, vergelijkbaar met RexB. Samen komt dit paar overeen met een bekend type “abortief infectiesysteem”: zodra een specifiek faag wordt gedetecteerd, stopt de geïnfecteerde cel opzettelijk zijn eigen groei zodat het virus zich niet kan vermenigvuldigen en zich naar buren kan verspreiden.
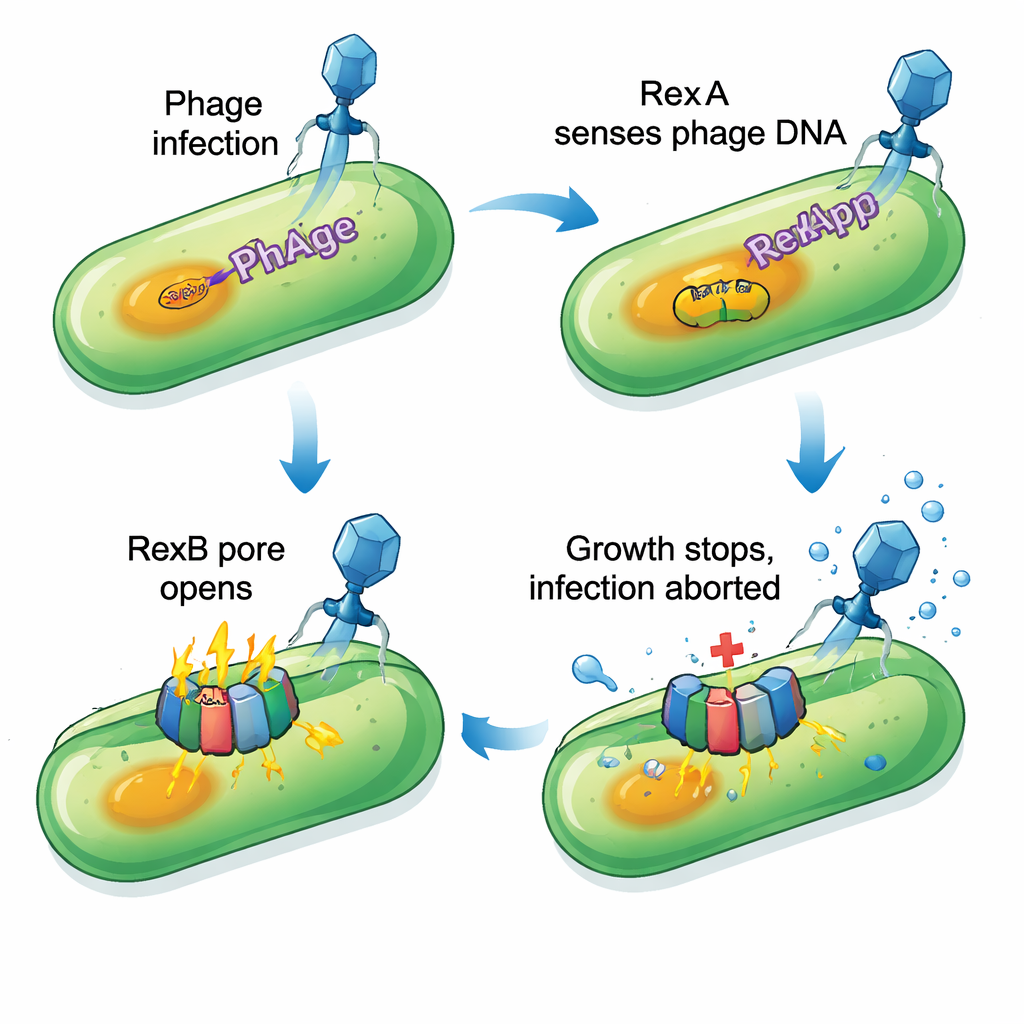
Hoe de verdediging geïnfecteerde cellen saboteert
Experimenten bevestigden dat de P1‑variant van RexA (RexApp genoemd) DNA bindt zonder sterk te letten op de exacte sequentie, waardoor het goed geschikt is om abnormale DNA‑structuren te herkennen die tijdens virale replicatie ontstaan. Het partner‑eiwit RexBpp is ingebed in het celmembraan. Wanneer RexApp kunstmatig in overmaat wordt geproduceerd, vertonen cellen die nog steeds het rexBpp‑gen dragen ernstige groeistilstand en tekenen van membraanschade: kleurstoffen die normaal niet door intacte membranen dringen, komen plots binnen, en kleine hoeveelheden van een cytoplasmatisch enzym lekken weg. Als rexBpp ontbreekt of gemuteerd is, schaadt overproductie van RexApp de cellen niet meer. Dit duidt erop dat RexApp als trigger fungeert, terwijl RexBpp de effector is die de celomhulling beschadigt. Interessant genoeg barsten de meeste aangetaste cellen niet volledig; in plaats daarvan gaan ze in een sterk vertraagde, bijna stationaire toestand die onverenigbaar lijkt met fagevermeerdering.
Waarom het opgeven van een paar cellen de populatie kan redden
Het beeld dat naar voren komt is dat van een altruïstische verdediging: wanneer een gevoelige faag P. putida infecteert, detecteert RexApp waarschijnlijk virale DNA–eiwitcomplexen en schakelt RexBpp in, dat het membraan beschadigt en de groei abrupt stopt. De geïnfecteerde cel betaalt de prijs, maar de levenscyclus van het faag wordt afgebroken en de bredere bacteriële gemeenschap wordt beschermd. Systemen van dit RexAB‑type zijn tot nu toe in slechts een handvol verschillende fagën gevonden, maar ze delen dezelfde kernlogica — een intracellulaire sensor gekoppeld aan een membraan‑effector die snel een productieve cel in een doodlopende weg voor het virus kan veranderen. Voor bacteriën kan het behouden van cryptische profaagjes die zulke verdedigingsmodules dragen, de kosten van het herbergen van viraal DNA compenseren en hen helpen overleven in een wereld waar fagën overal aanwezig zijn.
Bronvermelding: Rosendahl, S., Kängsep, A., Ainelo, A. et al. Prophage-encoded RexAB-type phage defense system in Pseudomonas putida. Sci Rep 16, 5898 (2026). https://doi.org/10.1038/s41598-026-36734-5
Trefwoorden: bacteriofaagafweer, profaag, Pseudomonas putida, abortieve infectie, RexAB-systeem