Clear Sky Science · nl
Ontwikkeling en validatie van een PSMA-positief triple-negatief borstkankermuismodel voor preklinische gerichte radionuclide-therapieën
Waarom dit onderzoek ertoe doet
Triple-negatieve borstkanker is een van de moeilijkst te behandelen vormen van borstkanker. Ze verspreidt zich vaak snel, biedt patiënten minder gerichte behandelingsopties en keert vaak terug na standaardtherapieën. Tegelijkertijd heeft een nieuwe klasse “slimme” radioactieve geneesmiddelen die zich richten op een specifiek molecuul genaamd PSMA de zorg voor gevorderde prostaatkanker getransformeerd. Deze studie stelt een eenvoudige maar krachtige vraag: kunnen we een realistisch laboratoriummodel van triple-negatieve borstkanker maken dat hetzelfde PSMA-doel draagt, zodat we op een eerlijke manier kunnen testen of deze slimme radioactieve middelen ook patiënten met deze agressieve borstkanker kunnen helpen?
Van prostaatdoel naar borstkankeruitdaging
PSMA, afkorting van prostate-specific membrane antigen, is een kleine structuur die op het oppervlak van bepaalde cellen zit. Het komt overvloedig voor in veel prostaatkankers en kan worden herkend door radioactieve middelen die tumoren zowel zichtbaar maken op scans als direct bestralen. Onderzoekers hebben onlangs ontdekt dat PSMA ook in wisselende mate voorkomt in de bloedvaten en cellen van verschillende andere kankers, waaronder triple-negatieve borstkanker. Bij deze niet-prostaattumoren is PSMA echter vaak ongelijk verdeeld en zwakker, waardoor het moeilijk is vast te stellen of PSMA-gerichte therapieën effectief zullen zijn. Voordat nieuwe behandelingen bij patiënten worden geprobeerd, hebben wetenschappers diermodellen nodig die dit PSMA-patroon in borstkankers trouw nabootsen—iets wat verrassend moeilijk te bereiken is geweest.
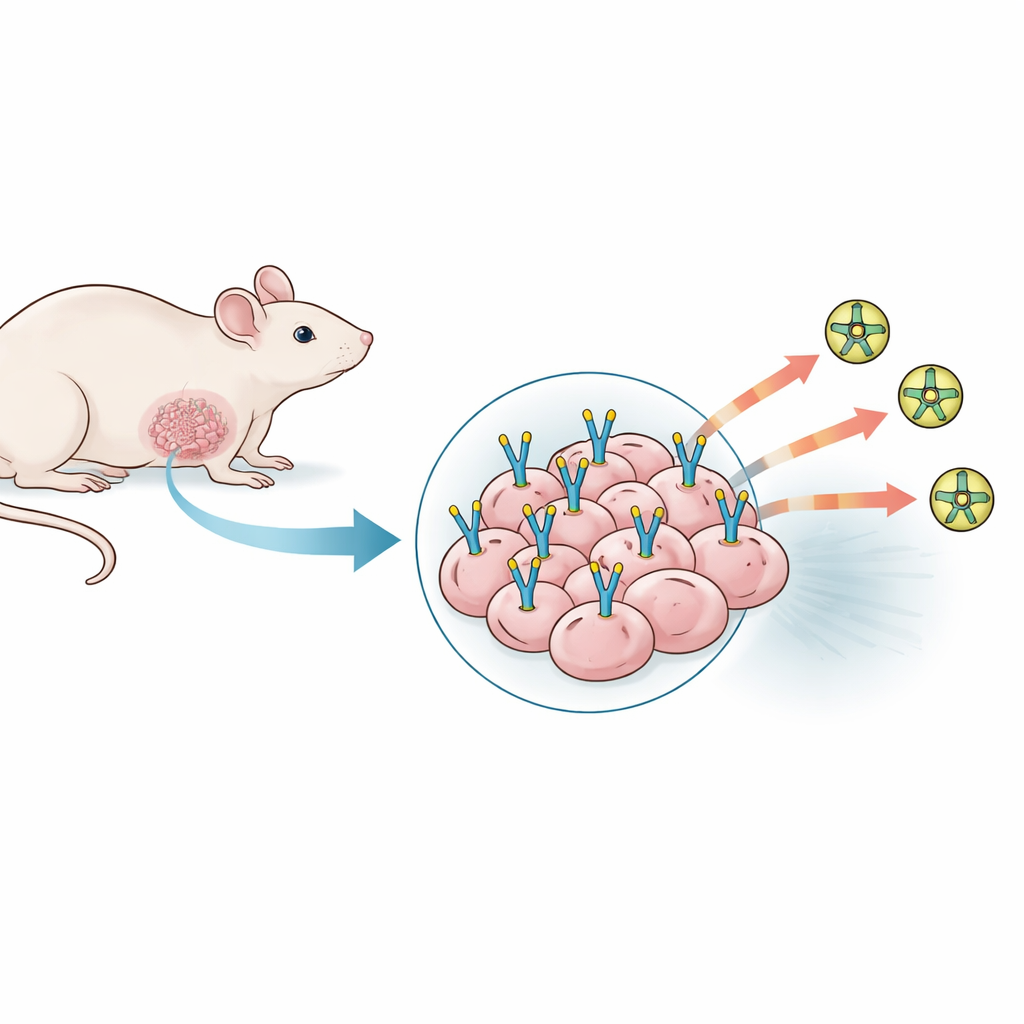
Het testen van vele tumor-modellen die niet wilden meewerken
Het team onderzocht eerst een breed scala aan bestaande muismodellen van triple-negatieve borstkanker, met zowel muis- als menselijke kankercellijnen die op verschillende plaatsen en onder uiteenlopende condities werden ingebracht. Ze varieerden het aantal geïnjecteerde kankercellen, voegden ondersteunende gels toe om de bloedvatgroei te bevorderen en mengden zelfs menselijke bloedvatcellen door in de hoop PSMA-niveaus te verhogen. Voor elk model bepaalden ze hoe betrouwbaar tumoren zich vestigden en groeiden, inspecteerden tumorplakjes onder de microscoop en gebruikten een PSMA-zoekende PET-tracer om te zien of de tumoren op full-body scans oplichtten. Ondanks sterke tumorgroei en rijke netwerken van bloedvaten toonde geen van deze 23 modellen een noemenswaardige aanwezigheid van PSMA, noch bij weefselkleuring noch bij PET-beeldvorming. De tumoren leken actief en goed doorbloed, maar de specifieke PSMA-‘aankoppelplaats’ die de onderzoekers nodig hadden, ontbrak in wezen.
Een tumor ontwerpen die het juiste doel toont
Geconfronteerd met deze blokkade namen de onderzoekers een directere route. Ze pasten genetische modificatie toe op een veelgebruikte menselijke triple-negatieve borstkankercellijn, MDA-MB-231, zodat deze geforceerd PSMA op het celoppervlak ging produceren. Deze gewijzigde cellen werden vervolgens geïmplanteerd in het borstvetkussen van immuundeficiënte muizen, een locatie die de natuurlijke borstomgeving beter nabootst. De wetenschappers creëerden twee versies van het model: één waarbij alle tumorcellen PSMA uitdrukten, en een andere ‘gemengde’ tumor die voor de helft uit PSMA-positieve en voor de helft uit gewone kankercellen bestond, om de ongelijkmatige patronen die bij patiënten worden gezien na te bootsen. Beide modellen vormden net zo betrouwbaar tumoren en groeiden in een vergelijkbaar tempo als tumoren van ongemodificeerde cellen, wat aantoont dat het toevoegen van PSMA het gedrag van de kanker zelf niet merkbaar veranderde.
Het nieuwe doel zien op scans en onder de microscoop
Wanneer de PSMA-zoekende PET-tracer in deze muizen werd geïnjecteerd, staken de gemodificeerde tumoren fel af op de scans, met tumoropname die ongeveer tien keer hoger was dan in de lever of spier. Dit sterke en selectieve signaal bevestigde dat PSMA nu overvloedig aanwezig was op de kankercellen en bereikbaar was voor een circulerend middel. Microscopische analyse van tumormateriaal bevestigde dit: PSMA-kleuring was hoog maar ongelijkmatig, met vlekken van sterker en zwakker tot expressie, wat lijkt op het heterogene patroon dat wordt waargenomen in menselijke triple-negatieve borstkankers. Belangrijk is dat het toegevoegde PSMA beperkt bleef tot tumorcellen en niet in omringende bloedvaten voorkwam, waardoor het model zich concentreert op celgerichte therapieën. Gebieden met afgestorven weefsel in grotere tumoren namen de tracer niet op, wat overeenkomt met klinische observaties.
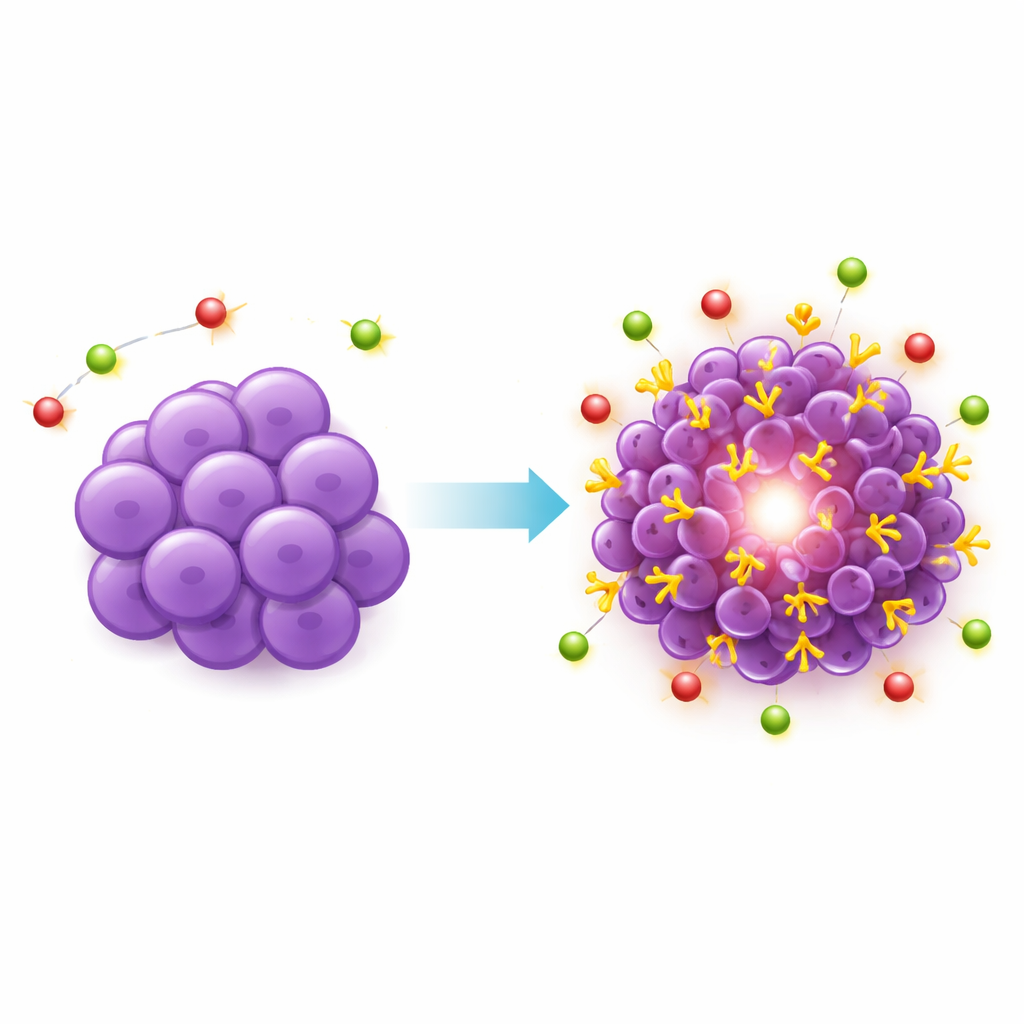
Wat dit betekent voor toekomstige behandelingen
Door systematisch aan te tonen dat standaard muismodellen van borstkanker PSMA niet betrouwbaar tot expressie brengen en vervolgens een nieuw model te bouwen dat dat wel doet, biedt dit werk een cruciale testomgeving voor volgende generatie gerichte radioactieve behandelingen. Het PSMA-positieve triple-negatieve borstkankermodel is stabiel, groeit voorspelbaar en toont een realistische mix van hoge en lage PSMA-gebieden, waardoor het goed geschikt is om te evalueren hoe PSMA-gerichte middelen zich gedragen voordat ze bij patiënten worden geprobeerd. Hoewel dit model niet elk aspect van de menselijke ziekte kan vatten—zoals de invloed van een volledig functionerend immuunsysteem—biedt het een krachtig instrument om te onderzoeken of het succes van PSMA-gebaseerde therapieën bij prostaatkanker ooit kan worden uitgebreid naar mensen die leven met deze bijzonder agressieve vorm van borstkanker.
Bronvermelding: Chaussin, B., Sanchez, L., Levesque, S. et al. Development and validation of a PSMA-positive triple-negative breast cancer mouse model for preclinical targeted radionuclide therapies. Sci Rep 16, 9348 (2026). https://doi.org/10.1038/s41598-026-36724-7
Trefwoorden: triple-negatieve borstkanker, PSMA, gerichte radionuclide-therapie, preklinisch muismodel, PET-beeldvorming