Clear Sky Science · nl
Verlaging van de lange isoform van de WNK1-kinase vermindert anti-basale membraan glomerulonefritis bij muizen
Waarom dit belangrijk is voor de niergezondheid
Snel progressieve nierziekten kunnen de kleine filters van het orgaan binnen enkele weken vernietigen, wat vaak leidt tot dialyse of een transplantatie. Deze studie onderzoekt of het terugschakelen van één eiwit, L-WNK1 genoemd, die vernietiging bij muizen kan vertragen. Omdat er al geneesmiddelen tegen dit eiwit worden ontwikkeld voor bloeddrukproblemen, wijzen de bevindingen op een mogelijke nieuwe manier om nieren te beschermen die worden aangevallen.
Een verkeersregelaar binnen de nierfilters
Elke nier bevat honderdduizenden microscopische filters, of glomeruli, die het bloed reinigen. Binnen deze filters werken twee belangrijke celtypen samen: podocyten, die zich als verstrengelde vingers om bloedvaten heen vouwen, en parietale epitheelcellen (PECs), die de buitenste wand bekleden. In een gevaarlijke aandoening die snel progressieve glomerulonefritis (RPGN) wordt genoemd, raken podocyten beschadigd en raken PECs overactief, waardoor ze zich ophopen tot “crescents” die de filtratie blokkeren. Het eiwit L-WNK1, een signaalschakelaar die vooral bekend is van zijn rol bij zout- en bloeddrukbalans, wordt juist in hoge hoeveelheden in deze glomerulaire cellen aangemaakt. De auteurs vroegen zich af of te veel L-WNK1 RPGN verergert en of het verminderen ervan de ziekte kan afzwakken.
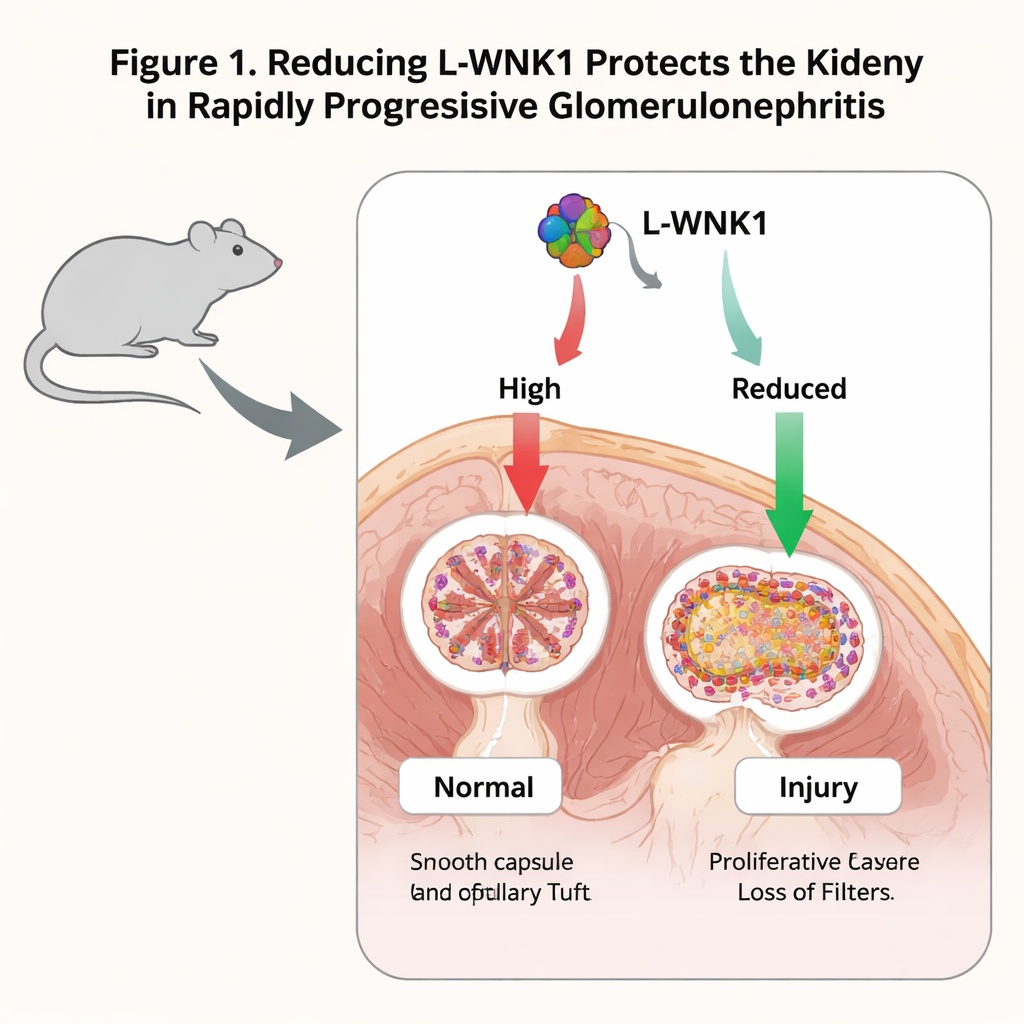
Het terugschakelen van L-WNK1 vermindert nierschade bij muizen
De onderzoekers gebruikten eerst een klassiek muismodel van RPGN dat wordt opgewekt door antilichamen die het glomerulaire basale membraan aanvallen, een belangrijk filterbestanddeel. Ze ontdekten dat de niveaus van L-WNK1 na beschadiging in de glomeruli toenamen, niet alleen bij muizen maar ook in nierbiopten van patiënten met verwante ziekten. Om oorzaak en gevolg te testen bestudeerden ze muizen die met slechts één werkende kopie van het L-WNK1-gen werden geboren. Deze dieren ontwikkelden nierfalen na antilichaam‑inductie, maar hun bloedafvalwaarden waren lager en hun nierweefsel liet minder crescents en minder littekenvorming zien dan bij normale muizen. Merkers van ontsteking en fibrose, zoals de signaalmoleculen MCP-1, TGF-β1 en collageengenen, waren ook verlaagd. Gezamenlijk suggereert dit dat gedeeltelijk verlies van L-WNK1 de ziekte milder maakt in plaats van erger.
Inzoomen op podocyten en hun buren
Aangezien podocyten centraal staan voor glomerulaire gezondheid en sterk L-WNK1 tot expressie brengen, verwijderde het team vervolgens WNK1 specifiek uit deze cellen met een genetische truc. Onder normale omstandigheden hadden deze muizen gezonde nieren, wat laat zien dat podocyten L-WNK1 niet nodig hebben om zich te ontwikkelen of te functioneren in het dagelijks leven. Toen RPGN werd geïnduceerd, stelden podocyt-specifieke knock-outmuizen zich opnieuw beter dan controles: hun bloedwaarden waren verbeterd en ze hadden de neiging minder crescents en minder CD44‑uitsprekende PECs (een activeringsmarker) te hebben. De bescherming was echter zwakker dan bij muizen met de bredere, lichaamsbrede vermindering van L-WNK1, en de niveaus van sommige ontstekingsmarkers daalden niet. Dit wijst op een rol voor L-WNK1 niet alleen in podocyten maar ook in andere glomerulaire of immuuncellen die aan de ziekte deelnemen.
Het vertragen van schadelijke celbeweging
Om te onderzoeken hoe L-WNK1 de vorming van crescents zou kunnen aanjagen, schakelden de onderzoekers over op celkweken. Met een klein-moleculair middel dat WNK‑kinasen blokkeert, behandelden ze humane podocyten in kweek en keken hoe snel deze cellen een kunstmatige wondgap opvulden. Remming van L-WNK1-activiteit vertraagde hun beweging duidelijk. Een vergelijkbaar effect werd gezien in gekweekte PECs: wanneer een groeifactor werd toegevoegd verspreidden PECs zich normaal om de gap te vullen, maar deze respons werd afgezwakt wanneer de WNK-remmer aanwezig was. Interessant genoeg verstoorde het middel in hun systeem niet merkbaar het interne cytoskelet van de podocyten, ondanks eerder werk in muizencellen dat grote structurele problemen suggereerde. Dit ondersteunt het idee dat, althans in levende dieren, de belangrijkste rol van L-WNK1 hier mogelijk is om te regelen hoe glomerulaire cellen en immuuncellen bewegen en reageren tijdens beschadiging in plaats van het handhaven van de basale filterarchitectuur.
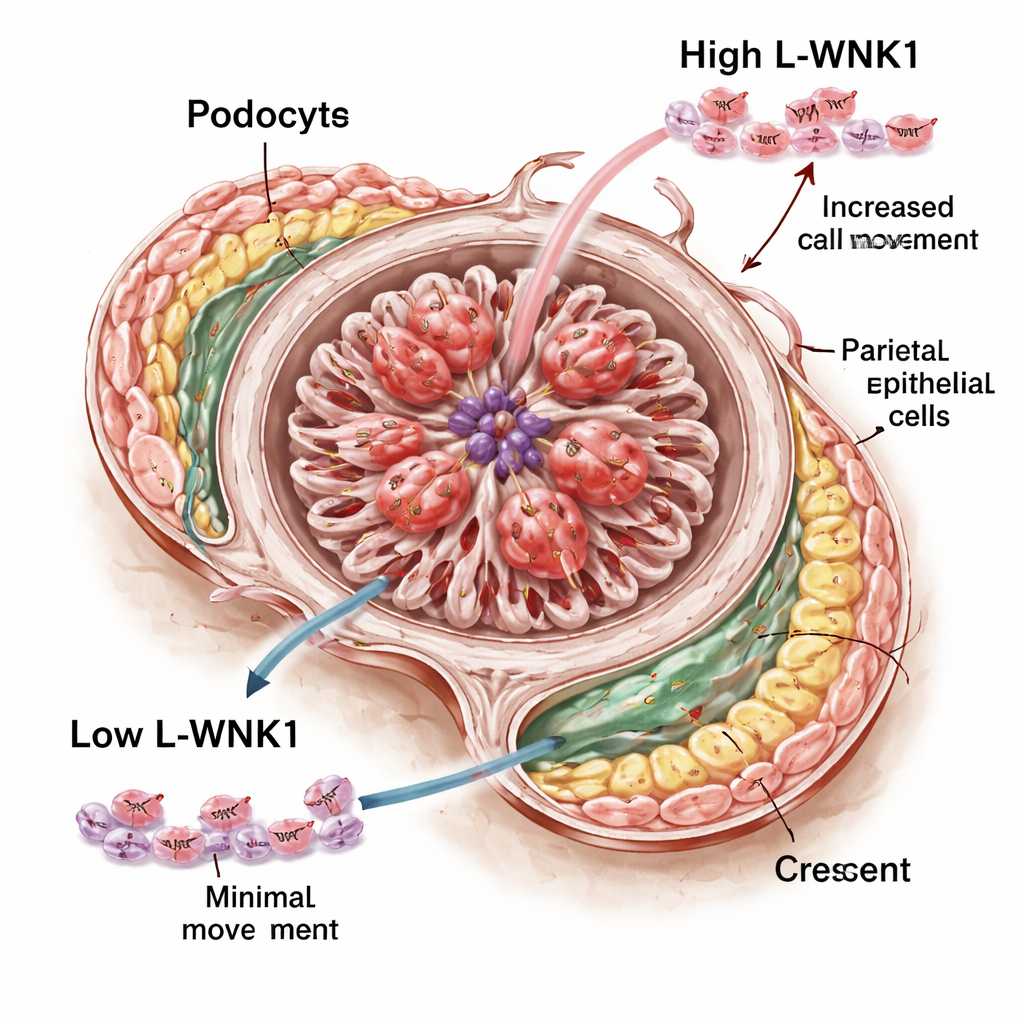
Wat dit betekent voor toekomstige behandelingen
Samengevat toont de studie L-WNK1 als een schadelijke versneller in een gewelddadige vorm van nierontsteking: wanneer dit eiwit omhoog wordt gereguleerd, bewegen en delen belangrijke cellen in het glomerulus zich op manieren die de filters verstoppen en littekenvorming bevorderen; wanneer de activiteit wordt verminderd, wordt de schade verzacht. Omdat L-WNK1 al wordt bestudeerd als een geneesmiddeldoel voor de bloeddruk, doen deze bevindingen de mogelijkheid rijzen dat zorgvuldig afgestemde remmers ooit patiënten met snel progressieve nierziekten zouden kunnen helpen beschermen. Er is nog veel werk nodig om muis- en celkweekresultaten naar veilige therapieën te vertalen, maar L-WNK1 komt nu naar voren als een veelbelovende nieuwe aangrijpingspunt voor een anderszins verwoestende aandoening.
Bronvermelding: Mousseaux, C., Migeon, T., Frère, P. et al. Knock-down of the long isoform of the WNK1 kinase mitigates the anti-glomerular basement membrane glomerulonephritis in mice. Sci Rep 16, 7335 (2026). https://doi.org/10.1038/s41598-026-36715-8
Trefwoorden: snel progressieve glomerulonefritis, nierontsteking, podocyten, glomerulaire crescents, WNK1-remming