Clear Sky Science · nl
Kan evolutionaire therapie worden toegepast bij niet-kleincellig longkanker?
Kankerbehandeling herdenken als een evolutionair strijdveld
De zorg voor kanker wordt vaak voorgesteld als een eenvoudige strijd: geef de krachtigste mogelijke middelen en probeer elke resterende kankercel uit te roeien. Toch werkt deze “maximale aanval” benadering vaak averechts bij snel progressieve kankers zoals gevorderde niet-kleincellige longkanker (NSCLC). Tumoren krimpen aanvankelijk, maar groeien bijna altijd terug, nu gedomineerd door medicijnresistente cellen. Deze studie stelt een prikkelende vraag: wat als artsen, in plaats van te proberen de tumor uit te roeien, deze zouden behandelen als een evoluerend ecosysteem en medicatieschema’s zouden gebruiken die bewust enkele medicijngevoelige cellen in leven houden om resistente cellen in toom te houden?
Waarom standaard behandeling met hoge doses resistentie kan versnellen
In de huidige praktijk krijgen patiënten met metastatische NSCLC en bepaalde genetische veranderingen vaak dagelijks pillen genaamd tyrosinekinaseremmers (TKI’s), zoals erlotinib. Deze middelen kunnen tumoren aanvankelijk sterk laten krimpen, maar vrijwel alle patiënten krijgen uiteindelijk een terugval omdat resistente kankercellen overleven en de overhand krijgen. Wanneer artsen de dosis tot het maximum opdrijven dat patiënten verdragen, doden ze voornamelijk de gevoelige cellen die goed op het middel reageren. Resistente cellen, die zelfs hoge doses kunnen overleven, krijgen plotseling minder concurrentie om ruimte en voedingsstoffen. Het resultaat is een evolutionaire “winst” voor de taaiste kankercellen, en de tumor keert uiteindelijk terug, nu veel moeilijker te behandelen. 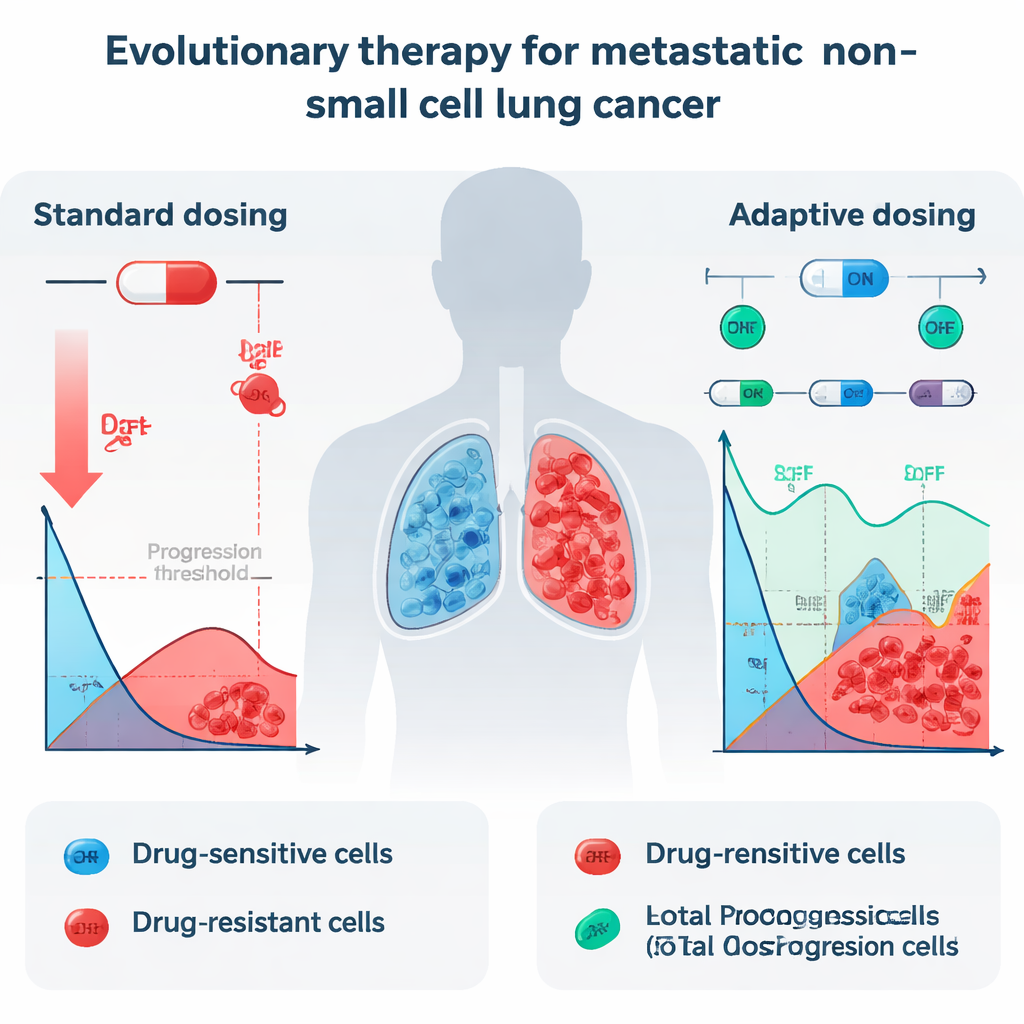
Wiskunde gebruiken om een nieuwe doseringsstrategie op echte patiënten te testen
De onderzoekers onderzochten of een andere strategie, evolutionaire therapie genoemd, zou kunnen werken bij stadium IV NSCLC. Evolutionaire therapie heeft niet als doel de tumor volledig uit te roeien. In plaats daarvan probeert zij de tumor te beheersen door een stabiele mix van gevoelige en resistente cellen te behouden, waarbij de gevoelige cellen de resistente cellen als het ware “wegdrukken”. Het team nam een specifiek aan/uit doseringsprotocol over dat al veelbelovend was gebleken bij prostaatkanker, en vroeg zich af: zou zo’n strategie theoretisch ook effectief zijn voor longkanker? Om dit te beantwoorden analyseerden ze gedetailleerde metingen van tumorgrootte van 13 NSCLC-patiënten behandeld met erlotinib in een klinische studie, zetten de scans om in het totale tumorvolume in de tijd en voerden deze gegevens in een reeks wiskundige modellen.
Het model vinden dat resistentie echt vangt
De onderzoekers testten 26 verschillende modellen van tumorgroei, allemaal met een indeling van kankercellen in twee groepen: medicijngevoelig en medicijnresistent. Deze modellen verschilden in hoe ze groeilimieten beschrijven, hoe de twee celtypen met elkaar concurreren, hoe het middel in het lichaam wordt verwerkt en hoe de behandeling cellen doodt. Veel eenvoudigere modellen pasten redelijk goed bij de patiëntgegevens wanneer tumoren alleen krimpten. Maar wanneer tumoren een realistischer “U-vormig” traject volgden—krimpend door behandeling en vervolgens weer groeiend door het ontstaan van resistentie—faalde het merendeel van de modellen. De beste match was een type dat het Gompertziaanse model wordt genoemd en dat twee cruciale ideeën omvatte: ten eerste kunnen tumoren niet onbeperkt groeien (ze ervaren verzadiging), en ten tweede concurreren gevoelige en resistente cellen op een asymmetrische manier, zodat het succes van het ene type afhangt van hoeveel van het andere aanwezig is.
Adaptieve therapie versus standaardzorg simuleren
Zodra ze de best passende modellen hadden geïdentificeerd, gebruikten de onderzoekers die om voor elke patiënt twee behandelingsstrategieën te simuleren: de gebruikelijke constante maximale dosis en een adaptief protocol geïnspireerd door Zhang en collega’s. In de adaptieve benadering wordt erlotinib gegeven totdat de tumor tot de helft van zijn oorspronkelijke grootte is geslonken, waarna het middel wordt gepauzeerd om de gevoelige cellen te laten teruggroeien; de behandeling wordt hervat zodra de tumor terugkeert naar zijn uitgangsmaat, en deze cyclus herhaalt zich. Over alle goed presterende modellen die competitie tussen celtypen omvatten, vertraagde deze adaptieve strategie consequent de tijd totdat de tumor 110% van zijn oorspronkelijke grootte overschreed—een veelgebruikte grens voor progressie. In het best passende Gompertziaanse model met competitie nam de mediane tijd tot progressie toe van ongeveer 24,8 maanden onder standaarddosering naar 42,3 maanden onder het adaptieve protocol, een winst van grofweg anderhalf jaar. 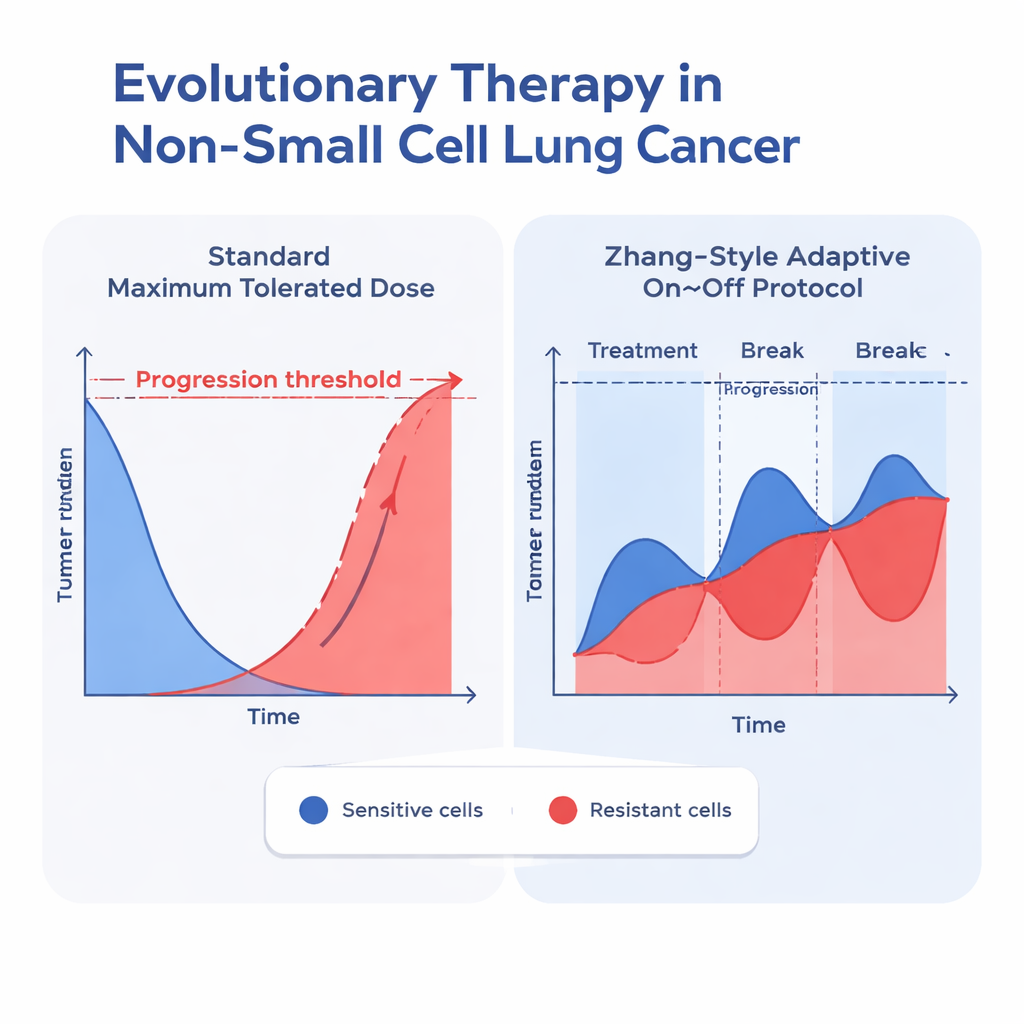
Wat dit voor toekomstige patiënten zou kunnen betekenen
Dit werk verandert de huidige behandeling van NSCLC-patiënten nog niet, maar het levert een krachtig proof of concept. Door hun modellen te verankeren in echte patiëntgegevens en te eisen dat de modellen niet alleen vroege krimp maar ook door resistentie aangedreven hergroei reproduceren, tonen de auteurs aan dat evolutionaire therapie theoretisch haalbaar is, zelfs bij een snelgroeiende en dodelijke kanker. Hun resultaten suggereren dat zorgvuldig getimede behandelonderbrekingen het beheer van de ziekte kunnen verlengen door medicijngevoelige cellen als bondgenoten te gebruiken in plaats van als collaterale schade. Om dit idee in de praktijk te brengen zijn meer gegevens nodig, betere biomarkers zoals bloedtests die tumor-DNA volgen, en rigoureuze klinische onderzoeken. Toch is de boodschap voor niet-specialisten helder: soms is de slimste manier om kanker te bestrijden niet om zo hard mogelijk toe te slaan, maar om zijn evolutie te sturen zodat het een beter beheerbare, langzamer bewegende vijand blijft.
Bronvermelding: Jansén-Storbacka, L.R., Honasoge, K.S., Molnárová, E. et al. Can evolutionary therapy be applied in non-small cell lung cancer?. Sci Rep 16, 7442 (2026). https://doi.org/10.1038/s41598-026-36712-x
Trefwoorden: evolutionaire therapie, niet-kleincellig longkanker, medicatieresistentie, adaptieve dosering, mathematische oncologie