Clear Sky Science · nl
Exosomen van cholangiocarcinoom verzwakken de antitumorfuncties van NK-cellen
Hoe een verborgen kankersoort het immuunsysteem te slim af is
Cholangiocarcinoom, een kanker van de galgangen in de lever, is berucht omdat het moeilijk vroeg te detecteren en lastig te behandelen is. Deze studie onderzoekt een subtactiek die deze tumoren gebruiken om het natuurlijke afweersysteem te omzeilen: ze sturen kleine pakketjes, exosomen genoemd, uit die natuurlijke killercellen (NK-cellen) op de voorgrond stilletjes verzwakken. NK-cellen vormen een snelle verdedigingslinie die gespecialiseerd is in het opsporen en doden van kankercellen. Inzicht in deze sluipende strategie kan nieuwe wegen openen voor therapieën die het immuunsysteem herstellen zodat het weer effectief kan terugvechten.
De eerste hulpverleners tegen kanker in het lichaam
NK-cellen behoren tot het aangeboren immuunsysteem, de snelle responsmacht van het lichaam. In tegenstelling tot veel immuuncellen die tijd nodig hebben om een specifiek gevaar te herkennen, kunnen NK-cellen snel abnormale cellen aanvallen, waaronder virusgeïnfecteerde en kankercellen. Ze doen dit door zich aan doelwitten vast te hechten en toxische moleculen zoals granzyme B en signaalstoffen zoals interferon-gamma (IFN-γ) vrij te geven, die zowel tumorcellen doden als andere immuundefenders mobiliseren. Bij veel bloedkankers en sommige solide tumoren heeft het stimuleren van NK-celactiviteit veelbelovend als behandelingsstrategie aangetoond. Maar in solide tumoren zoals galgangskanker lijken NK-cellen vaak merkbaar schaars en trager aanwezig juist daar waar ze het meest nodig zijn.
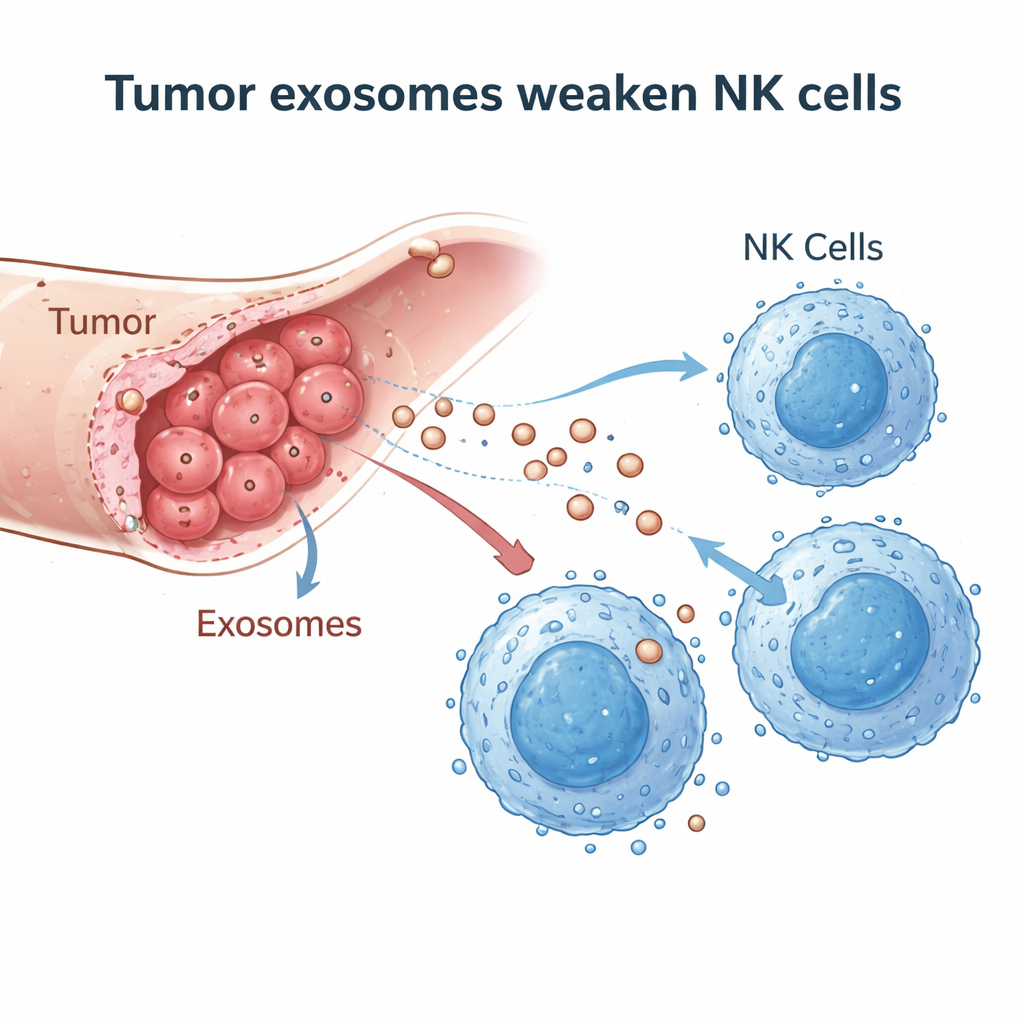
Kleine blaasje met grote impact
De onderzoekers vermoeden dat cholangiocarcinoomcellen NK-cellen saboteren met exosomen—nano-grote membraanblaasjes vol met eiwitten en genetisch materiaal die cellen vrijgeven om te communiceren. Ze verzamelden exosomen uit een menselijke galgangskankercellijn en uit het bloed van cholangiocarcinoompatiënten en bevestigden hun identiteit en grootte met elektronenmicroscopie, deeltjestracking en standaard exosoommarkers. In tumorweefselmonsters van 20 patiënten vergeleken ze kankergebieden met dichtbij gelegen niet-kankerachtig leverweefsel en vonden veel minder NK-cellen die de tumoren binnendrongen, wat suggereert dat iets in de tumoromgeving NK-cellen weghoudt of uitschakelt.
Over schakelen van overlevings- en dodelijke signalen
Om te onderzoeken hoe deze tumor-exosomen NK-cellen beïnvloeden, stelde het team een NK-cellijn (NK-92) bloot aan exosomen van kankercellen en van patiëntbloed. De NK-cellen vertoonden hogere niveaus van geprogrammeerde celdood, vooral na behandeling met exosomen van de tumorcellijn. Op moleculair niveau verminderden de NK-cellen de productie van belangrijke "blijfburn"-eiwitten (BCL-2 en BCL-XL), waardoor de balans naar celdood kantelde. Interessant genoeg veranderde hun algemene groei en deling niet, wat betekent dat de exosomen vooral NK-cellen gevoeliger voor overlijden maakten in plaats van hun proliferatie te vertragen. De exosoom-behandelde NK-cellen gaven ook minder IFN-γ en minder granzyme B af, waardoor zowel hun vermogen om doelwitten direct te doden als hun vermogen om bredere immuunresponsen te coördineren afnam. Laboratoriumtesten die meten hoe goed NK-cellen standaarddoelcellen konden doden, lieten zien dat dit dodelijk vermogen afnam na blootstelling aan cholangiocarcinoom-exosomen.
Het uiteenvallen van immuuncel-samenwerking
NK-cellen moeten aan elkaar en aan tumorcellen kleven om effectief te werken, waarbij ze vertrouwen op oppervlakte-"adhesiemoleculen" die als moleculair klittenband fungeren. Na behandeling met kankergeproduceerde exosomen verloren NK-cellen hun normale geklusterde groeipatroon en leken ze meer verspreid. De onderzoekers vonden dat de niveaus van verschillende belangrijke adhesiemoleculen (CD11a, CD18 en CD54) zowel op gen- als eiwitniveau daalden, terwijl een andere adhesiemarker, CD2, ongewijzigd bleef. Dit verlies aan adhesie bemoeilijkt waarschijnlijk het vermogen van NK-cellen om tumoren te bereiken, stabiel contact met kankercellen te vormen en dodelijke slagen toe te dienen. Cruciaal is dat, wanneer het team NK-cellen direct uit het bloed van cholangiocarcinoompatiënten bestudeerde, die cellen dezelfde kenmerken lieten zien: zwakkere dodelijke activiteit en lagere niveaus van dezelfde adhesiemoleculen in vergelijking met NK-cellen van gezonde vrijwilligers.
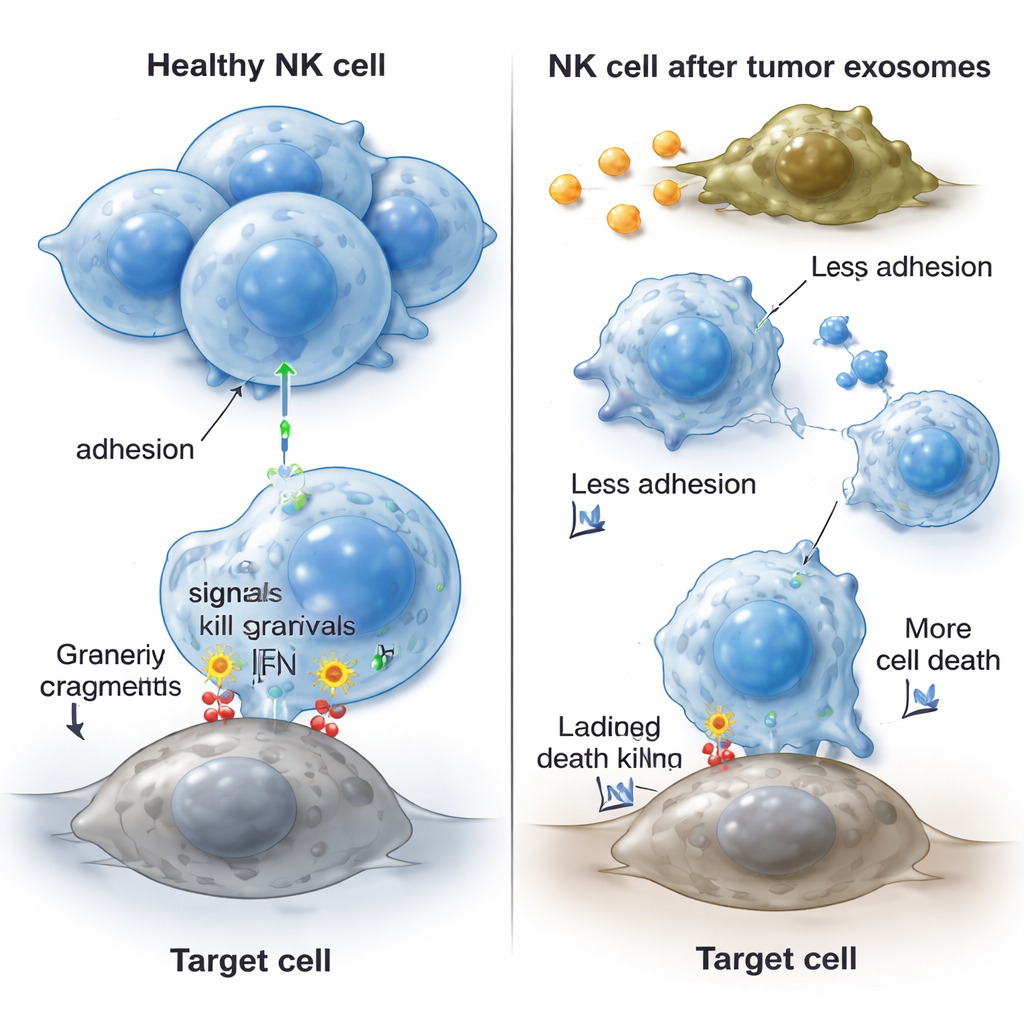
Wat dit betekent voor patiënten en toekomstige behandelingen
Samen suggereren de bevindingen dat cholangiocarcinoom exosomen gebruikt als een vorm van moleculaire sabotage om immuunaanvallen te ontlopen. Deze kleine vesikels duwen NK-cellen richting celdood, verminderen hun productie van belangrijke dodelijke factoren en ontdoen ze van adhesieve eiwitten die hen in staat stellen te clusteren en tumoren aan te pakken. Het resultaat is minder functionele NK-cellen in en rondom de tumor en een afgezwakte immuunrespons die de kanker meer vrij spel geeft. Hoewel dit werk grotendeels in gecontroleerde laboratoriumomstandigheden en met een beperkt aantal patiëntmonsters is uitgevoerd, wijst het op nieuwe strategieën: het blokkeren van tumorexosomen, het herstellen van NK-overlevingssignalen of het versterken van adhesiemoleculen kan helpen het natuurlijke afweervermogen tegen deze dodelijke galgangskanker te heractiveren.
Bronvermelding: Wang, X., Zhang, F., Cao, Z. et al. Cholangiocarcinoma derived exosomes attenuate the anti-tumor functions of NK cells. Sci Rep 16, 5810 (2026). https://doi.org/10.1038/s41598-026-36706-9
Trefwoorden: cholangiocarcinoom, natural killer-cellen, exosomen, tumor immuunontsnapping, tumormicro-omgeving