Clear Sky Science · nl
Bioinformatische karakterisering en geautomatiseerde detectie van metabool geactiveerde monocyten-subpopulaties bij dyslipidemie
Waarom verborgen immuuncellen belangrijk zijn voor hartgezondheid
Cholesterolproblemen worden meestal besproken in termen van dieet, uitslagen van bloedtesten en het risico op hartaanvallen. Maar onder die cijfers verandert ons immuunsysteem stilletjes. Deze studie bekijkt een speciale groep witte bloedcellen in het bloed van jongvolwassenen met hoog LDL(“slecht”) cholesterol. Deze cellen lijken “metabool geactiveerd” te raken en onthouden vroeger contact met overtollige vetten, wat ontsteking van de bloedvaten — en toekomstig hart- en vaatfalen — waarschijnlijker kan maken. Inzicht in deze verborgen celtypen kan artsen helpen problemen eerder te detecteren en preciezere behandelingen te ontwerpen.
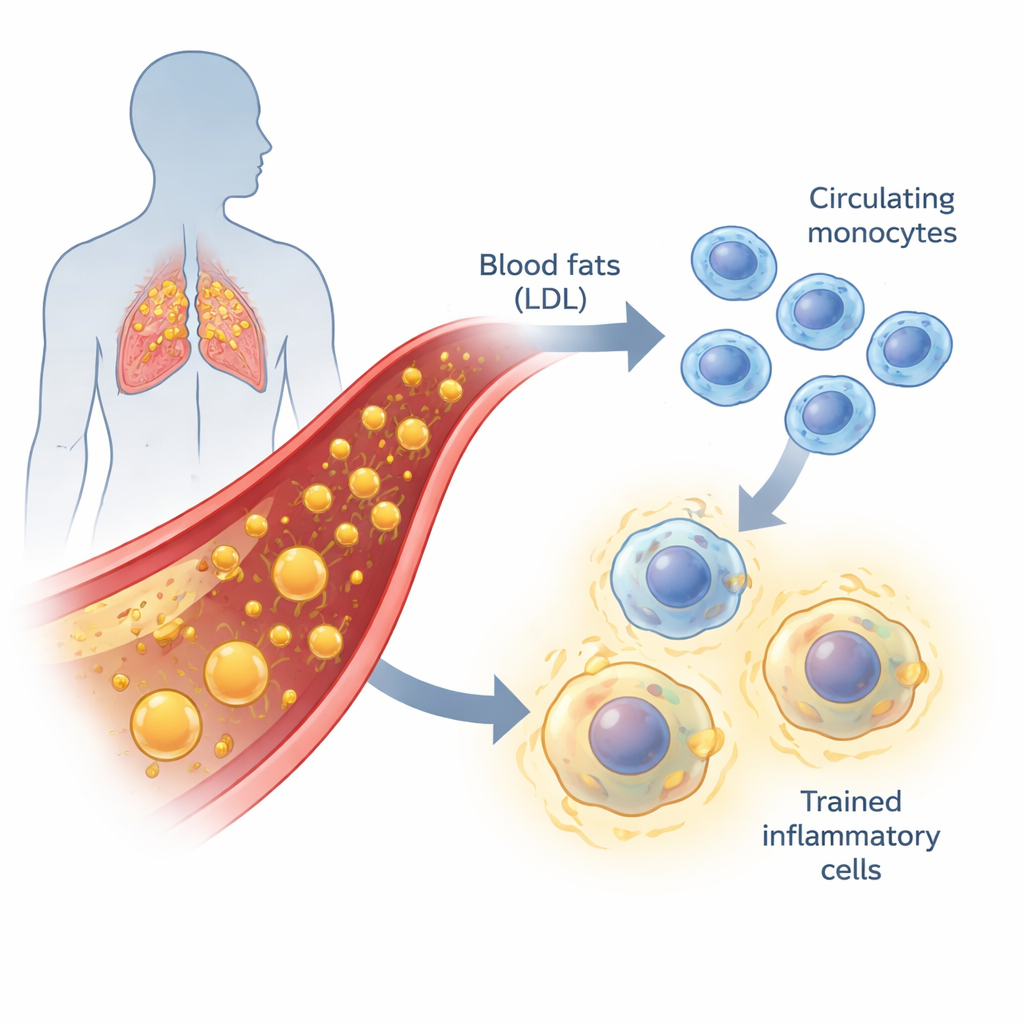
Vet in het bloed en langzaam smeulende ontsteking
Atherosclerose, het proces dat leidt tot verstopte bloedvaten, gaat niet alleen over vet dat zich aan vaatwanden hecht. Het is ook een trage, chronische ontstekingsziekte. Wanneer LDL-cholesterol hoog is, vooral in geoxideerde vormen, prikkelt het de vaatwand. Monocyten — circulerende witte bloedcellen — en de macrofagen waartoe ze differentiëren worden naar deze plekken aangetrokken en beginnen vet op te nemen. Als dit opruimproces slecht gereguleerd is, veranderen de cellen in “foam cells” en dragen ze bij aan de opbouw van vette plaques. Traditioneel delen wetenschappers bloedmonocyten in drie groepen op basis van oppervlaktemarkeringen, elk met verschillende rollen bij het patrouilleren van bloedvaten, het opwekken van ontsteking of het onderhoud van weefsels.
Voorbij eenvoudige labels: nieuwe monocyten ontdekken
De auteurs veronderstelden dat sommige circulerende monocyten bij mensen met dyslipidemie al zijn geherprogrammeerd naar een metabool actieve staat, klaar om schadelijke macrofagen te worden. Om dit te onderzoeken verzamelden ze bloed van 23 jongvolwassenen met hoog LDL-cholesterol en 17 gezonde deelnemers met normale lipidenprofielen. Niemand gebruikte cholesterolverlagende medicatie of had andere belangrijke aandoeningen, waardoor de impact van dyslipidemie zelf beter geïsoleerd kon worden. Met een techniek genaamd flowcytometrie maten ze niet alleen klassieke oppervlaktemarkers maar ook eiwitten die betrokken zijn bij vetverwerking en chemische tags op histonen — kleine proteïnehaspels die helpen bepalen welke genen in een cel aan- of uitgezet zijn.
Slimme algoritmes om complexe immuunlandschappen te lezen
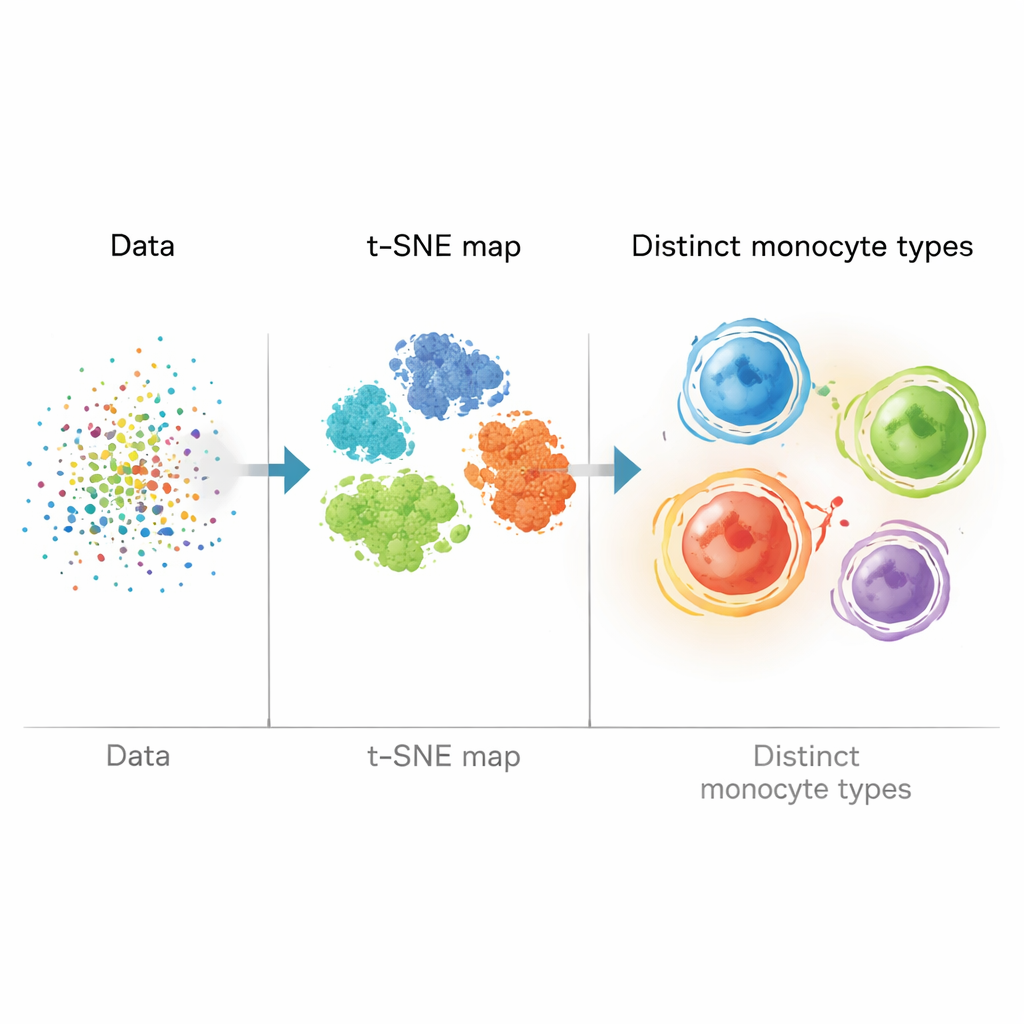
In plaats van alleen te vertrouwen op handmatig “gating” (met het oog grenzen trekken op tweemarkerplots), bouwde het team een bioinformatica-pijplijn die elke cel als een punt in hoge-dimensieruimte behandelde. Ze schonen en standaardiseerden de data, en gebruikten vervolgens t-SNE, een wiskundige methode die veel-markermetingen omzet in een tweedimensionale kaart waarop vergelijkbare cellen clusteren. Daarna pasten ze clustermethodes toe (X-shift en FlowSOM) om automatisch cellen met vergelijkbare markerpaterns te groeperen. Dit stelde hen in staat verder te kijken dan de drie klassieke monocyten-types en vier belangrijke monocytenpopulaties te identificeren, gedefinieerd door combinaties van vetverwerkende eiwitten (ABCA1, PLIN2, CD36) en de gebruikelijke CD14- en CD16-markers.
Een geprimede ontstekingspopulatie bij dyslipidemie
Twee van deze vier monocyten-groepen vielen op. Één in het bijzonder — gekenmerkt door hoge CD14-waarden, afwezigheid van CD16 en sterke ABCA1 met variabele PLIN2 en CD36 — kwam overeen met het profiel van “metabool geactiveerde” monocyten (MoMe). Bij mensen met dyslipidemie waren deze MoMe-populatie en een verwante groep significant vaker aanwezig dan bij gezonde controles. Toen de onderzoekers epigenetische markers onderzochten — specifiek H3K4me3 en H3K27me3, chemische labels op histoneiwitten die gelinkt zijn aan genactiviteit — vonden ze dat MoMe-cellen van dyslipidemische individuen hogere niveaus van H3K4me3 droegen. Deze marker wordt geassocieerd met genen die ontsteking bevorderen, wat suggereert dat deze cellen een vorm van aangeboren “geheugen” of getrainde immuniteit hebben na herhaalde blootstelling aan hoge LDL.
Van circulerende cellen naar plaque-vormende macrofagen
Om te zien wat deze monocyten in weefsels zouden kunnen worden, kweekte het team gezuiverde monocyten in een laboratoriumomgeving die het metabool syndroom nabootste, waarbij ze gestimuleerd werden om macrofagen te worden. Ze gebruikten opnieuw geavanceerde analyse om macrofaag-subgroepen te identificeren en maten hun epigenetische markers. Interessant genoeg toonden macrofagen afkomstig van gezonde donoren vaak hogere niveaus van activerende histonetags dan die van dyslipidemische patiënten, wat doet vermoeden dat de ontstekings-”training” zich anders kan manifesteren zodra cellen het bloed verlaten. Hoewel de steekproefomvang bescheiden was, ondersteunen de bevindingen het idee dat langdurige blootstelling aan overtollige bloedlipiden monocyten zowel op eiwit- als epigenetisch niveau hervormt, waardoor ze vatbaarder worden voor sterkere ontstekingsreacties.
Wat dit betekent voor patiënten en toekomstige zorg
Voor een leek is de conclusie dat hoog LDL-cholesterol niet alleen een probleem is van “te veel vet” maar ook van “herschakelde” immuuncellen. Deze studie toont aan dat zelfs bij jongvolwassenen dyslipidemie gekoppeld is aan een onderscheidende populatie monocyten die metabool opgeladen en epigenetisch geprimed lijken om vaatontsteking te voeden. Door krachtige computationele tools te combineren met gedetailleerde celmetingen kunnen onderzoekers deze risicovolle celtypen nu in bloed opsporen, lang voordat een hartaanval plaatsvindt. In de toekomst zouden dergelijke benaderingen artsen kunnen helpen cardiovasculair risico beter in te schatten, te volgen hoe goed behandelingen schadelijke immuuntraining omkeren, en uiteindelijk therapieën te ontwerpen die zich niet alleen op cholesterolniveaus richten maar ook op de immuuncellen die daarop reageren.
Bronvermelding: Ramírez-Torres, R., Ramírez-Segovia, S.G., González-Huerta, M.J. et al. Bioinformatic characterization and automated detection of metabolically activated monocyte subpopulations in dyslipidemia. Sci Rep 16, 6170 (2026). https://doi.org/10.1038/s41598-026-36678-w
Trefwoorden: dyslipidemie, monocyten, getrainde immuniteit, atherosclerose, flowcytometrie