Clear Sky Science · nl
Toepassing van groep A streptokokken collagene‑achtig eiwit 1‑exprimerende Lactococcus als nieuwe immunotherapie tegen pancreaskanaaladenocarcinoom
Vriendelijke bacteriën omvormen tot kankerkrijgers
Pancreaskanker behoort tot de dodelijkste vormen van kanker, deels omdat ze zich verbergt achter krachtige verdedigingsmechanismen die het immuunsysteem uitschakelen. Deze studie onderzoekt een onverwachte bondgenoot in de strijd tegen deze ziekte: een veelvoorkomende “goede” melkzuurbacterie, herontworpen om zich op pancreastumoren te richten en het immuunsysteem effectiever te laten aanvallen. Door een kleverig oppervlak-eiwit te gebruiken van een gevaarlijke streptokok, veranderden de onderzoekers een onschadelijke microbe in een gericht antikankermiddel in muizen.
Een taaie kanker die het immuunsysteem slim om de tuin leidt
Pancreas ductaal adenocarcinoom is berucht om zijn hoge sterftecijfer: slechts ongeveer één op de acht patiënten leeft vijf jaar na de diagnose. Een belangrijke reden is de tumormicro‑omgeving: een dichte, littekenachtige laag vol ondersteunende cellen en moleculen die immuunaanvallen afzwakken en veel medicijnen blokkeren. Onder de boosdoeners bevinden zich neutrofiele extracellulaire netwerken, of NETs—webben van DNA en eiwitten die witte bloedcellen in de omgeving uitwerpen. Bij pancreaskanker doen deze kleverige netten meer kwaad dan goed: ze helpen tumoren groeien, houden cytotoxische T‑cellen buiten bereik en worden geassocieerd met slechtere uitkomsten. NETs uitschakelen, terwijl antitumor‑immuniteit wordt geactiveerd, is daardoor een aantrekkelijke strategie geworden.
Een kleverig eiwit lenen, maar niet de gevaarlijke kiem
Eerder werk toonde aan dat een oppervlakte‑eiwit van groep A Streptococcus, Scl1 genoemd, zich kan vasthechten aan tumor‑geassocieerde vezels en bovendien NET‑vorming kan remmen, waardoor de groei van pancreastumoren in muizen vertraagde. Maar groep A‑streptokokken veroorzaken ook keelontsteking en ernstige invasieve infecties, waardoor ze ongeschikt zijn als levende therapie. Om het nuttige eiwit te behouden zonder de schadelijke bacterie, bouwde het team Lactococcus lactis—een probioticum dat veel in voedsel wordt gebruikt en als veilig geldt—zodanig om dat het Scl1 op het oppervlak toont. Deze nieuwe stam, Lactococcus::620 genoemd, werd getest in muizen met pancreastumoren, zowel in eenvoudige flanktumor‑modellen als in realistischere tumoren die in de alvleesklier groeien.
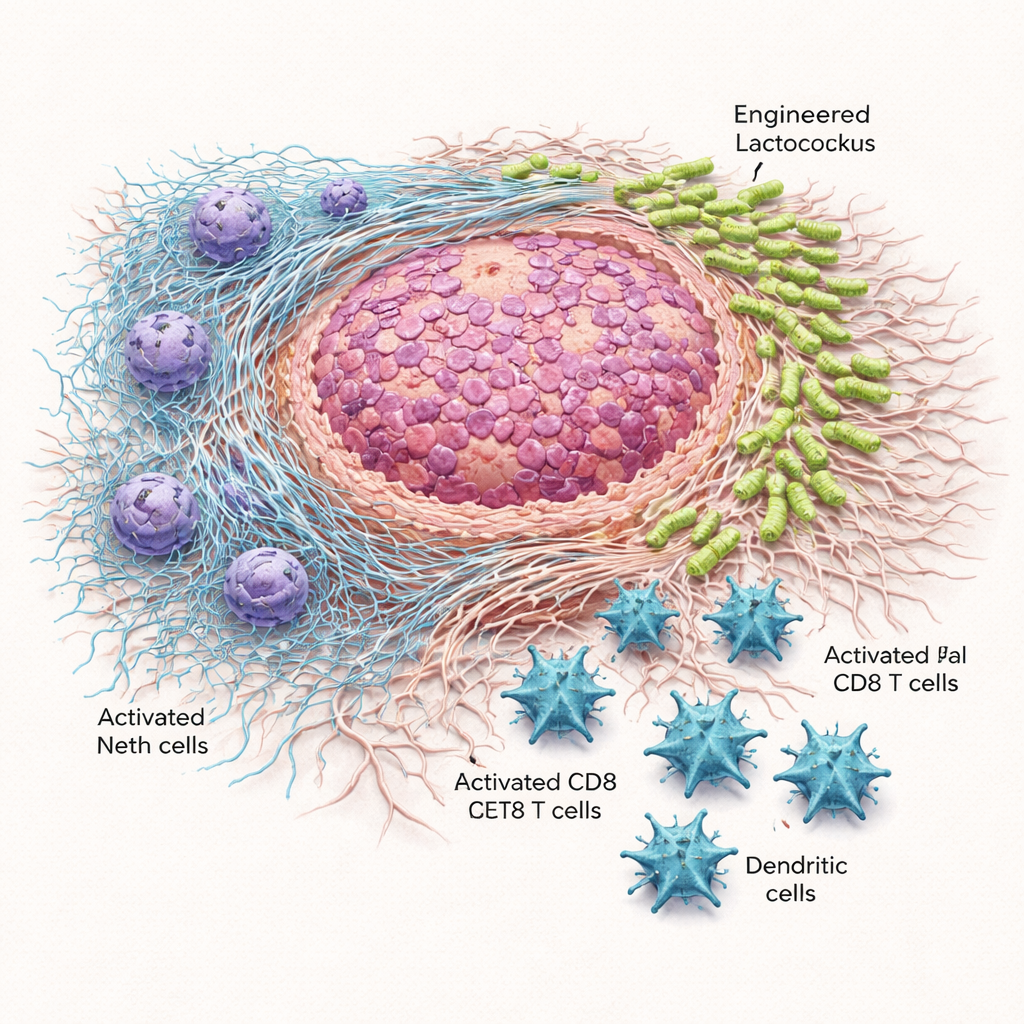
Geleide bacteriën remmen tumorgroei en verlengen overleving
Wanneer een enkele dosis van de gemodificeerde bacteriën rechtstreeks in flanktumoren werd geïnjecteerd, of in de buikholte werd toegediend, groeiden de tumoren langzamer en waren ze lichter dan bij muizen die gewone Lactococcus of een zoutoplossing kregen. In het zwaardere pancreasmodel waren meerdere doses om de drie dagen nodig, maar de voordelen waren opvallend. Lactococcus::620 verkleinde tumoren, verminderde hun gewicht en verlengde de overleving van de dieren zonder behandeling‑gerelateerde sterfgevallen te veroorzaken. Microscopie en kweek van tumorweefsel toonden aan dat de Scl1‑dragende bacteriën betrouwbaar zich ophoopten in het tumorgebied, vooral in de vezelrijke matrix die door kanker‑geassocieerde fibroblasten wordt gelegd, terwijl de milt grotendeels gespaard bleef. Ongewijzigde Lactococcus verspreidde zich daarentegen meer door het lichaam en was soms toxisch bij systemische toediening.
Schadelijke netten ontwapenen en immuuncellen binnenlaten
De gemodificeerde bacteriën veranderden ook het immuunsysteem rondom de tumoren. Tumoren van met Lactococcus::620 behandelde muizen bevatten meer CD8‑“killer” T‑cellen en dendritische cellen—belangrijke spelers in het herkennen en vernietigen van kankercellen—en die T‑cellen vertoonden minder uitputtingsmarkers en meer activiteitsgerelateerde moleculen. Tegelijkertijd namen maten voor NET‑activiteit af. In laboratoriumtesten gaven neutrofielen, blootgesteld aan Lactococcus::620, minder vrij DNA af en toonden ze een lagere activiteit van myeloperoxidase, een enzym dat nodig is voor de opbouw van NETs. Bij behandelde muizen was circulerend DNA dat met NETs geassocieerd is verminderd. Cruciaal was dat, wanneer dezelfde experimenten werden herhaald in muizen die genetisch niet in staat zijn NETs te vormen, de gemodificeerde bacteriën de tumorgroei niet langer remden. Dat verlies van effect wijst sterk op het belang van NET‑blokkade voor de werkzaamheid van de therapie.
Wat dit kan betekenen voor toekomstige kankerzorg
Gezamenlijk schetsen de bevindingen een nieuw concept: het gebruik van een veilig, voedselgeschikt bacterie als programmeerbaar afleveringsvoertuig om een NET‑blokkerend, tumor‑aantrekkend eiwit direct in de vijandige omgeving van pancreaskanker te brengen. In muizen verminderde deze aanpak de tumorlast, verbeterde de overleving en maakte ze het immuunsysteem effectiever. Hoewel er nog veel werk nodig is voordat een dergelijke strategie bij mensen kan worden getest—onder andere proeven in modellen van uitgezaaide ziekte en combinaties met moderne immunotherapieën—laat de studie zien dat zorgvuldig gemodificeerde “goede” bacteriën mogelijk ooit het evenwicht kunnen doen kantelen tegen een van onze meest hardnekkige kankers.
Bronvermelding: Godfrey, E.A., Choi, S.J., Sestito, M. et al. Application of group A streptococcal collagen-like protein 1-expressing Lactococcus as a novel immunotherapeutic against pancreatic ductal adenocarcinoma. Sci Rep 16, 5911 (2026). https://doi.org/10.1038/s41598-026-36657-1
Trefwoorden: pancreaskanker, probiotische therapie, tumormicro‑omgeving, immuunmodulatie, neutrofiele extracellulaire netwerken