Clear Sky Science · nl
Oppervlaktemarkers op supermeres overtreffen extracellulaire vesikels bij de diagnose van colorectale kanker
Waarom piepkleine bloeddeeltjes de kankercontrole kunnen veranderen
Colorectale kanker is een van de meest voorkomende vormen van kanker wereldwijd, en artsen hebben dringend betere bloedtesten nodig die de ziekte in een vroeg stadium kunnen opsporen en kunnen volgen of een behandeling aanslaat. Deze studie onderzoekt een nieuw erkende klasse van ultrasmalle deeltjes in het bloed, “supermeres” genoemd, en laat zien dat ze mogelijk duidelijkere kankersignalen dragen dan beter bekende deeltjes. De auteurs presenteren ook een snelle sensor die deze supermeres rechtstreeks uit een kleine druppel bloed binnen een half uur kan meten, wat mogelijk de deur opent naar snellere en nauwkeurigere kankerdiagnostiek.
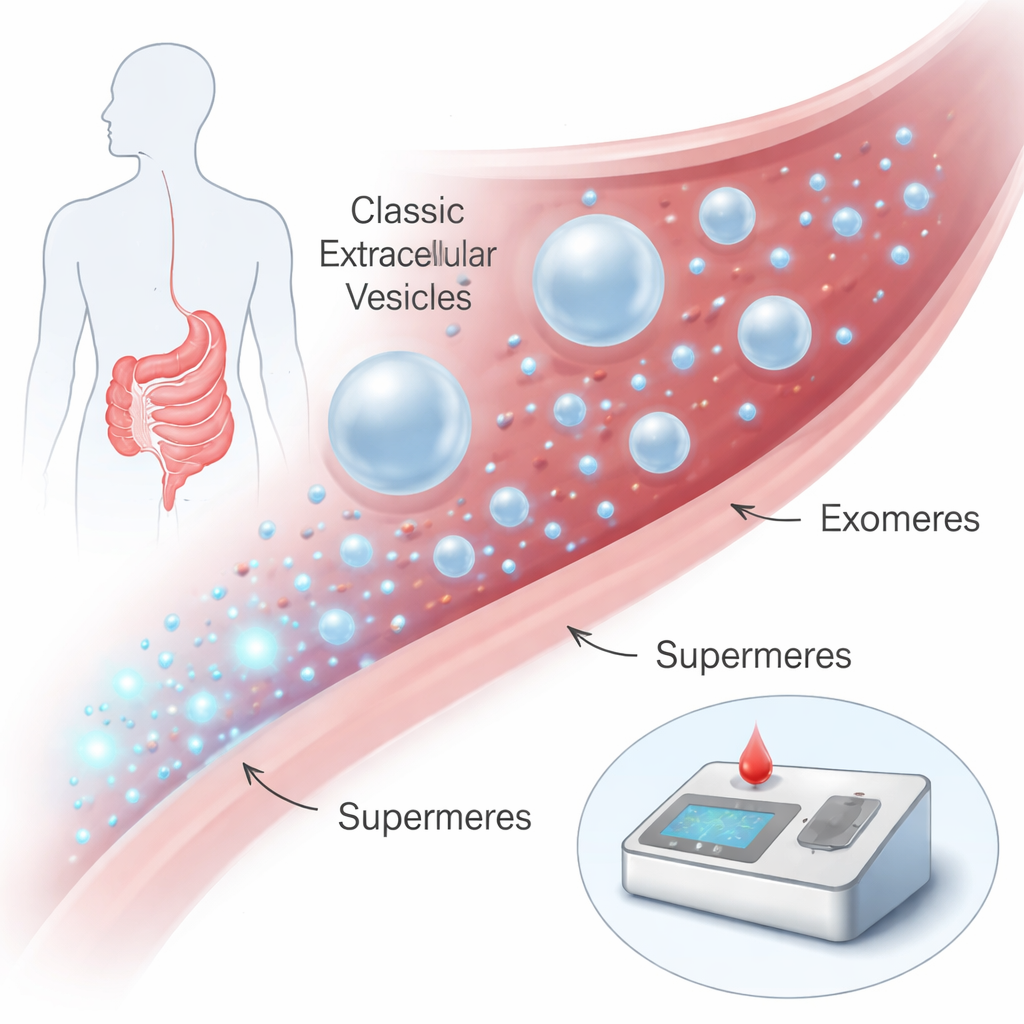
Piepkleine boodschappers in de bloedbaan
Onze cellen geven voortdurend nanoschaalpakketjes af aan lichaamsvloeistoffen zoals bloed. Jarenlang lag de focus op membraan-gebonden deeltjes zoals exosomen en andere extracellulaire vesikels, die eiwitten en genetisch materiaal tussen cellen kunnen vervoeren en als ziektebiomarkers zijn onderzocht. Recente ontdekkingen tonen nog kleinere, membraanloze deeltjes aan, exomeren en, nog kleiner, supermeres. Supermeres zijn slechts ongeveer 15–25 nanometer groot — duizenden zouden over de breedte van een mensenhaar passen — en ze zitten boordevol moleculen gerelateerd aan ziekte. Eerder werk suggereerde dat supermeres bijzonder rijk aan kankersignalen kunnen zijn, maar ze waren moeilijk te isoleren en bestuderen, en vereisten dagenlange ultracentrifugatie met gespecialiseerde apparatuur.
Wat supermeres onderscheidt
Het team scheidde zorgvuldig drie belangrijke typen nanodeeltjes uit kankercelcultures en menselijk bloed: kleine extracellulaire vesikels, exomeren en supermeres. Ze bevestigden dat elke groep een kenmerkend groottebereik heeft, waarbij supermeres het kleinst zijn. Het cruciale verschil was echter elektrisch van aard. Supermeres droegen een veel sterker negatieve oppervlakte-lading dan de andere deeltjes — ongeveer twee keer het niveau waarbij willekeurige thermische beweging relevant wordt — grotendeels door RNA-strengen die aan hun oppervlak kleven. Toen de onderzoekers dit RNA met enzymen afbraken, daalde de lading scherp, wat aantoont dat oppervlakte-RNA centraal staat in het elektrostatische signatuur van supermeres. Eiwitmapping liet zien dat supermeres ook eigen “ID-tags” hebben: eiwitten zoals HSPA13, ENO2 en DDR1 waren sterk verrijkt op supermeres maar grotendeels afwezig op de andere deeltjestypen, vergelijkbaar met klassieke markers die gewone extracellulaire vesikels identificeren.
Een snelle sensor die naar lading luistert
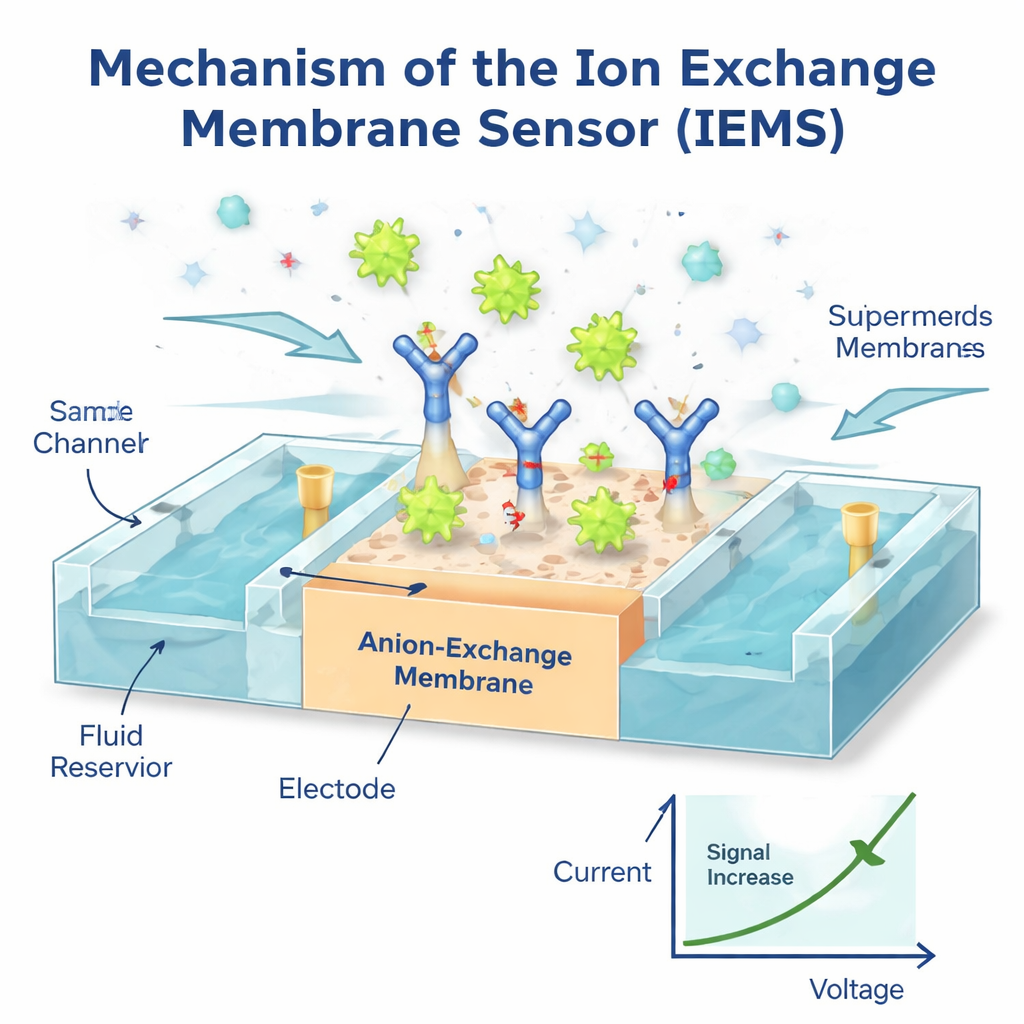
Om van deze unieke eigenschappen gebruik te maken, bouwden de auteurs een Ion Exchange Membrane Sensor (IEMS), een klein apparaat dat veranderingen in elektrische stroom detecteert wanneer geladen deeltjes aan het oppervlak binden. Ze coatten een speciale membraan met antilichamen die een gekozen eiwit, bijvoorbeeld een kankermarker, uit een stromend bloedmonster grijpen. Omdat supermeres zo sterk geladen zijn terwijl de meeste andere deeltjes en vrije eiwitten zwakker geladen zijn, veranderen alleen gevangen supermeres merkbaar het stroom–spanning-gedrag van het membraan. Het resultaat is een sterk, selectief elektrisch signaal dat het aantal supermeres met die marker weerspiegelt. Met deze opstelling kon het team tot slechts één miljoen supermeres per milliliter detecteren over een concentratiebereik van duizendvoud, allemaal binnen ongeveer 30 minuten en met slechts 50 microliter monster — zonder langdurige zuivering. Tests waarbij bekende hoeveelheden supermeres aan gezond plasma werden toegevoegd, toonden bijna volledige terugwinning, en de metingen kwamen overeen met die van langzamere, geavanceerde optische instrumenten.
Betere prestaties dan bestaande nanopartikelmarkers
Met zowel traditionele als snelle methoden vergeleken de onderzoekers supermeres direct met exomeren en kleine extracellulaire vesikels in bloed van mensen met colorectale kanker en gezonde vrijwilligers. Ze concentreerden zich op meerdere eiwitten die op alle drie de deeltjes voorkomen, inclusief bekende tumormarkers zoals CEA en GPC1. Voor bijna elk gedeeld eiwit deed het signaal dat supermeres droegen het beter of even goed bij het onderscheiden van kankerpatiënten en gezonde personen, terwijl exomeren vaak weinig diagnostische waarde lieten zien. Supermere-specifieke eiwitten zoals HSPA13, ENO2 en DDR1 waren bijzonder veelzeggend: deze waren nauwelijks detecteerbaar in gezond plasma maar sterk verhoogd bij colorectale kanker, wat een uitstekende scheiding tussen de twee groepen gaf. Opmerkelijk was dat bij twee patiënten die vóór en na tumoroperatie werden bestudeerd, de niveaus van supermeres scherp daalden na tumorverwijdering, terwijl signalen van traditionele vesikels weinig veranderden, wat suggereert dat supermeres nauw aansluiten bij de tumorbelasting.
Wat dit kan betekenen voor toekomstige kankertests
Om hun nieuwe sensor onder realistische omstandigheden te testen, gebruikte het team de IEMS om supermeres met verschillende markers te meten in plasma van patiënten met colorectale kanker, alvleesklierkanker, glioblastoom en van gezonde donors. De snelle, isolatievrije aflezingen kwamen nauw overeen met die van de veel langzamere ultracentrifugatie plus optische analyse, wat bevestigt dat snelheid niet ten koste ging van nauwkeurigheid. Bij colorectale kanker presteerden supermere-gebaseerde metingen beter dan de totale bloedspiegels van CEA, een lang gebruikte klinische marker. Gezamenlijk suggereren de bevindingen dat supermeres niet slechts een microscopische curiositeit zijn, maar een krachtige en toegankelijke bron van kankerinformatie. Als dit gevalideerd wordt in grotere en meer diverse patiëntengroepen, zou het meten van marker-dragende supermeres met compacte, op lading gebaseerde sensoren een praktische manier kunnen worden om te screenen op colorectale kanker, behandelingen te monitoren en mogelijk therapieën op maat te maken met veel minder tijd, monstervolume en complexiteit dan de huidige methoden.
Bronvermelding: Kumar, S., Sinclair, J.A., Shi, T. et al. Surface markers on supermeres outperform extracellular vesicles in colorectal cancer diagnosis. Sci Rep 16, 5989 (2026). https://doi.org/10.1038/s41598-026-36626-8
Trefwoorden: colorectale kanker, bloedbiomarkeerders, extracellulaire nanodeeltjes, supermeres, biosensortechnologie