Clear Sky Science · nl
Gecombineerde effecten van nitraat en antimicrobiële middelen op in vitro subgingivale biofilms
Waarom je tandvlees en darmmedicatie verbonden zijn
Bloedend tandvlees en tandvleesaandoeningen worden meestal toegeschreven aan “slechte” bacteriën. Tandartsen grijpen om ze te bestrijden vaak naar sterke mondspoelingen en antibiotica. Deze studie stelt een grotere vraag: wat als sommige van deze behandelingen stilletjes de nuttige bacteriën beschadigen die we nodig hebben, terwijl een eenvoudig voedingsstof in bladgroenten onze mondmicroben juist richting gezondheid kan duwen?
Tandvleesontsteking als een gemeenschapsprobleem
Parodontitis is een langdurige infectie rond de tanden die de weefsels vernietigt die tanden op hun plaats houden en wordt in verband gebracht met hartziekten, diabetes en zelfs aandoeningen van de hersenen. In plaats van veroorzaakt te worden door één enkele kiem, ontstaat het wanneer de hele gemeenschap van mondbacteriën verschuift naar een schadelijke toestand, dysbiose genoemd. Moderne behandeling leunt nog steeds sterk op breedwerkende middelen: antibiotica zoals amoxicilline en metronidazol, en antiseptische spoelingen zoals chloorhexidine. Deze middelen kunnen probleemveroorzakers doden—maar ze kunnen ook vriendelijke bacteriën uitroeien en de ontwikkeling van resistentie stimuleren.
Een nadere blik op biofilms uit echte patiënten
Om te zien wat deze behandelingen daadwerkelijk met tandvleesbacteriën doen, verzamelden de onderzoekers tandplak uit diepe pockets rond de tanden van 12 mensen met parodontitis. In het laboratorium kweekten ze deze monsters als dunne lagen bacteriën, of biofilms, gedurende acht uur onder acht verschillende condities: geen behandeling, nitraat alleen, elk middel afzonderlijk, en elk middel gecombineerd met nitraat. Nitraat, een natuurlijk verbinding die rijkelijk voorkomt in spinazie, sla en biet, kan door bepaalde mondbacteriën worden omgezet in stikstofoxide, een gas dat bloedvaten helpt ontspannen en de groei van ziekteveroorzakende microben kan remmen. Het team mat hoeveel biofilm gevormd werd, hoe goed het nitraat werd omgezet en welke bacteriële soorten onder elke behandeling gedijen.
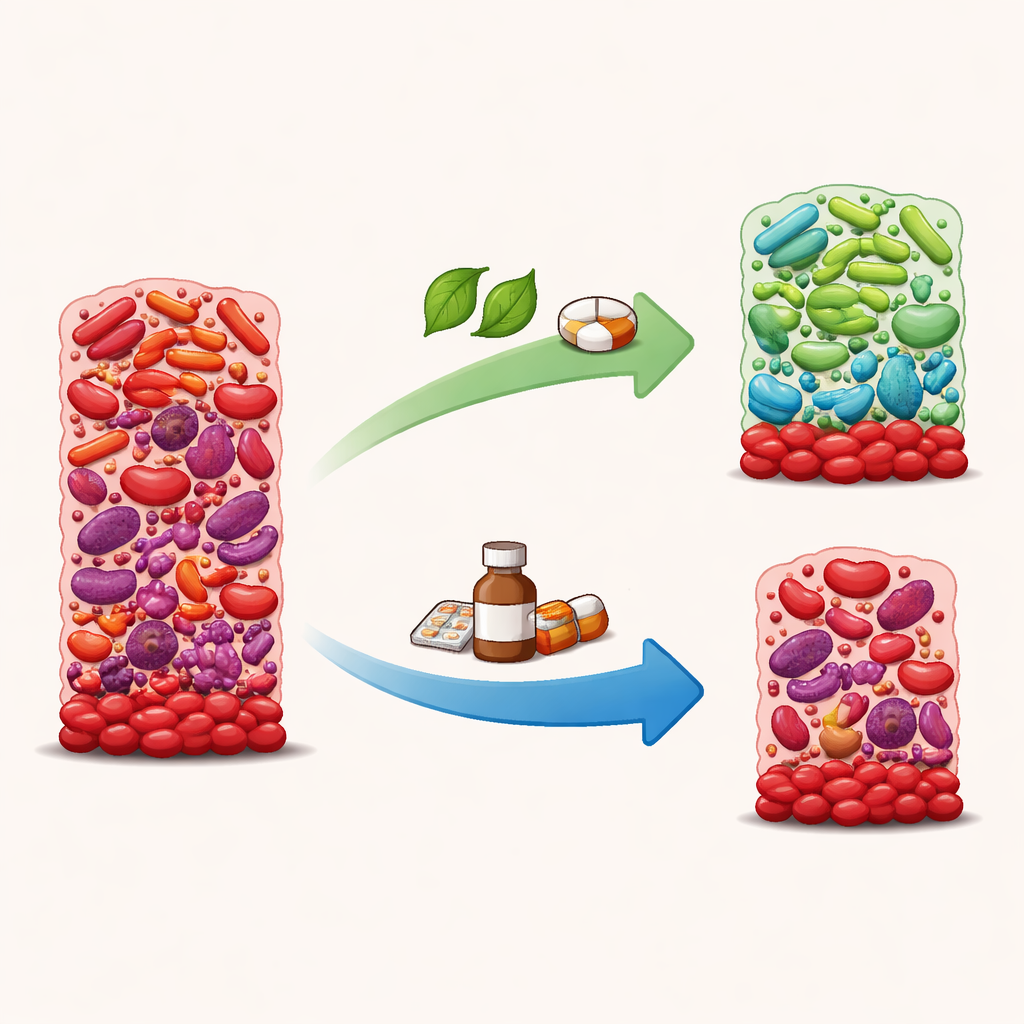
Geneesmiddelen die groei krimpen maar de balans kunnen verslechteren
Lage doses chloorhexidine en amoxicilline halveerden de biofilmgroei ruwweg en verminderden sterk het vermogen van de bacteriën om nitraat te verwerken. Maar dit was geen selectieve “goede schoonmaak”. DNA-sequencing toonde dat onder deze condities gezondheidsgemedieerde bacteriën zoals Rothia, Gemella en Kingella de neiging hadden af te nemen, terwijl meerdere soorten die met tandvleesziekte geassocieerd zijn—waaronder Fusobacterium, Treponema en Eubacterium—ofwel op hun plek bleven of prominenter werden. Een index die aangeeft hoe “ziek” een gemeenschap eruitziet onder de microscoop was hoger bij chloorhexidine en amoxicilline dan bij nitraat, wat suggereert dat deze middelen de biofilm naar een schadelijkere, uit balans geraakte toestand kunnen duwen, zelfs terwijl ze de algehele groei onderdrukken.
Brandstof uit bladgroenten en een zachter antibioticum
Nitraat vertelde een ander verhaal. Toen plaques werden gekweekt met alleen nitraat, namen bacteriën die gespecialiseerd zijn in het omzetten van nitraat in nuttige producten, zoals Neisseria en sommige Aggregatibacter‑soorten, toe. De dysbiose‑score daalde vergeleken met chloorhexidine of amoxicilline condities, wat wijst op een gezondere gemeenschap. Metronidazol, op een niveau vergelijkbaar met wat daadwerkelijk de tandvleeszakken bij patiënten bereikt, verminderde op zichzelf niet sterk de groei of het nitraatgebruik. Maar wanneer het gecombineerd werd met nitraat, leek het de balans op een gunstige manier te kantelen: ziekte‑geassocieerde soorten zoals Fusobacterium en Treponema daalden, terwijl nitraat‑gebruikende Neisseria en Kingella toenamen. Deze combinatie leek de ergste boosdoeners terug te snoeien zonder sleutelactiviteiten weg te vagen.
Wat dit betekent voor dagelijkse zorg
Voor mensen met tandvleesziekte suggereren deze bevindingen dat “sterkst” niet altijd “beste” is als het om antimicrobiële middelen gaat. In dit laboratoriummodel vertraagden lage doses chloorhexidine en amoxicilline de bacteriegroei maar verzwakten ook een natuurlijk, nitraat‑gebaseerd pad dat zowel de mondgezondheid als de algehele gezondheid ondersteunt, en ze waren gekoppeld aan meer ziekteachtige microbieel patronen. Nitraat, vooral in combinatie met metronidazol, bevoordeelde bacteriën die met gezonder tandvlees geassocieerd worden en behield de nitraatstofwisseling. Hoewel echte monden complexer zijn dan laboratoriumschaaltjes, ondersteunt dit werk het idee van zachtere, microbiom‑vriendelijke strategieën—zoals nitraatrijke diëten en zorgvuldig gekozen antibiotica—om tandvleesziekte te beheersen zonder de bacteriën te ondermijnen die ons helpen gezond te blijven.
Bronvermelding: Moran, S.P., Nadal-Ruiz, M., Mira, A. et al. Combined effects of nitrate and antimicrobial compounds on in vitro subgingival biofilms. Sci Rep 16, 6686 (2026). https://doi.org/10.1038/s41598-026-36588-x
Trefwoorden: tandvleesaandoening, orale microbiota, nitraat, mondspoeling, antibiotica