Clear Sky Science · nl
Diagnose van de ziekte van Alzheimer met hoge nauwkeurigheid via Petri-netmodellering van signaalroutes
Waarom vroege detectie van hersenziekten ons allemaal aangaat
De ziekte van Alzheimer tast geheugen en zelfstandigheid langzaam aan, vaak lang voordat duidelijke symptomen zichtbaar worden. Huidige diagnostische middelen, zoals hersenscans en cognitieve testen, kunnen duur zijn, moeilijk toegankelijk en weinig gevoelig in de vroegste stadia. Deze studie introduceert een nieuwe manier om de moleculaire "bedrading" van het lichaam te lezen met behulp van bloed- of hersenmonsters en een wiskundig kader dat een Petri-net wordt genoemd. Het doel is eenvoudig maar diepgaand: met zeer hoge nauwkeurigheid vaststellen of iemands genactiviteitspatroon meer lijkt op dat van een gezond persoon of op dat van iemand met de ziekte van Alzheimer — idealiter vroeg genoeg om het beloop van de ziekte te beïnvloeden.
De ziekte lezen in de signaal-"circuits" van het lichaam
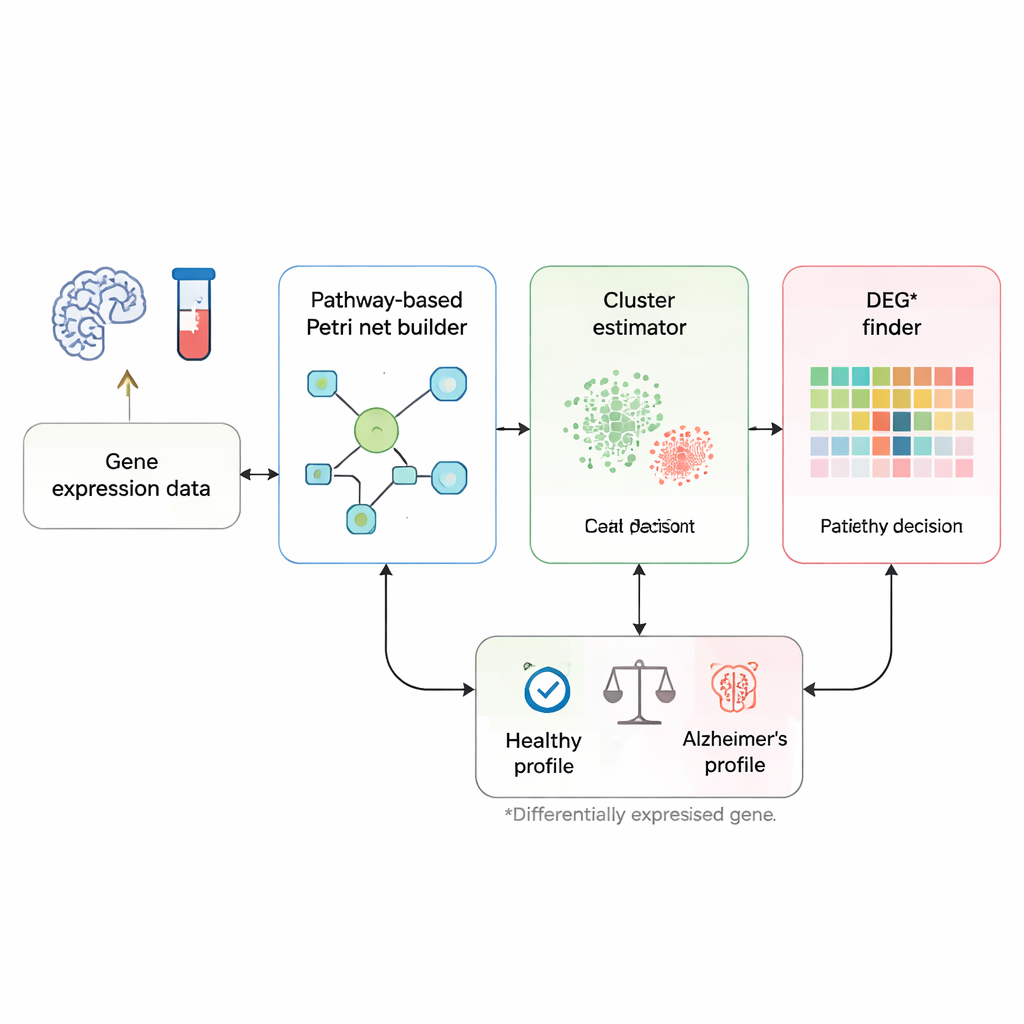
In plaats van elk gen als een geïsoleerde marker te behandelen, richten de onderzoekers zich op hoe genen met elkaar communiceren langs bekende biologische signaalroutes die aan Alzheimer zijn gekoppeld. Ze beginnen met een gecureerde routekaart uit de KEGG-database, die genen en de activerende of remmende relaties tussen hen opsomt. Deze route wordt omgezet in een Petri-net — een soort stroomdiagram waarbij cirkels genen voorstellen, rechthoeken interacties en kleine tokens signalen zijn die door het netwerk bewegen. Wanneer een token van het ene uiteinde van de route naar speciale "ziekte"-knopen reist, vertegenwoordigt dat een keten van gengebeurtenissen die kunnen leiden tot het afsterven van hersencellen en dementie.
Van een bloedmonster naar een ja-of-nee-antwoord
De methode begint met genexpressieprofielen: metingen die aangeven hoe actief duizenden genen zijn in iemands bloed of hersenweefsel. Eerst vergelijkt een aangepaste "cluster estimator" een nieuw monster met eerder gelabelde gezonde en patiëntmonsters, met de nadruk op genen die al bekend staan als verschillend tussen deze groepen. Voor elk zulk gen controleert het hulpmiddel welke trainingsmonsters de meest vergelijkbare expressieniveaus hebben en gebruikt een soort buurman-stemprocedure om het nieuwe monster een initiële label te geven als waarschijnlijk gezond of waarschijnlijk ziek. Deze stap vormt twee werkclusters van monsters: één die typische gezonde patronen vertegenwoordigt en één die typische Alzheimer-patronen vertegenwoordigt.
De meest informatieve genen per persoon vinden
Vervolgens komt een meer gepersonaliseerde stap. Voor een bepaalde persoon bekijkt de methode gen voor gen waar hun expressieniveaus werkelijk uitspringen. Voor elk gen vergelijkt het de waarde van die persoon met het bereik dat in zowel de gezonde cluster als de patiëntcluster wordt gezien, met behulp van robuuste statistieken die de invloed van ruisende uitschieters verminderen. Als de expressie van een gen duidelijk binnen het "zieke" bereik valt en buiten het gezonde bereik, wordt het gemarkeerd als een DEG* — een bijzonder informatief gen voor dat individu. Deze DEG*-genen krijgen initiële tokens in het Petri-net, die aangeven waar abnormale activiteit zich eerst voordoet in het signaalcircuit.
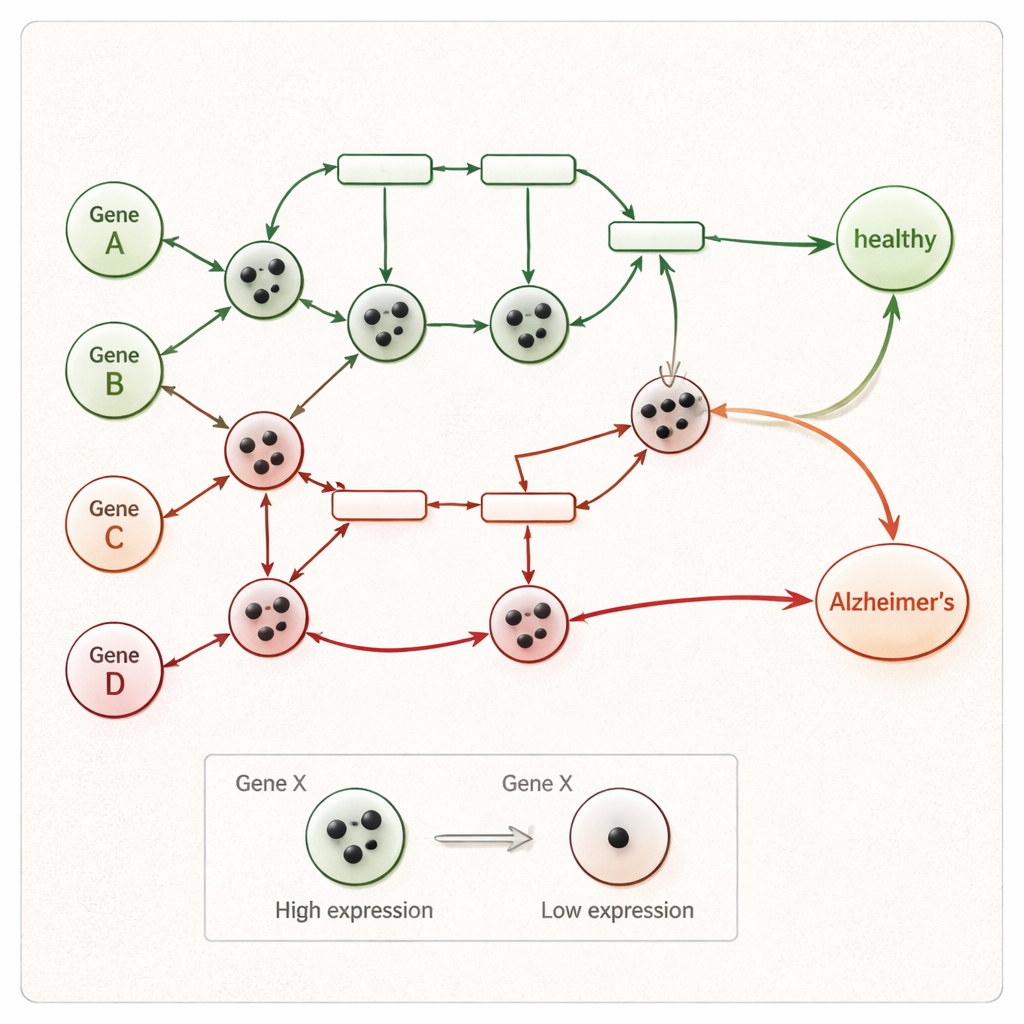
Het netwerk laten aflopen naar een diagnose
Zodra de tokens geplaatst zijn, draait het Petri-net stap voor stap. In elke stap "vuren" alle interacties waarvan de invoergenen genoeg tokens hebben, waarbij tokens naar downstream-genen verplaatsen volgens activerings- en inhibitieregels. Dit gaat door totdat geen verdere verplaatsingen meer mogelijk zijn. Als er aan het einde ten minste één token het eind-ziekteknooppunt van het netwerk bereikt — dat processen als neuronale celdood of neurodegeneratie representeert — wordt het monster geclassificeerd als Alzheimer; zo niet, dan wordt het als gezond gelabeld. Omdat elke vuurstap wordt vastgelegd, kunnen onderzoekers een duidelijke route traceren van iemands afwijkende genactiviteit tot aan een gezond of ziek resultaat, in plaats van te vertrouwen op een ondoorzichtige statistische score.
Hoe nauwkeurig is deze methode in de praktijk?
Het team testte hun raamwerk op verschillende grote, openbare genexpressiedatasets van zowel bloed- als hersenweefsel. In twee veelgebruikte bloeddatasets onderscheidde hun methode Alzheimerpatiënten correct van gezonde individuen in ongeveer 98–99% van de gevallen, wat eerdere machine learning-benaderingen, die vaak slechts 65–81% bereikten, ruimschoots overtrof. Ze lieten ook sterke prestaties zien in aanvullende hersen- en bloeddatasets, zelfs wanneer het aantal monsters klein was. Belangrijk is dat, in tegenstelling tot veel concurrenten, hun methode geen luidruchtige of moeilijk te interpreteren monsters weggooide; in plaats daarvan gebruikt het ontwerp interne mechanismen om variabiliteit te verwerken terwijl alle data in de analyse blijven.
Wat dit betekent voor toekomstige Alzheimer-tests
Voor de leek is de belangrijkste boodschap dat de studie complexe genetica en routekaarten omzet in een duidelijke, stapsgewijze beslisprocedure die vroege tekenen van de ziekte van Alzheimer kan lezen uit een eenvoudig monster, mogelijk zelfs alleen bloed. Door te modelleren hoe afwijkende genen samenwerken, en niet alleen hoe ze afzonderlijk handelen, levert het Petri-netkader zowel hoge diagnostische nauwkeurigheid als een begrijpelijk "verhaal" over hoe de ziekte zich bij elk individu kan ontvouwen. Hoewel dit werk nog onderzoek is en nog geen klinische test, wijst het op toekomstige hulpmiddelen die Alzheimer eerder kunnen detecteren, behandelkeuzes kunnen sturen en uiteindelijk kunnen worden aangepast aan andere hersenziekten en kankers met hetzelfde onderliggende idee.
Bronvermelding: Ebrahimian, H., Asadzadeh, F., Rahgozar, M. et al. Diagnosis of Alzheimer’s disease with high accuracy via Petri net modeling of signaling pathways. Sci Rep 16, 6457 (2026). https://doi.org/10.1038/s41598-026-36585-0
Trefwoorden: Diagnose van Alzheimer, genexpressie, signaalroutes, Petri-netmodellering, bloedbiomarkers