Clear Sky Science · nl
De tumor-micro-omgeving bij slokdarmkanker en de relatie met klinische kenmerken en respons op neoadjuvante behandeling
Waarom de omgeving van de tumor ertoe doet
Slokdarmkanker behoort tot de dodelijkste vormen van kanker wereldwijd, en zelfs met moderne chemotherapie en radiotherapie reageren veel patiënten niet zo goed als gehoopt. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote implicaties: wat gebeurt er in de “buurt” rond de tumor — de tumor-micro-omgeving — en kan de samenstelling daarvan helpen verklaren waarom sommige patiënten wel op behandeling reageren en anderen niet? Door immuuncellen en gerelateerde markers vóór en na therapie nauwkeurig te bestuderen, beginnen de onderzoekers in kaart te brengen hoe het lichaam en de tumor op elkaar reageren, en hoe dit verborgen gesprek toekomstige, meer gepersonaliseerde behandelingen zou kunnen sturen.
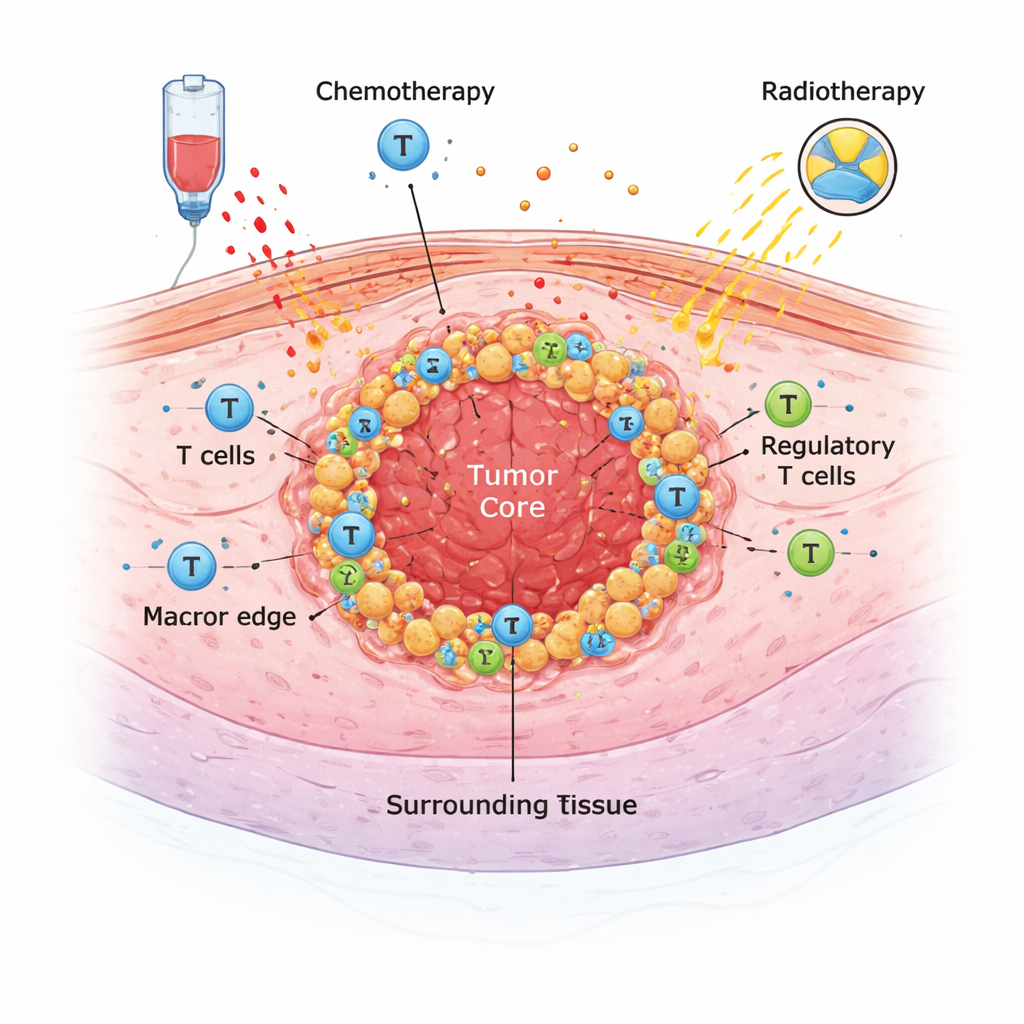
Het verborgen ecosysteem rond een tumor
Solide tumoren groeien niet geïsoleerd. Ze liggen in een complex ecosysteem van immuuncellen, ondersteuningcellen en signaalmoleculen dat bekendstaat als de tumor-micro-omgeving. In deze studie onderzochten artsen en pathologen in Lausanne tumormonsters van 68 patiënten die tussen 2009 en 2021 een operatie ondergingen voor slokdarmkanker. De meeste hadden krachtige behandeling vóór de operatie gekregen — chemotherapie, chemoradiatie of beide — om de tumor te verkleinen. Met speciale kleuringen op weefselsneden telde het team verschillende belangrijke immuunceltypen (inclusief algemene T-cellen, cytotoxische T-cellen en verschillende soorten macrofagen) en mat markers die respons op immunotherapie kunnen voorspellen, zoals PD-L1 en HER2.
Wie de patiënten waren en wat werd gemeten
De patiënten in deze reeks waren voornamelijk mannen begin zestig, en de meerderheid had adenocarcinoom, het type slokdarmkanker dat vaak in verband wordt gebracht met chronische zure reflux en Barrett-slokdarm. Een kleinere groep had plaveiselcelcarcinoom, een andere vorm die ontstaat uit de platte bekledingscellen van de slokdarm. De onderzoekers koppelden zorgvuldig wat ze onder de microscoop zagen aan klinische gegevens zoals ziektestadium, rookgedrag, gewichtsverlies en het soort preoperatieve behandeling. Ze volgden ook hoe volledig elke tumor op therapie reageerde, met een gradesysteem dat volledige verdwijning van kankercellen onderscheidt van weinig of geen respons.
Leefstijl, tumortype en een stillere immuunaanwezigheid
Verschillende alledaagse en ziektegerelateerde factoren bleken geassocieerd met een zwakkere immuunaanwezigheid rond de tumor. Patiënten die actief rookten hadden over het algemeen minder macrofagen en minder zogenoemde M2-achtige macrofagen, die vaak verbonden zijn met tumorondersteuning en immuunsuppressie. Mensen met meer gevorderde tumoren, groter preoperatief gewichtsverlies of plaveiselcelkankers hadden doorgaans minder T-cellen en macrofagen die de tumor infiltreerden. Daarentegen waren tumoren met hoge PD-L1-scores — een indicator die vaak wordt gebruikt bij selectie voor immunotherapie — ‘heter’, met meer T-cellen en macrofagen, maar dit patroon is eerder in verband gebracht met slechtere uitkomsten, waarschijnlijk omdat de tumor actief PD-L1 gebruikt om immuunaanvallen uit te schakelen.
Hoe behandeling de omgeving van de tumor herschikt
Neoadjuvante (preoperatieve) behandeling herschikte de tumor-micro-omgeving ingrijpend. Zowel chemotherapie als chemoradiatie verhoogden het aantal macrofagen, inclusief M2-achtige cellen, terwijl regulerende T-cellen — een groep die normaal immuunreacties dempt — sterk werden verminderd. Het totale aantal T-cellen en cytotoxische T-cellen veranderde minder consistent. Opmerkelijk was dat chemoradiatie geneigd was PD-L1-niveaus op tumor- en omliggende cellen te verlagen, waardoor het aandeel patiënten met hoge PD-L1-scores na behandeling afnam. Dit suggereert dat standaardbehandeling tumoren minder geschikt kan doen lijken voor PD-1/PD-L1-blokkade-immunotherapie als men alleen afgaat op één momentopname na chemoradiatie.
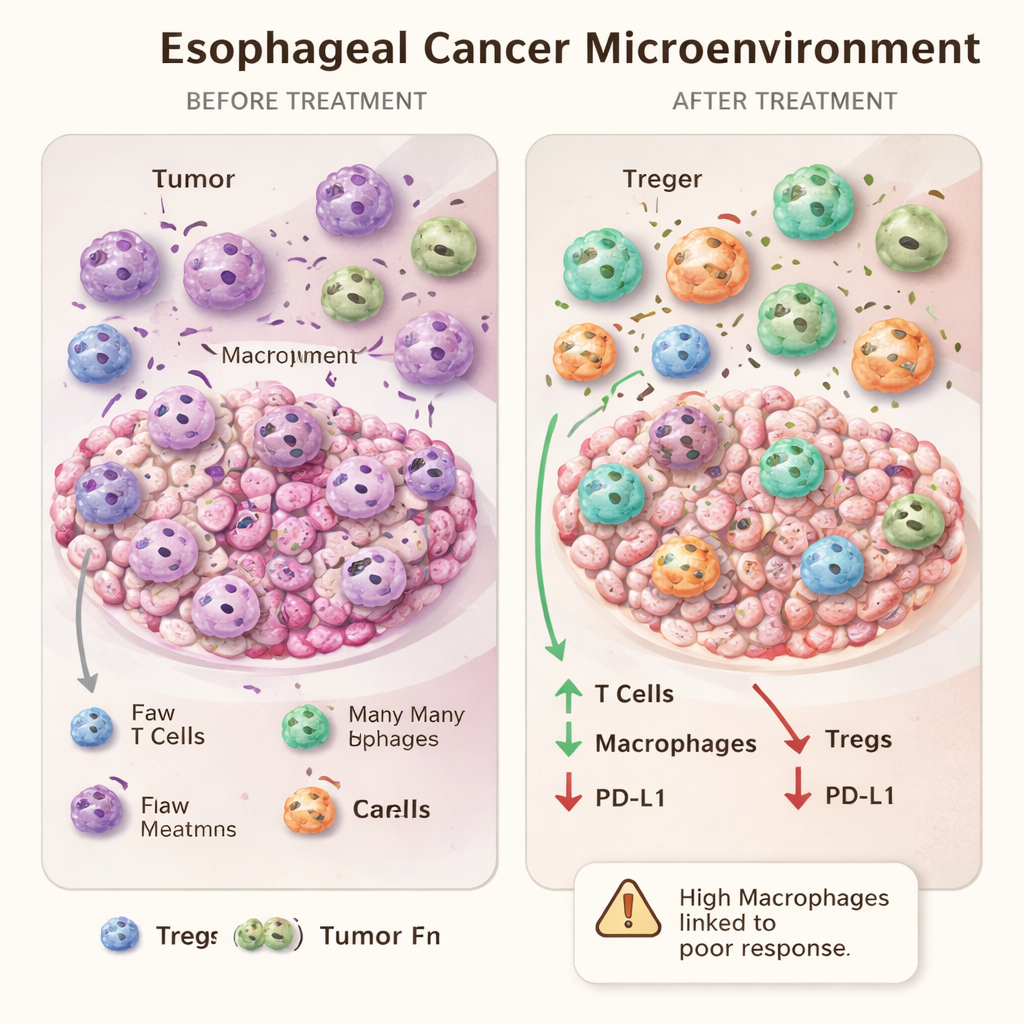
Wanneer meer immuuncellen mogelijk resistentie signaleren
Een van de meest intrigerende bevindingen kwam uit de vergelijking van de uitersten van behandelrespons. Patiënten bij wie tumoren onder de microscoop volledig verdwenen, verschilden bij aanvang niet van slechte responders wat betreft de immuuncellen rond hun kanker. Na behandeling hadden slechte responders echter hogere aantallen macrofagen in hun tumorgebieden dan complete responders. In plaats van een simpel teken van sterke immuniteit, kan een overvloed aan macrofagen na therapie wijzen op een uitgeputte of gekantelde respons die de tumor heeft geleerd te exploiteren. Dit ondersteunt het idee dat sommige macrofagen, met name M2-achtige typen, de overleving van de tumor en resistentie kunnen bevorderen.
Wat dit betekent voor toekomstige zorg
Voor patiënten en clinici is de kernboodschap dat de biologie rond een slokdarmtumor — de micro-omgeving — gevormd wordt door roken, tumortype, ziekte-ernst en door de behandelingen zelf. Standaard chemo en chemoradiatie verkleinen niet alleen tumoren; ze rekruteren en herschikken ook immuuncellen op manieren die de lange termijn controle van de ziekte kunnen bevorderen of belemmeren. De studie suggereert dat het tellen van bepaalde immuuncellen, met name macrofagen, vóór en na therapie mogelijk kan helpen voorspellen wie behandeling zal weerstaan en wie baat kan hebben bij aanvullende middelen die deze cellen of de PD-1/PD-L1-route richten. Hoewel grotere vervolgonderzoeken nodig zijn, brengt dit werk ons dichter bij het afstemmen van slokdarmkankergeneeskunde, niet alleen op de genetica van de tumor, maar ook op het dynamische ecosysteem dat de tumor omringt.
Bronvermelding: Fasquelle, F., Teixeira Farinha, H., Sempoux, C. et al. The tumor microenvironment in esophageal cancer and its association with clinical features and neoadjuvant treatment response. Sci Rep 16, 5664 (2026). https://doi.org/10.1038/s41598-026-36537-8
Trefwoorden: slokdarmkanker, tumor-micro-omgeving, immuuncellen, chemoradiatie, immunotherapie