Clear Sky Science · nl
Gastheer m6A-modificaties vormen microbiota die celspecifieke ferroptose aansturen als causale route naar chronische luchtwegaandoeningen
Waarom uw microben van belang zijn voor uw longen
Chronische ademhalingsproblemen zoals astma en chronische obstructieve longziekte (COPD) worden meestal toegeschreven aan roken, vervuiling of allergieën. Deze studie suggereert een andere, minder voor de hand liggende speler: de biljoenen microben die in onze darmen en op onze huid leven. Met grootschalige genetische gegevens tonen de auteurs aan dat bepaalde microben niet alleen met longziekte samengaan, maar er mogelijk aan bijdragen — via subtiele chemische veranderingen in onze cellen en een vorm van door ijzer aangedreven celschade. Inzicht in dit verborgen netwerk kan uiteindelijk leiden tot nieuwe manieren om chronische luchtwegaandoeningen te voorkomen of te behandelen door onze microben en hun moleculaire paden in gezondere richtingen te sturen.
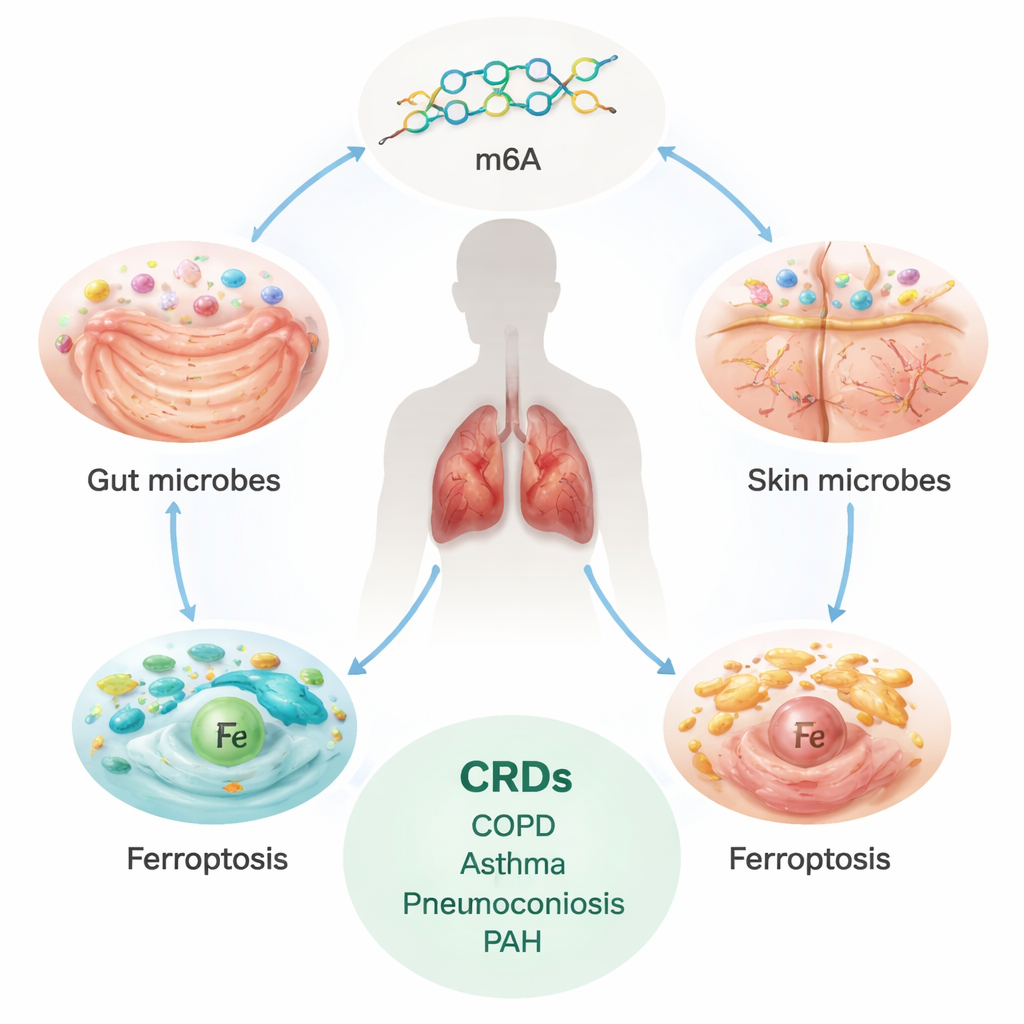
De verborgen last van chronische longziekten
Chronische luchtwegaandoeningen, waaronder COPD, astma, interstitiële longziekte (ILD), pneumoconiose en pulmonale arteriële hypertensie (PAH), treffen wereldwijd honderden miljoenen mensen en veroorzaken jaarlijks miljoenen doden. Deze aandoeningen vorderen vaak langzaam maar onverbiddelijk, met littekenvorming of herstructurering van de longen en bloedvaten als gevolg, waardoor mensen kortademig raken. Huidige behandelingen richten zich voornamelijk op symptoomcontrole; ze stoppen of keren de onderliggende schade niet volledig om. Dat heeft wetenschappers ertoe aangezet op zoek te gaan naar diepere, oorzakelijke factoren, vooral naar factoren die mogelijk kunnen worden aangepast voordat ernstige ziekte optreedt.
Microbiële buren in de darm en op de huid
We weten nu dat de darm en de huid complexe microbiele gemeenschappen herbergen die het immuunsysteem trainen, het metabolisme vormen en barrièrefuncties in stand houden. Maar drijven deze microben werkelijk longziekte aan, of veranderen ze simpelweg nadat mensen ziek worden? Om oorzaak en gevolg te ontwarren, gebruikten de onderzoekers een methode genaamd Mendeliaanse randomisatie, die natuurlijke genetische verschillen tussen mensen aanwendt als een soort levenslange "proef." Ze combineerden genetische gegevens over honderden darm- en huidmicrobe-typen met gegevens over vijf belangrijke chronische longziekten uit grote Europese studies, en testten of aangeboren neigingen naar hogere of lagere niveaus van specifieke microben verband houden met het risico op elke ziekte.
Microben die de longen helpen of schaden
De analyse identificeerde tientallen darmmicroben die het risico op elke ademhalingsziekte verhoogden of verlaagden, vaak in ziekte-specifieke patronen. Zo leken bepaalde darmbacteriën bescherming te bieden tegen COPD, astma of PAH, terwijl andere de kans op ILD of COPD vergrootten. Huidmicroben lieten meer bescheiden maar nog steeds detecteerbare verbanden zien, waarbij sommige soorten met hoger risico en andere met lager risico geassocieerd waren bij verschillende aandoeningen. Het team keerde ook de analyserichting om en vond dat genetisch risico voor COPD, astma en andere longziekten op zijn beurt veranderingen in zowel darm- als huidmicrobiota voorspelde. Dit tweerichtingsverkeer suggereert een feedbacklus: microben kunnen helpen longziekte vorm te geven, en longziekte kan onze microbiale ecosystemen hervormen.
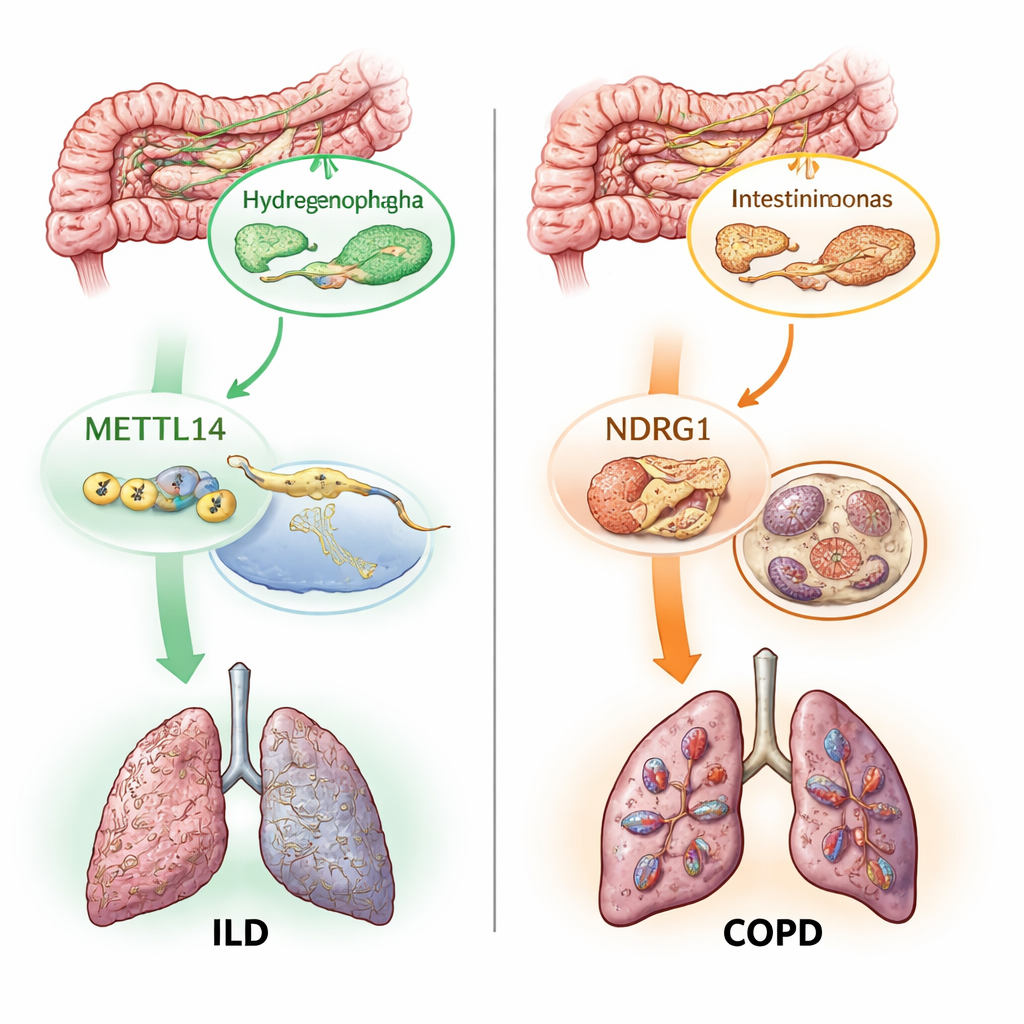
Twee moleculaire schakelaars: RNA-tags en door ijzer gedreven celdood
Buiten het in kaart brengen welke microben relevant zijn, onderzochten de auteurs hoe deze microscopische partners longweefsel zouden kunnen beïnvloeden. Ze concentreerden zich op twee moleculaire processen die al worden verdacht van betrokkenheid bij longschade. De eerste, m6A-modificatie genoemd, is een klein chemisch label dat aan RNA wordt toegevoegd en de manier waarop genen aan- en uitgezet worden bijstuurt. De tweede, ferroptose, is een vorm van ijzerafhankelijke celdood die wordt aangedreven door ongecontroleerde oxidatie van vetten in celmembranen. Met genetische proxies voor 19 m6A-gerelateerde genen en honderden ferroptose-gerelateerde genen testten ze of veranderingen in deze paden causaal verband houden met longziekte. Ze vonden dat één m6A-schrijvergen, METTL14, gekoppeld was aan een lager risico op ILD, en dat meerdere ferroptose-genen, waaronder NDRG1, geassocieerd waren met een hoger risico op COPD, ILD en astma.
De verbanden leggen: van microben naar cellen naar ziekte
Het meest nieuwe aan het werk was het traceren van hoe deze onderdelen zich in ketens van oorzaak en gevolg ontvouwen. Statistische mediationanalyses suggereerden dat een deel van METTL14’s beschermende effect op ILD verloopt via veranderingen die het induceert in een specifieke darmbacterie genaamd Hydrogenophaga. In een ander pad leek een specifieke darmbacterie, Intestinimonas massiliensis, het COPD-risico deels te beïnvloeden door NDRG1 en het ferroptose-zelfmoordprogramma te activeren. Het team controleerde vervolgens longweefselgegevens van mensen en bevestigde dat zowel METTL14 als NDRG1 anders tot expressie komen in zieke versus gezonde monsters. Ten slotte, met behulp van single-cell genetische kaarten van immuuncellen, pinpointten ze het schadelijke effect van NDRG1 op COPD naar één subset van immuuncellen, een type monocyten, wat suggereert dat toekomstige geneesmiddelen die op dit gen richten mogelijk celspecifiek moeten werken.
Wat dit betekent voor toekomstige behandelingen
Voor niet-specialisten is de kernboodschap dat longgezondheid niet alleen afhangt van wat we inademen, maar ook van de microben die in en op ons leven en de moleculaire schakelaars die ze binnen onze cellen omzetten. Deze studie kan niet elke stap experimenteel bewijzen en is hoofdzakelijk beperkt tot mensen van Europese afkomst, maar ze biedt sterke genetische aanwijzingen dat darmmicroben, RNA-tags zoals m6A en door ijzer aangedreven celdood een verbonden pad vormen dat leidt tot chronische longschade. Op de lange termijn kan dit onderzoeksveld nieuwe strategieën inspireren die microbioom-gebaseerde therapieën combineren met geneesmiddelen die METTL14, NDRG1 of ferroptose targeten, met het doel niet alleen symptomen te verlichten maar de biologische circuits te onderbreken die chronische luchtwegaandoeningen laten voortschrijden.
Bronvermelding: Zhang, J., Liu, X., Liu, X. et al. Host m6A modifications shape microbiota that drives cell specific ferroptosis as a causal pathway to chronic respiratory diseases. Sci Rep 16, 5809 (2026). https://doi.org/10.1038/s41598-026-36513-2
Trefwoorden: darmmicrobioom, chronische longziekte, astma en COPD, RNA-epigenetica, celsterftepaden