Clear Sky Science · nl
Het voorspellen van verstopte dialysatorvezels is moeilijk door grote intrapatiëntvariabiliteit en beperkte bruikbaarheid van trombinegeneratiemarkers
Waarom bloedklontering in de dialysemachine ertoe doet
Voor mensen van wie de nieren niet meer werken, is hemodialyse een levensondersteunende behandeling die meerdere keren per week het bloed reinigt. Het werk vindt plaats in een cartridge met duizenden kleine holle vezels. Wanneer die vezels verstopt raken met gestold bloed, wordt de behandeling minder effectief en mogelijk onveiliger. Artsen proberen dit te voorkomen door bloedverdunners toe te dienen, maar te veel daarvan verhoogt het bloedingsrisico. Deze studie stelt een schijnbaar simpele vraag met grote praktische consequenties: kunnen we betrouwbaar meten en voorspellen hoeveel van deze vezels dichtslibben tijdens routinematige dialyse?
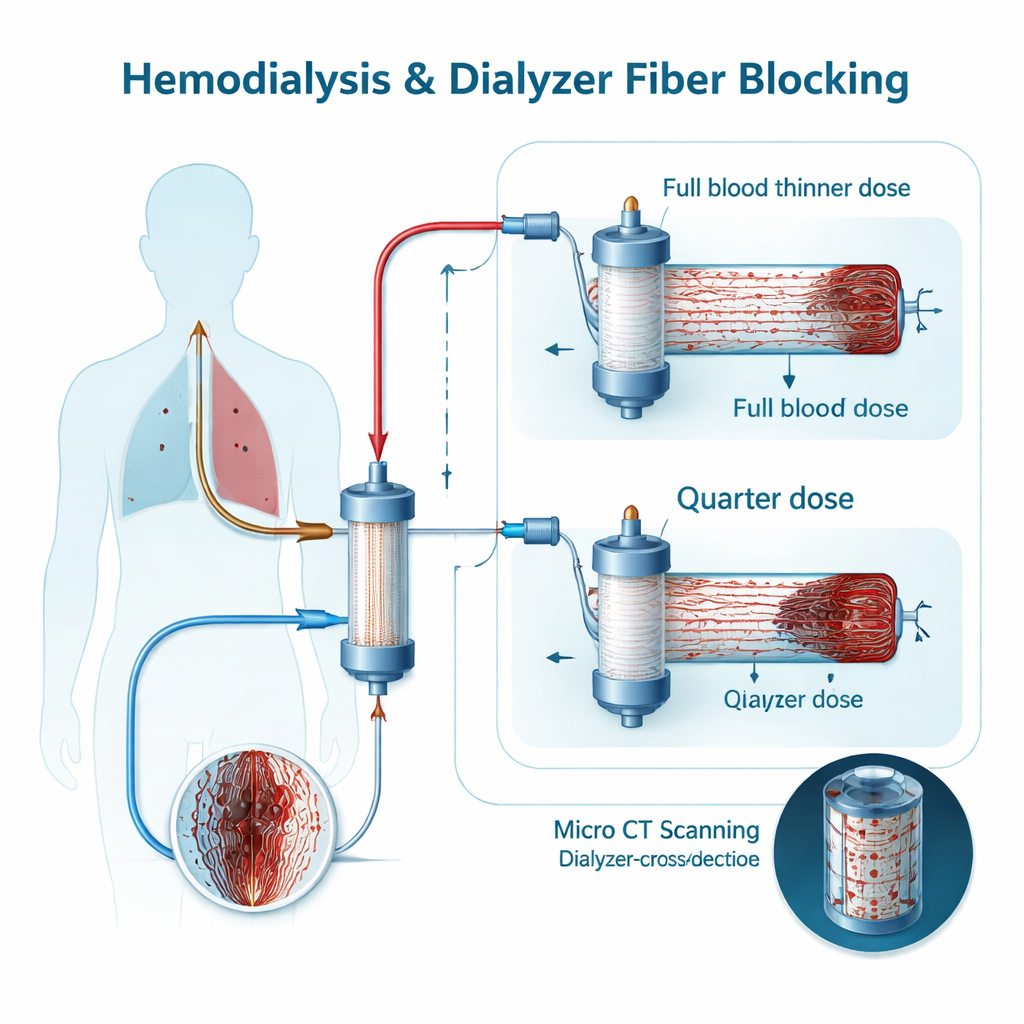
Een blik in het filter
Vandaag de dag is de enige echt nauwkeurige manier om te zien hoeveel vezels geblokkeerd zijn het scannen van de gebruikte dialysator met micro‑computertomografie (micro‑CT), een soort hoge‑resolutie 3D‑röntgen. Daarmee kun je letterlijk tellen hoeveel van de ongeveer 13.000 vezels na een sessie open blijven. Dat detailniveau is uitstekend voor onderzoek maar te traag en te complex voor dagelijkse zorg. In klinieken vertrouwen verpleegkundigen in plaats daarvan op een snelle visuele score van hoe “rood” het filter eruitziet en op het uiteindelijke droge gewicht van het filter, die beide ruwe benaderingen van klontering zijn. De onderzoekers wilden weten hoeveel deze verschillende maatstaven van de ene behandeling op de andere binnen dezelfde persoon fluctueren, en of een verfijnde bloedtest een eenvoudigere, vroegere waarschuwing zou kunnen geven.
Minder versus meer bloedverdunner testen
Het team bestudeerde tien stabiele dialysepatienten gedurende twee weken. Iedere persoon had drie sessies met de gebruikelijke dosis laagmoleculair heparine als bloedverdunner en drie sessies met slechts een kwart van die dosis, in gerandomiseerde volgorde. Na elke behandeling werd de dialysator gespoeld, gedroogd, gewogen, visueel beoordeeld door twee onafhankelijke waarnemers en gescand met micro‑CT om het percentage open vezels te berekenen. Zoals verwacht leidde het gebruik van slechts een kwart van de normale dosis tot meer verstopte filters: visuele scores waren slechter, dialysatoren wogen meer en micro‑CT toonde een daling van het aandeel open vezels van een mediaan van ongeveer 94% naar 74%. De methoden onderscheidden dus duidelijk meer versus minder klontering in het algemeen.
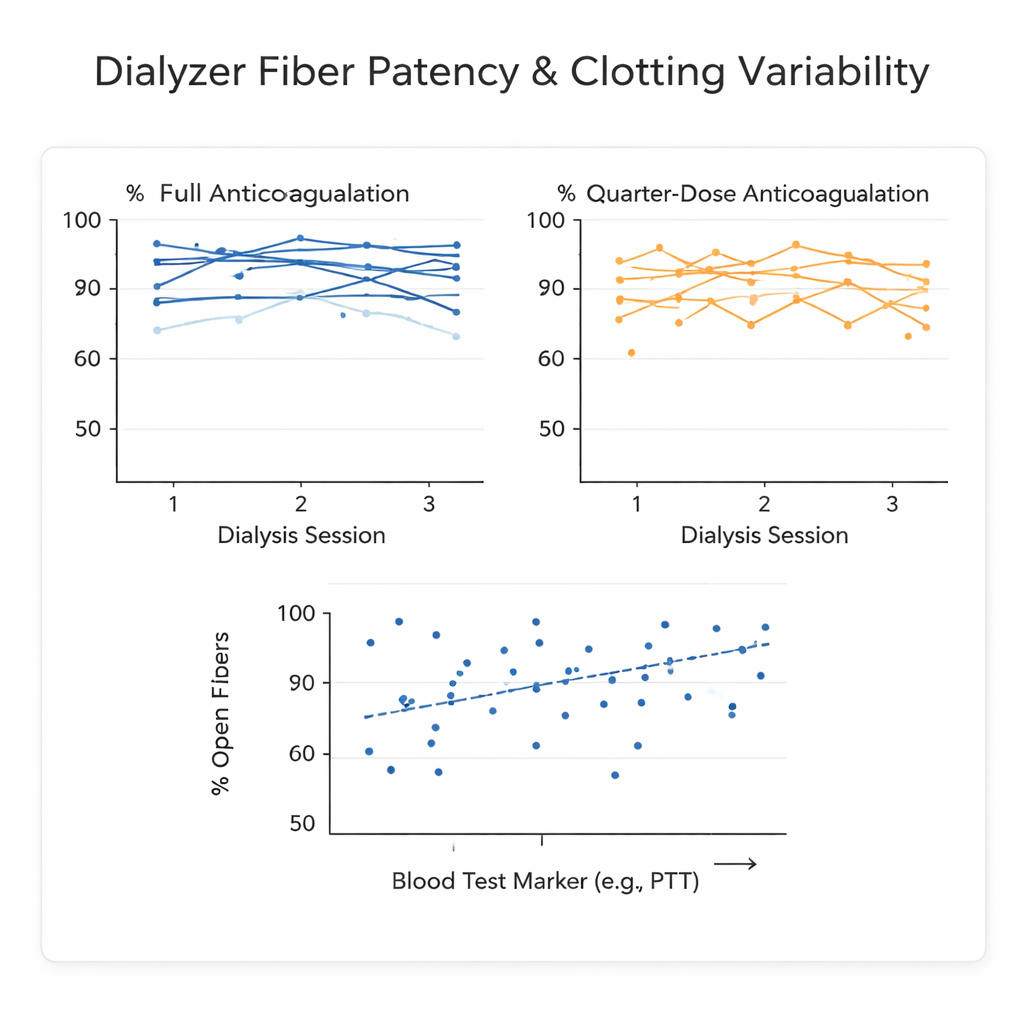
Grote dag‑tot‑dag schommelingen bij dezelfde patiënt
Een belangrijke bevinding was hoeveel de resultaten van de ene sessie op de andere sprongen binnen dezelfde persoon, zelfs bij dezelfde dosis bloedverdunner. De gebruikte statistische maat, de intraklassecorrelatiecoëfficiënt, bleef rond 0,5 voor zowel de massa van de dialysator als voor het aandeel open vezels op micro‑CT — ruim onder de vaak gewenste 0,7 drempel. Simpel gezegd waren de natuurlijke dag‑tot‑dag veranderingen binnen een patiënt bijna net zo groot als de verschillen tussen patiënten. Die schommeling wordt waarschijnlijk gedreven door biologische factoren zoals laaggradige infecties, ontsteking of subtiele veranderingen in de vasculaire toegang, en niet door enige onnauwkeurigheid van de scantest zelf.
Waarom een veelbelovende bloedtest tekortschiet
De onderzoekers onderzochten ook een volbloed‑“trombinegeneratie”‑assay, die volgt hoe snel en hoe krachtig bloed trombine vormt, een centraal stollingseiwit. Omdat deze test plaatjes en rode bloedcellen omvat, zou hij de algehele neiging tot stollen beter vastleggen dan klassieke laboratoriumtests zoals stollingstijden. Verschillende parameters werden voor en na elke dialysesessie gemeten. Twee tijdgerelateerde maten — de vertraging voordat stolling aantrekt en de tijd tot de piek van trombine — toonden matige correlaties met hoeveel vezels aan het einde open waren, maar alleen wanneer ze na de dialyse werden gemeten. De spreiding in de gegevens was echter groot: veel sessies met vergelijkbare bloedtestwaarden eindigden met heel verschillende graden van vezelverstopping. Dat betekent dat deze tests niet betrouwbaar kunnen voorspellen of bij een bepaalde patiënt op een bepaalde dag de dialysator sterk zal klonteren.
Wat dit betekent voor patiënten en onderzoekers
Voor patiënten en clinici is de hoofdboodschap zowel geruststellend als waarschuwend. Sterkere bloedverdunning houdt gemiddeld de dialysator meer open, maar de mate van klontering kan sterk variëren van de ene sessie op de andere bij dezelfde persoon. Een enkele scan, gewicht of visuele indruk van een gebruikt filter is daarom een rumoerige momentopname, geen stabiel visitekaartje. Onderzoekers die toekomstige studies over klontering bij dialyse ontwerpen, moeten rekening houden met deze hoge binnen‑patiëntvariabiliteit bij het kiezen van steekproefgroottes en het interpreteren van resultaten. En hoewel geavanceerde bloedtesten van stollingsgedrag interessant zijn, zijn ze nog niet nauwkeurig genoeg om dagelijkse beslissingen te sturen over hoeveel bloedverdunner een individuele patiënt nodig heeft.
Bronvermelding: Eloot, S., Mertens, T., Josipovic, I. et al. Predicting dialyzer fiber blocking is hard due to high intrapatient variability and limited utility of thrombin generation markers. Sci Rep 16, 5913 (2026). https://doi.org/10.1038/s41598-026-36507-0
Trefwoorden: hemodialyse, verstopping van de dialysator, antistolling, trombinegeneratie, micro‑CT‑beeldvorming