Clear Sky Science · nl
NEK7-fosforylering van cortactine moduleert de migratiecapaciteit van cellen die EML4-ALK V3 tot expressie brengen
Waarom celbeweging van belang is bij longkanker
Kanker wordt levensbedreigend wanneer cellen leren te reizen. Bij niet-kleincellige longkanker verspreiden sommige tumoren zich sneller door het lichaam dan andere, en een belangrijke veroorzaker is een defect fusie-eiwit genaamd EML4-ALK. Een specifieke versie, bekend als variant 3 (V3), wordt geassocieerd met bijzonder agressieve ziekte en slechte reacties op gerichte middelen. Deze studie stelt een basale maar cruciale vraag: wat stelt deze door V3 aangedreven kankercellen in staat om hun vorm zo efficiënt te veranderen en te bewegen, en kunnen we de moleculaire onderdelen aanwijzen die dit mogelijk maken?
Een hypermigrerende longkankervariant
Artsen weten al lang dat slechts een minderheid van de longkankers de EML4-ALK-fusie draagt, maar patiënten wier tumoren de V3-vorm tot expressie brengen doen het doorgaans slechter dan degenen met andere varianten. Onder de microscoop zien V3-expresserende cellen er anders uit: in plaats van compact en met een keitjesachtige vorm zijn ze uitgerekt in lange, dunne vormen met verlengde uitstulpingen, gelijkend op mobiele cellen. Eerder werk toonde aan dat dit gedrag afhangt van twee enzymen, NEK9 en NEK7, die fungeren als moleculaire schakelaars in cellen. De cruciale downstream-doelwitten van deze schakelaars—degenen die direct het interne skelet van de cel hervormen—waren echter nog weinig begrepen.
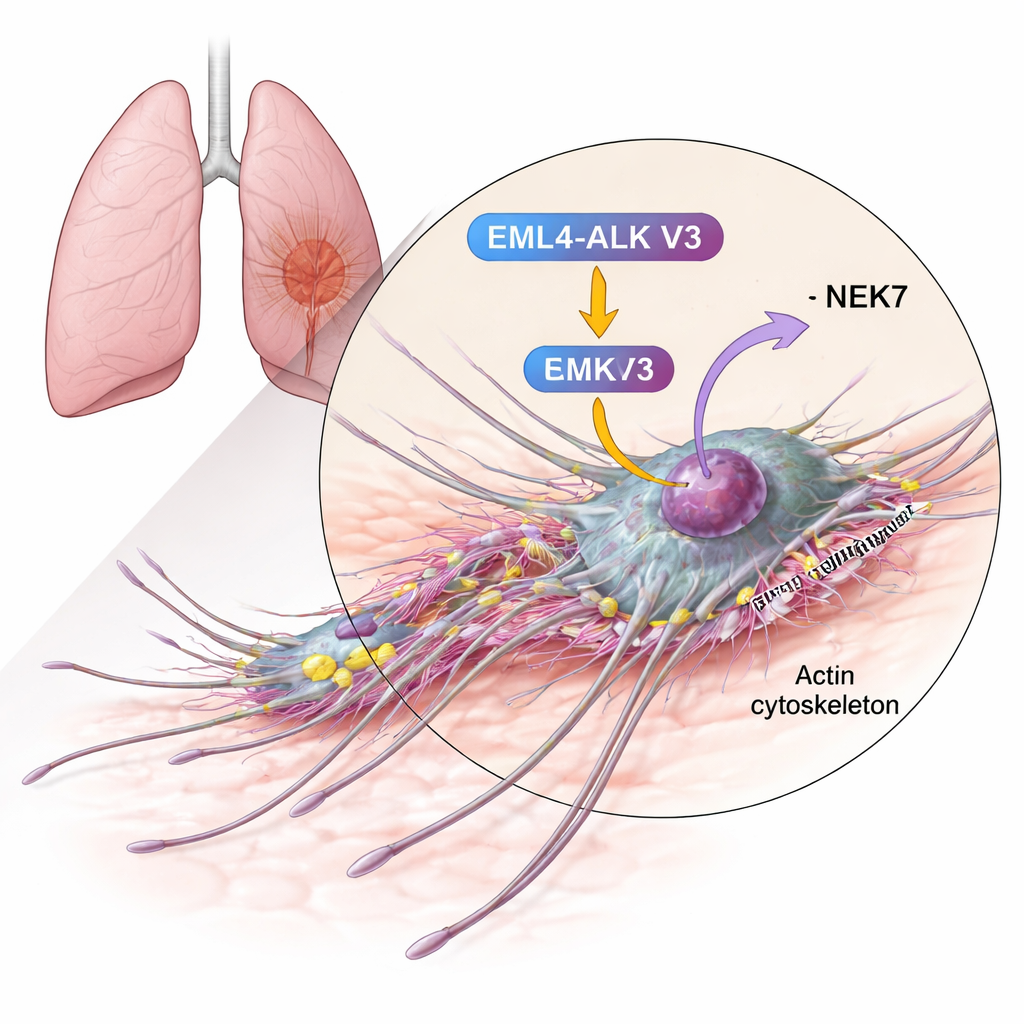
Een bewegingsproteïne koppelen aan een agressieve fusie
De auteurs concentreerden zich op cortactine, een eiwit dat al bekendstaat als overvloedig aanwezig in veel invasieve kankers en dat helpt bij het opbouwen van netwerken van actinefilamenten die het celmembraan naar voren duwen. Met biochemische tests lieten ze zien dat cortactine chemisch gemodificeerd kan worden (gefosforyleerd) door NEK6 en, nog sterker, door NEK7. De enzymen voegen fosfaatgroepen toe aan specifieke serineresiduen binnen het actine-bindende domein van cortactine—net dat segment dat actinevezels grijpt en vertakte netwerken stabiliseert. Wanneer NEK7 aanwezig was, was cortactine op meer plaatsen en in grotere mate gefosforyleerd dan bij NEK6, wat suggereert dat NEK7 hier de primaire regulator is.
Cortactine uitschakelen remt kankercelmigratie
Om te onderzoeken wat cortactine daadwerkelijk doet in levende cellen, namen de onderzoekers het weg met RNA-interferentie in cellen die waren geconstrueerd om NEK9 of NEK7 te activeren, of om zelf EML4-ALK V3 tot expressie te brengen. In alle drie de omstandigheden viel de opvallende uitgerekte, mesenchymale vorm uiteen: cellen werden platter en ronder, verloren hun lange uitstulpingen en vormden in plaats daarvan dikke, rechte actine "stressvezels" die het cellichaam overkruisten. Meerdere migratie-assays—van het sluiten van kunstmatige "wonden" in een cellaag tot het volgen van individuele cellen en het meten van beweging naar een chemische prikkel—lieten zien dat deze zeer beweeglijke cellen zonder cortactine drastisch vertraagden. Vergelijkbare effecten werden waargenomen in gevestigde longkankercellijnen die van nature EML4-ALK V3 dragen, wat de klinische relevantie van de route benadrukt.
Fijne filamenten en scherpe punten aan het voortstuwende front
Hoge-resolutiebeeldvorming in bronchiale epitheelcellen toonde een nog gedetailleerder beeld. EML4-ALK V3-expressieve cellen produceerden veel fijne, soms vertakte, filopodia-achtige uitsteeksels die hun protrusies bestreken. Op de punten en vertakkingsplaatsen van deze structuren verzamelden cortactine, EML4-ALK V3, NEK7 en een gefosforyleerde vorm van cortactine zich samen. Deze nauwe co-locatie suggereert een gefocuste "constructieplaats" waar NEK7 cortactine wijzigt om de delicate, vertakte actinenetwerken te bouwen en te onderhouden die de cel helpen sturen. Wanneer cortactine werd verwijderd, verdwenen deze verfijnde uitstulpingen en werd invasieve groei vanuit driedimensionale tumorachtige sferen in een omringende gel sterk verminderd.
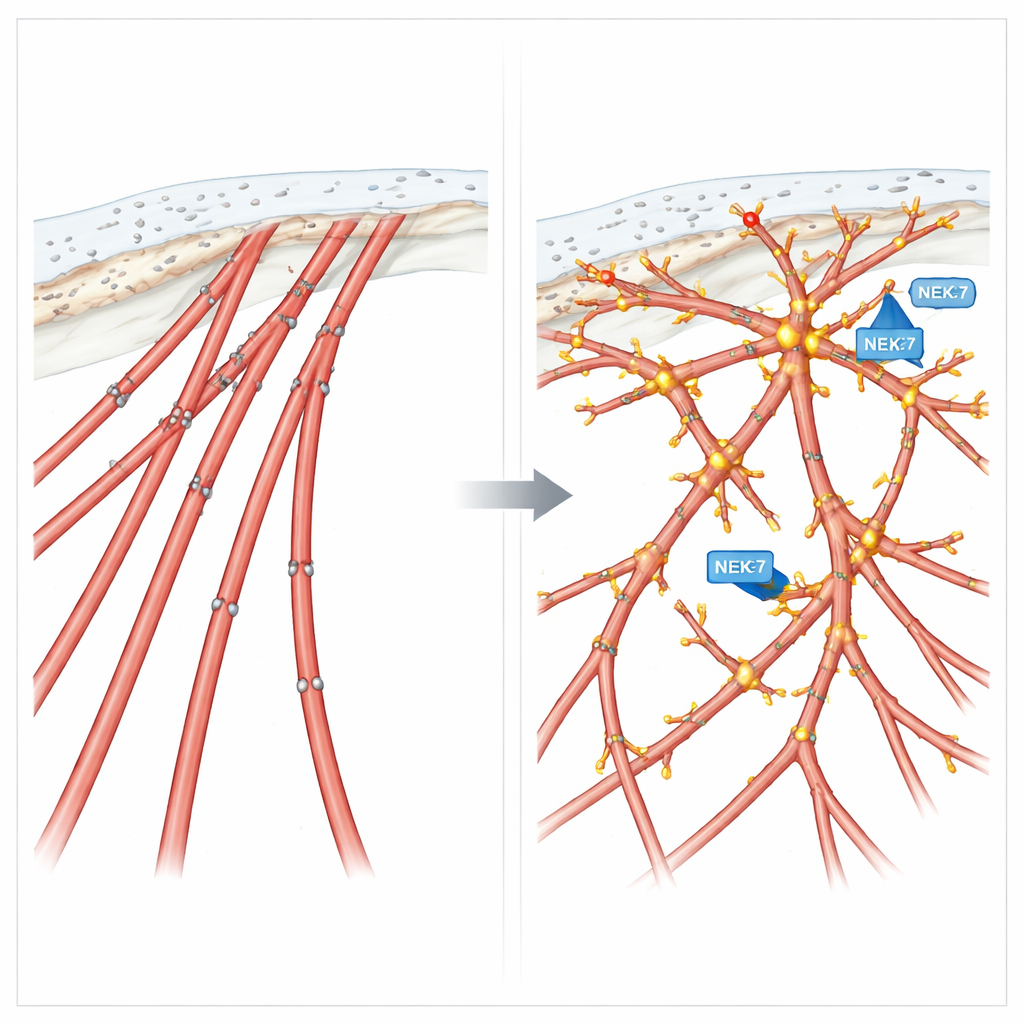
Fosforylering als migratiedraaiknop
Om te testen hoe deze chemische etiketten op cortactine het gedrag beïnvloeden, maakten de onderzoekers twee ontworpen versies van het eiwit: een fosfo-mimetische vorm die constante fosforylering op vier sleutelplaatsen nabootst, en een fosfo-null vorm die daar niet gefosforyleerd kan worden. Cellen die de mimetische versie tot expressie brachten ontwikkelden veel filopodia-achtige uitstulpingen en vertoonden verbeterde gerichte migratie, vergelijkbaar met cellen met actieve NEK7 of EML4-ALK V3. Daarentegen vormden cellen die de niet-fosforyleerbare versie uitdrukten rigide stressvezels, verloren die fijne uitstulpingen en bewogen op een snelle maar doelloze manier—goed in zwerven, slecht in het volgen van een signaal. In driedimensionale culturen dreef deze fosfo-null cortactine invasieve uitgroei die ongeordend was in plaats van precies geleid.
Wat dit betekent voor het begrijpen—en richten van—verspreiding
In simpele bewoordingen toont de studie aan dat de agressieve EML4-ALK V3-longkankervariant een normaal celvormend systeem kaapt. Door NEK7 te activeren veroorzaakt hij fosforylering van cortactine op specifieke sites binnen het actine-bindende domein. Deze modificatie stelt cortactine in staat fijn vertakte actinestructuren en filopodia-achtige uitstulpingen te bouwen die snelle, gerichte celmigratie en invasie ondersteunen. Het verstoren van cortactine of zijn fosforylering keert het systeem om: cellen bewegen nauwelijks of bewegen chaotisch zonder richting. Deze inzichten onthullen een concrete moleculaire keten—van een kankerveroorzakende fusie, via NEK7, naar cortactine en het actine-cytoskelet—die helpt verklaren waarom sommige longkankers zo effectief uitzaaien, en wijzen op nieuwe manieren om hun beweging te vertragen of te misleiden.
Bronvermelding: Richardson, E.L., Knebel, A., Straatman, K.R. et al. NEK7 phosphorylation of cortactin modulates the migratory capacity of cells expressing EML4-ALK V3. Sci Rep 16, 6407 (2026). https://doi.org/10.1038/s41598-026-36484-4
Trefwoorden: niet-kleincellig longkanker, EML4-ALK V3, celmigratie, cortactine, actine-cytoskelet