Clear Sky Science · nl
ATF4 reguleert mitochondriale disfunctie en mitofagie, wat bijdraagt aan apoptose van het cornea‑endothelium
Waarom het venster van het oog troebel kan worden
Onze hoornvliezen — de heldere voorruiten van de ogen — blijven doorzichtig dankzij een dunne, hardwerkende laag cellen aan hun binnenzijde. Bij Fuchs’ endotheliale corneale dystrofie (FECD) verliezen miljoenen mensen deze cellen langzaam, wat leidt tot zwelling, wazig zicht en vaak tot corneatransplantaties. Deze studie stelt een eenvoudige maar cruciale vraag: wat zet deze cellen ertoe aan te sterven, en zou het uitschakelen van één moleculaire “schakelaar” hen kunnen redden?
Een kwetsbare cellaag die het zicht helder houdt
Het cornea‑endothelium is een enkel vel hexagonale cellen dat voortdurend vocht uit de cornea pompt om die helder te houden. Bij FECD raken deze cellen gestrest en verdwijnen ze geleidelijk, terwijl bultjes van abnormaal materiaal, guttae genoemd, zich op het onderliggende membraan ophopen. Omdat er geen goedgekeurde medicijnen voor FECD zijn en corneatransplantaties de belangrijkste behandeling vormen, proberen onderzoekers precies te begrijpen hoe stress binnen deze cellen hen richting celdood duwt. Eerder werk wees afzonderlijk op spanning in twee belangrijke cellulaire compartimenten — het endoplasmatisch reticulum (de eiwitvouwwerf van de cel) en mitochondriën (de energiecentrales van de cel) — maar hoe deze twee stressreacties met elkaar communiceren bleef onduidelijk.
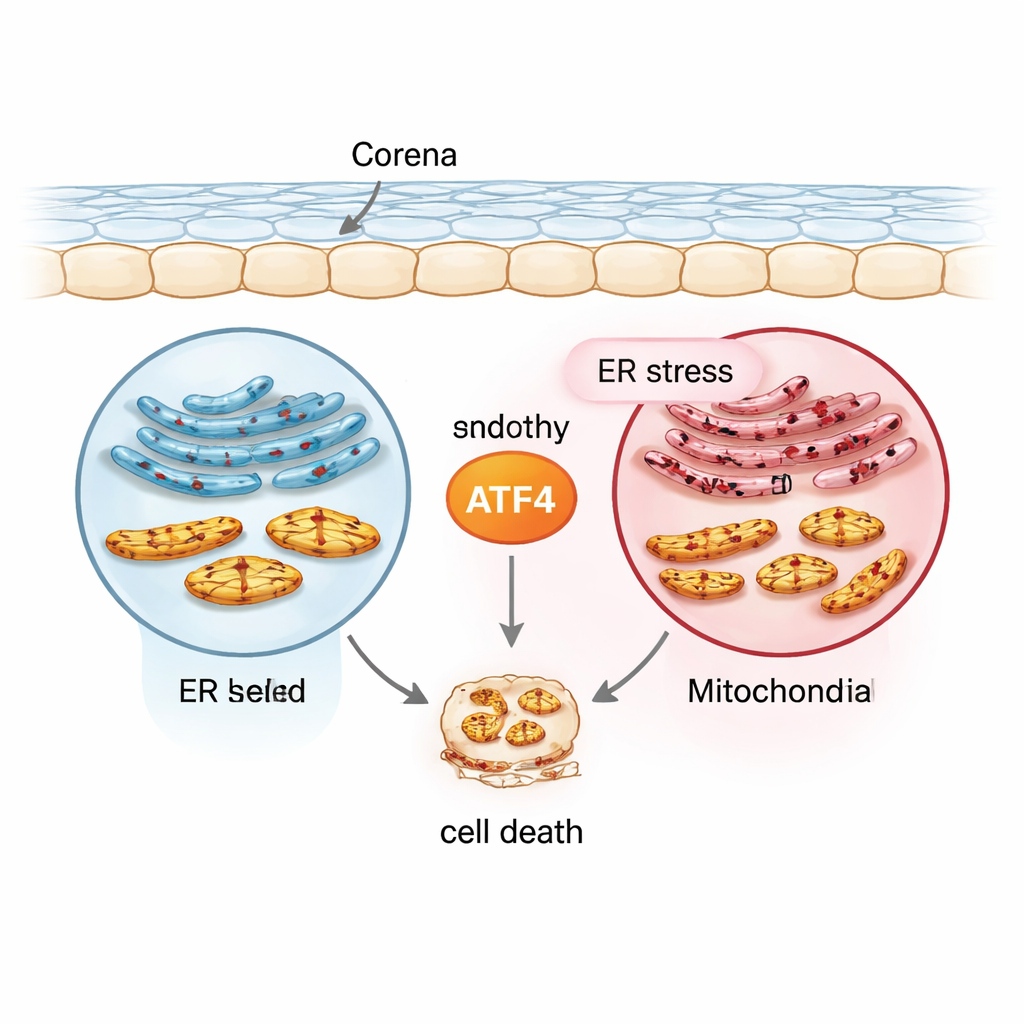
De stressboodschapper in het middelpunt: ATF4
Het team richtte zich op een eiwit genaamd ATF4, een transcriptiefactor die vele stress‑responsgenen aan of uit zet. Met gebruik van een normale menselijke cornea‑endotheelcellijn (21T), een FECD‑achtige cellijn met de ziekte‑gerelateerde TCF4‑repeatexpansie (F35T), primaire menselijke cornea‑endotheelcellen en muismodellen blootgesteld aan ultraviolet A (UVA) licht, creëerden ze een reeks omstandigheden die chronische stress nabootsen. Ze wekten endoplasmatisch reticulum‑stress op met een middel genaamd tunicamycine en maten vervolgens ATF4 en andere merkers. Vergeleken met normale cellen startten FECD‑achtige cellen met hogere niveaus van ATF4 en verwante stressproteïnen, en ATF4 nam onder chronische stress nog verder toe in zowel gekweekte cellen als menselijk corneaweefsel. Dit patroon plaatste ATF4 op het kruispunt tussen vroege beschermende reacties en latere, zelfdestructieve signalering.
Van stroomuitval naar geprogrammeerde celdood
Vervolgens onderzochten de onderzoekers hoe deze stress de mitochondriën beïnvloedde. In FECD‑achtige cellen produceerden mitochondriën minder ATP, verloren ze hun elektrische membraanpotentiaal en braken ze van lange, netwerkachtige vormen in veel kleine fragmenten. Deze veranderingen verergerden wanneer endoplasmatisch reticulum‑stress langdurig bleef. Tegelijkertijd namen klassieke celdoodproteïnen — zoals geactiveerde caspases en het DNA‑herstelproteïne PARP in zijn gekliefde, pro‑dode vorm — toe, terwijl beschermende eiwitten zoals Bcl‑2 afnamen. Samen wijzen deze veranderingen erop dat gestresseerde cornea‑endotheelcellen bij FECD richting mitochondriaveroorzaakte apoptose worden geduwd, een nette maar onomkeerbare vorm van geprogrammeerde celzelfmoord.
Het opruimsysteem stokt bij chronische stress
Normaal gesproken worden zwaar beschadigde mitochondriën verwijderd door een recyclingproces dat mitofagie heet, waarbij ze gemarkeerd en ingesloten worden in kleine zakjes voor afvoer. Het team ontdekte dat vroege mitofagie‑“starter”moleculen (Parkin en LC3) in zowel normale als FECD‑achtige cellen werden aangezet, vooral na stress. Maar essentiële ondersteunende eiwitten waren verminderd, en elektronenmicroscopie liet een opeenhoping zien van gedeeltelijk verteerde mitochondriën gevangen in vesikels. Dit suggereert dat hoewel het opruimproces werd gestart, het niet werd afgerond, waardoor cellen vol defecte energiecentrales achterbleven die de stress en celdood eerder aanwakkeren dan herstel bevorderen.
ATF4 uitschakelen om cellen te redden
Om te testen of ATF4 deze neerwaartse spiraal aandreef, gebruikten de onderzoekers small interfering RNA om ATF4 gedeeltelijk te onderdrukken in gekweekte cornea‑endotheelcellen. Onder dezelfde chronische stress vertoonden cellen met verlaagd ATF4 lagere niveaus van celdoodbevorderende eiwitten, een gezondere mitochondriale membraanpotentiaal, minder fragmentatie en betere overleving in vitaliteitstests. Belangrijk was dat het aantal vastgelopen mitofagie‑structuren afnam, wat suggereert dat verlaging van ATF4 hielp een effectiever evenwicht tussen schade en opruiming te herstellen. In muizen die zo waren gemodificeerd dat ze slechts één werkende kopie van het ATF4‑gen hadden, veroorzaakte UVA‑blootstelling minder activatie van een pro‑dood partnerproteïne, CHOP, en bleef een groter aantal normaal gevormde endotheelcellen behouden vergeleken met muizen met volledige ATF4‑expressie.
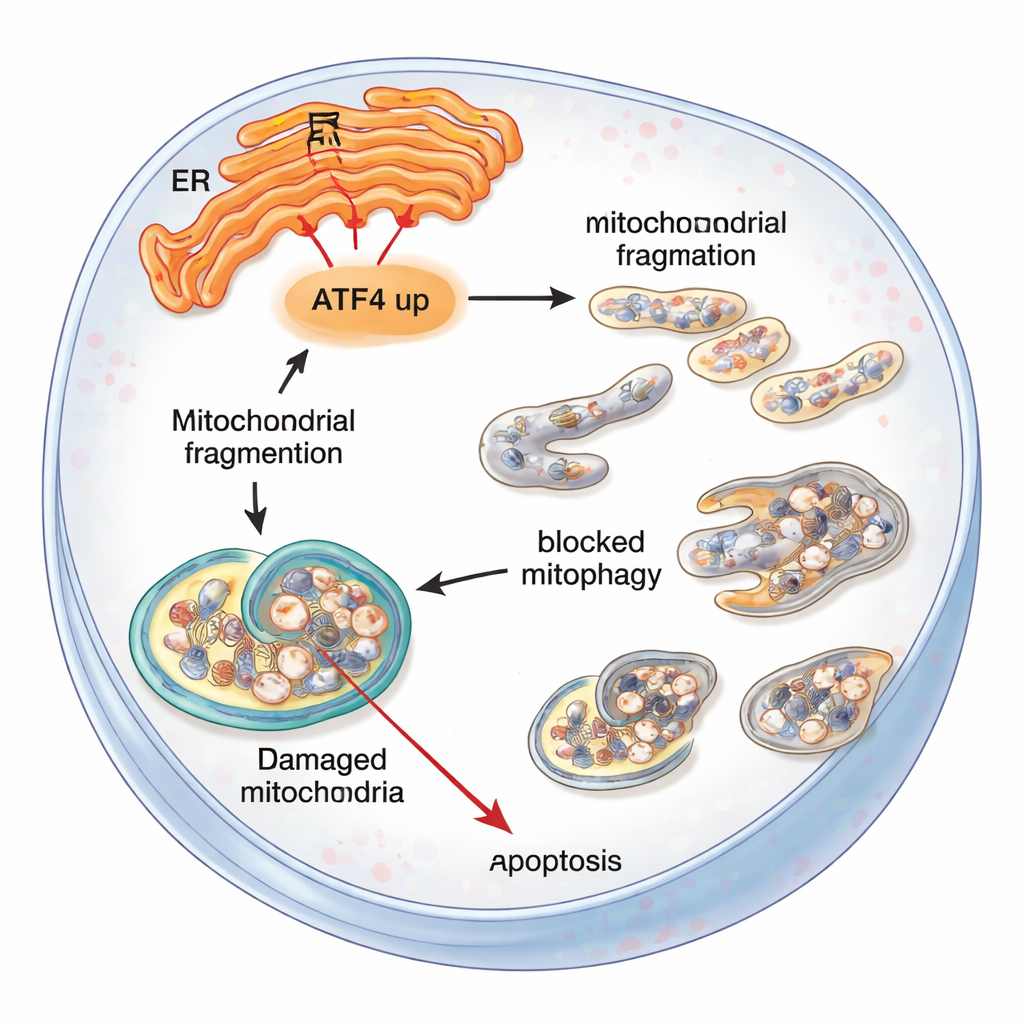
Wat dit betekent voor mensen met FECD
Voor niet‑specialisten is de boodschap dat één stressboodschapper, ATF4, cornea‑endotheelcellen kan doen kantelen van het vermogen om te herstellen naar instorten. Wanneer endoplasmatisch reticulum‑stress langdurig is, draagt ATF4 bij aan verstoring van mitochondriën, blokkeert het het opruimmechanisme van de cel en stimuleert het uiteindelijk deze vitale cellen tot zelfvernietiging. Het terugschakelen van ATF4 — hetzij genetisch in muizen, hetzij met gerichte moleculaire middelen in cellen — beschermt mitochondriën, verbetert afvalverwijdering en houdt meer cellen in leven. Hoewel dit werk zich nog in laboratorium- en diermodellen bevindt, benadrukt het ATF4 en verwante stressroutes als veelbelovende medicatiedoelen die mogelijk op termijn de progressie van Fuchs’ dystrofie kunnen vertragen of voorkomen en de behoefte aan corneatransplantatie kunnen verminderen.
Bronvermelding: Qureshi, S., Kim, S.Y., Lee, S. et al. ATF4 regulates mitochondrial dysfunction and mitophagy, contributing to corneal endothelial apoptosis. Sci Rep 16, 5960 (2026). https://doi.org/10.1038/s41598-026-36453-x
Trefwoorden: Fuchs endotheliale corneale dystrofie, cornea endothelium, mitochondriale stress, mitofagie, ATF4