Clear Sky Science · nl
Een integratieve benadering om nieuwe miRNA-mRNA-interactienetwerken in LMNA-cardiomyopathie te identificeren
Waarom kleine hartregelaars ertoe doen
Gedilateerde cardiomyopathie is een ernstige aandoening waarbij het hart vergroot en verzwakt raakt, wat vaak leidt tot hartfalen, gevaarlijke hartritmestoornissen en zelfs plotseling overlijden. Bij veel families is deze ziekte erfelijk, en veranderingen in een gen dat LMNA heet, zijn vaak de boosdoener. Deze studie stelt een schijnbaar eenvoudige vraag met grote gevolgen: in harten die beschadigd zijn door LMNA-mutaties, welke genen staan aan of uit en welke kleine RNA-moleculen schakelen die genen? Door deze moleculaire gesprekken nauwkeurig in kaart te brengen, wijst het werk op nieuwe manieren om deze agressieve vorm van hartaandoening te voorspellen, te volgen en mogelijk in de toekomst te behandelen.
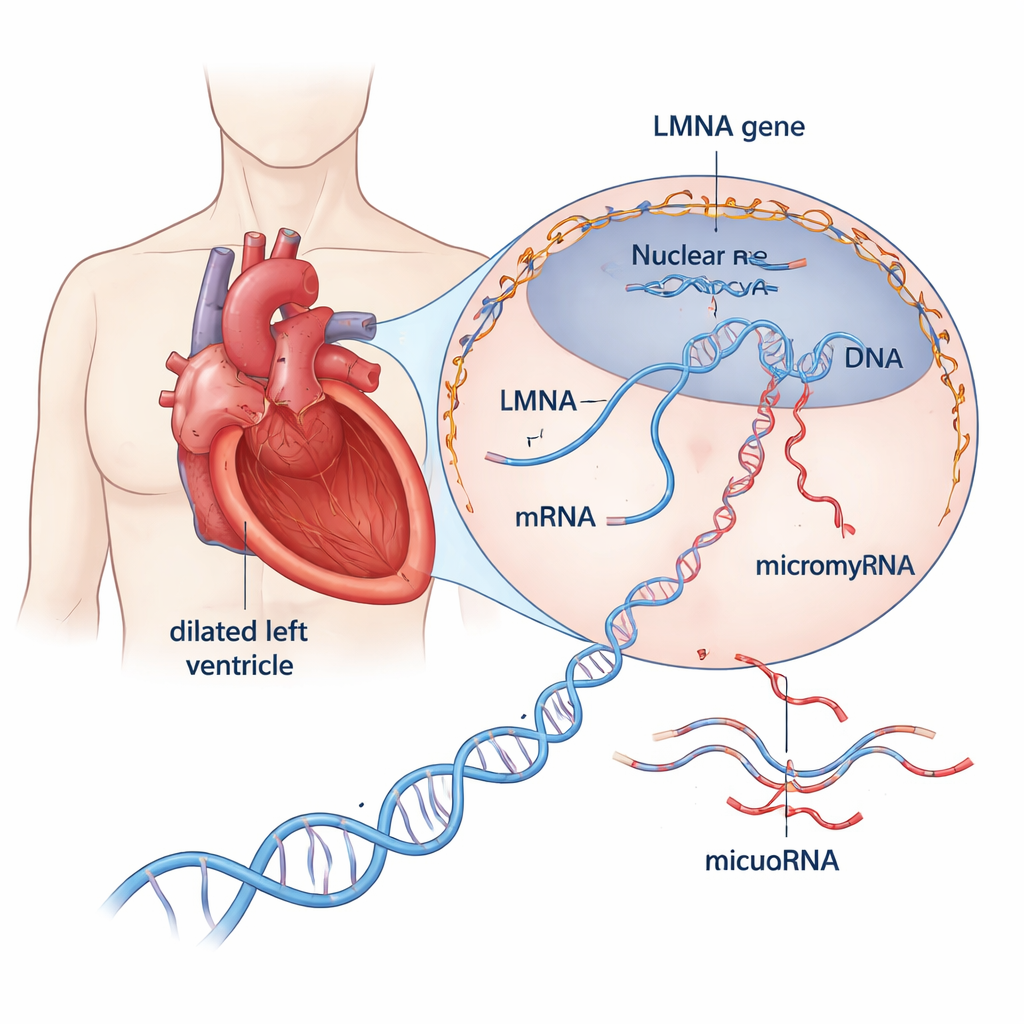
Een nadere blik op een gevaarlijke hartaandoening
Gedilateerde cardiomyopathie rekt en verdunt de belangrijkste pompkamer van het hart, waardoor het vermogen om bloed door het lichaam te pompen verzwakt. Ongeveer een derde tot de helft van de gevallen die vroeger “idiopathisch” werden genoemd, blijkt nu een genetische basis te hebben. Van de meer dan 30 betrokken genen springt LMNA eruit: schadelijke varianten in dit gen verklaren ongeveer 10% van de erfelijke gevallen en worden geassocieerd met snelle ziekteprogressie, vroegtijdige ritmestoornissen en een groot risico op plotselinge hartdood. LMNA maakt structurele eiwitten die een scaffold rond het DNA van de cel vormen, helpen de vorm van de kern te behouden en beïnvloeden welke genen actief zijn. Toch is het nog slecht begrepen hoe foutieve LMNA-eiwitten harten naar falen drijven.
De boodschappen binnen muizenharten volgen
Om dit te onderzoeken gebruikten de onderzoekers een muismodel met een goedbekende LMNA-mutatie (R249W) dat een vorm van gedilateerde cardiomyopathie ontwikkelt die op de menselijke ziekte lijkt. Op 50 weken leeftijd—wanneer de muizen vergrote ventrikels, verminderde pompfunctie en fibrotische littekenvorming laten zien—haalde het team hartweefsel af en onderzocht twee typen RNA: boodschapper-RNA (mRNA), dat instructies voor het maken van eiwitten draagt, en microRNA (miRNA), korte niet-coderende strengetjes die genactiviteit bijstellen door specifieke mRNAs te blokkeren of af te breken. Met behulp van high-throughput sequencing en strikte statistische filters identificeerden ze 2.148 genen waarvan de activiteit veranderde in mutant-harten en 53 miRNAs die verhoogd of verlaagd waren vergeleken met gezonde muizen.
Wat er verandert in zieke hartcellen
Toen de onderzoekers de veranderde genen in biologische routes groeperen, kwamen verschillende thema’s naar voren. Veel van de veranderde genen waren gerelateerd aan hoe hartspiercellen samentrekken, hoe ze aan elkaar en aan hun omringende steunsubstantie hechten, hoe elektrische signalen door het hart reizen en hoe cellen vetten verwerken om energie te genereren. Deze bevindingen sluiten goed aan bij het klinische beeld van LMNA-gerelateerde ziekte: stijve, fibrotische weefsels; verstoorde elektrische geleiding die aritmieën bevordert; en verstoorde energiebalans. Padanalyses met behulp van gevestigde databases bevestigden verrijking in extracellular matrix-remodellering, spanningsafhankelijke ionkanalen, synaptische-achtige communicatie in het hart en vetzuurmetabolisme—wat suggereert dat de LMNA-mutatie meerdere onderling verbonden systemen verstoort in plaats van één enkel defect mechanisme.
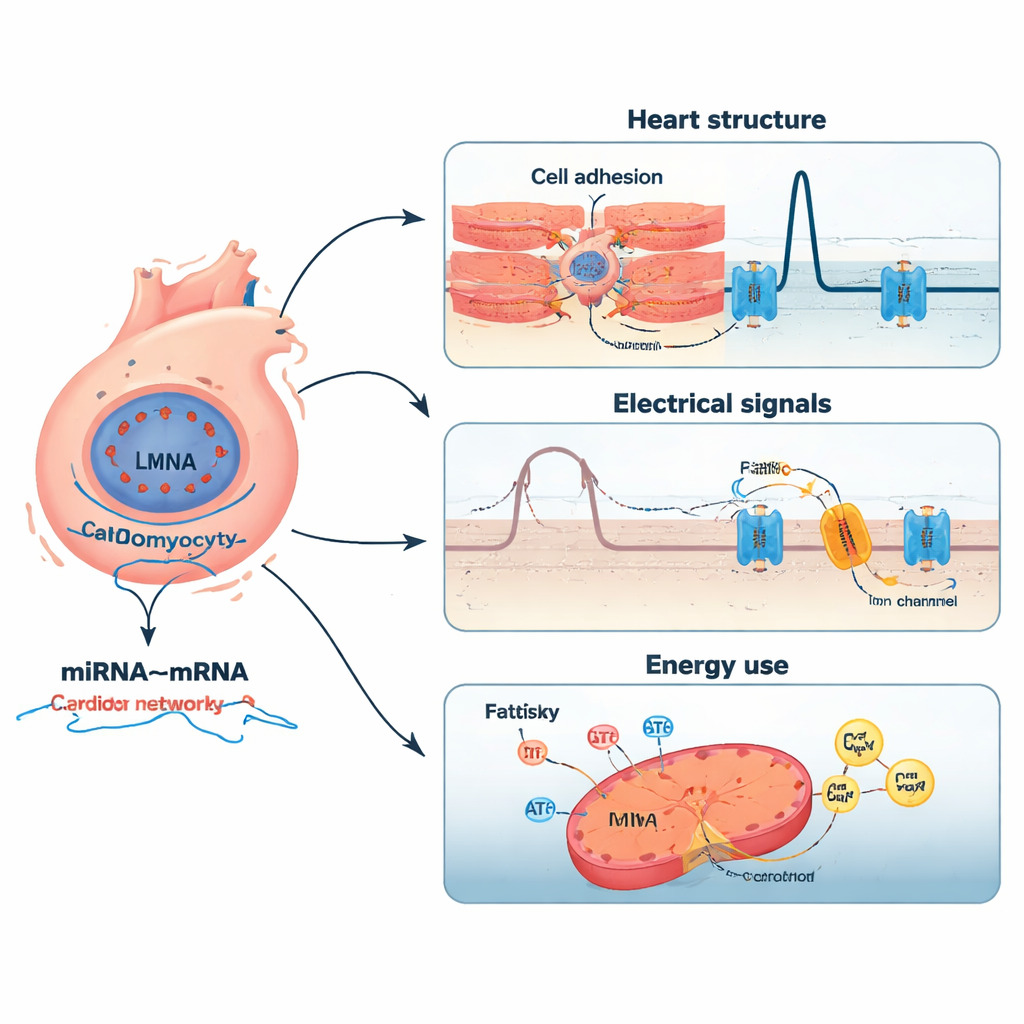
Netwerken van kleine schakelaars en hun doelwitten
De studie ging verder door miRNAs te koppelen aan hun waarschijnlijke mRNA-doelwitten. Met correlatieanalyses en kruiscontrole tegen grote databases van experimenteel geverifieerde interacties stelden de auteurs een netwerk met hoge betrouwbaarheid samen van 2.197 miRNA–mRNA-paren die 12 sleutel-miRNAs omvatten. Sommige miRNAs waren actiever en leken genen te dempen die essentieel zijn voor hartontwikkeling, calciumhuishouding en reacties op oxidatieve stress. Andere waren minder actief, waardoor mogelijk de rem op genen die betrokken zijn bij celadhesie, ontsteking en remodeling van het structurele skelet van het hart werd opgeheven. Bijvoorbeeld, één miRNA (miR-183-5p) werd gekoppeld aan een receptor in het Wnt-signaleringspad, dat cel-tot-celcommunicatie beïnvloedt, terwijl een andere (miR-3473a) verbonden was met een calcium-releasekanaal dat centraal staat in het hartritme. Samen schetsen deze netwerken hoe subtiele verschuivingen in kleine RNA-regelaars het effect van een LMNA-mutatie kunnen versterken.
Van moleculaire kaarten naar toekomstige therapieën
Voor niet-specialisten komt het erop neer dat deze studie een gedetailleerde kaart biedt van hoe een LMNA-mutatie de interne bedrading van het hart herschikt op het niveau van genregulatie. In plaats van één “slecht gen” weerspiegelt de ziekte een cascade van gewijzigde boodschappen—veel orchestrated door miRNAs—die hartstructuur, elektrische stabiliteit en energiegebruik beïnvloeden. Hoewel het werk in muizen is uitgevoerd en sterk leunt op computationele analyses, belicht het specifieke miRNA–gen-paren als veelbelovende kandidaten voor toekomstige bloedgebaseerde biomarkers of gerichte therapieën. Op de lange termijn kan het bijstellen van deze kleine RNA-schakelaars artsen helpen beter te voorspellen wie het grootste risico loopt, de ziekteprogressie preciezer te volgen en meer gepersonaliseerde behandelingen te ontwerpen voor families die getroffen zijn door LMNA-gerelateerde cardiomyopathie.
Bronvermelding: Córdoba-Caballero, J., Martínez, F.B., Campuzano, O. et al. An integrative approach to identify novel miRNA-mRNA interaction networks in LMNA-cardiomyopathy. Sci Rep 16, 6110 (2026). https://doi.org/10.1038/s41598-026-36439-9
Trefwoorden: gedilateerde cardiomyopathie, LMNA-gen, microRNA, genregulatie, hartfalen