Clear Sky Science · nl
Verhoogde cerebrale zuurstofextractie bij de ziekte van Parkinson correleert met de ernst van motorische stoornissen
Waarom energie in de hersenen ertoe doet bij Parkinson
De ziekte van Parkinson staat vooral bekend om zichtbare tekenen—tremor, stijfheid en vertraagde beweging—maar achter die symptomen gaat een hersenstelsel schuil dat moeite heeft zijn energiebehoefte te beheren. Deze studie onderzoekt hoe de hersenen van mensen met vroeg- tot middenstadium Parkinson zuurstof gebruiken, een belangrijke brandstof voor zenuwcellen. Door te kijken hoeveel zuurstof de hersenen uit het bloed halen, hopen de onderzoekers een niet-invasieve marker te vinden die de ernst van iemands bewegingsproblemen volgt, en meer inzicht te geven in wat er misgaat in de aangedane hersengebieden.
Binnenkijken in de werkende hersenen
Traditioneel hebben wetenschappers Parkinson bestudeerd door te meten hoe de hersenen suiker gebruiken of door radioactieve tracers te gebruiken om zuurstofgebruik te volgen. Deze methoden hebben aangetoond dat bepaalde diepe hersenstructuren die betrokken zijn bij beweging, zoals de basale ganglia, afwijkende activiteitspatronen laten zien bij Parkinson. Zuurstofgebruik zelf is echter moeilijker veilig en routinematig te meten omdat klassieke technieken kortlevende radioactieve stoffen en geavanceerde apparatuur vereisen. In dit werk vertrouwt het team in plaats daarvan op geavanceerde MRI-scans—technieken die al in veel ziekenhuizen beschikbaar zijn—om te schatten hoeveel zuurstof de hersenen uit het bloed halen, een grootheid die de zuurstofextractiefractie of OEF wordt genoemd. Een hogere OEF betekent dat hersenweefsel meer zuurstof uit dezelfde bloedtoevoer opneemt.
Hoe de studie is uitgevoerd
De onderzoekers onderzochten 50 mensen met de ziekte van Parkinson en 30 gezonde vrijwilligers. Alle deelnemers ondergingen een gespecialiseerde MRI-scan waarmee het team kaarten van OEF over de hele hersenen kon maken. De wetenschappers richtten zich met name op de basale ganglia—gebieden zoals de substantia nigra, nucleus ruber, globus pallidus, putamen en nucleus caudatus—die centraal staan in de bewegingsturing en waarvan bekend is dat ze bij Parkinson verstoord zijn. Ze bestudeerden ook het witte stof, de bekabeling van de hersenen die verschillende regio’s met elkaar verbindt. Voor patiënten werden standaard klinische scores van bewegingsproblemen en ziektegraad verzameld, zodat hersenmetingen direct vergeleken konden worden met de ernst van de symptomen.
Waar zuurstofgebruik verhoogd is bij Parkinson
De MRI-kaarten toonden aan dat mensen met Parkinson gemiddeld ongeveer 8 procent hogere OEF hadden in sleutelregio’s voor beweging vergeleken met gezonde vrijwilligers. Deze verhoging was het duidelijkst zichtbaar in de substantia nigra, nucleus ruber, globus pallidus en putamen, met iets zwakkere maar nog steeds betekenisvolle veranderingen in de nucleus caudatus en het witte stof. Met andere woorden: de diepe knooppunten die helpen bij het coördineren van vloeiende bewegingen leken harder te werken—of in elk geval meer zuurstof uit het bloed te halen—dan bij mensen zonder de ziekte. Wanneer het team de hersenen per zeer klein volume over het hele hoofd bekeek, zagen zij wijdverspreide plekken waar de OEF was verhoogd, vooral in het diepe grijze stof en het omliggende weefsel.
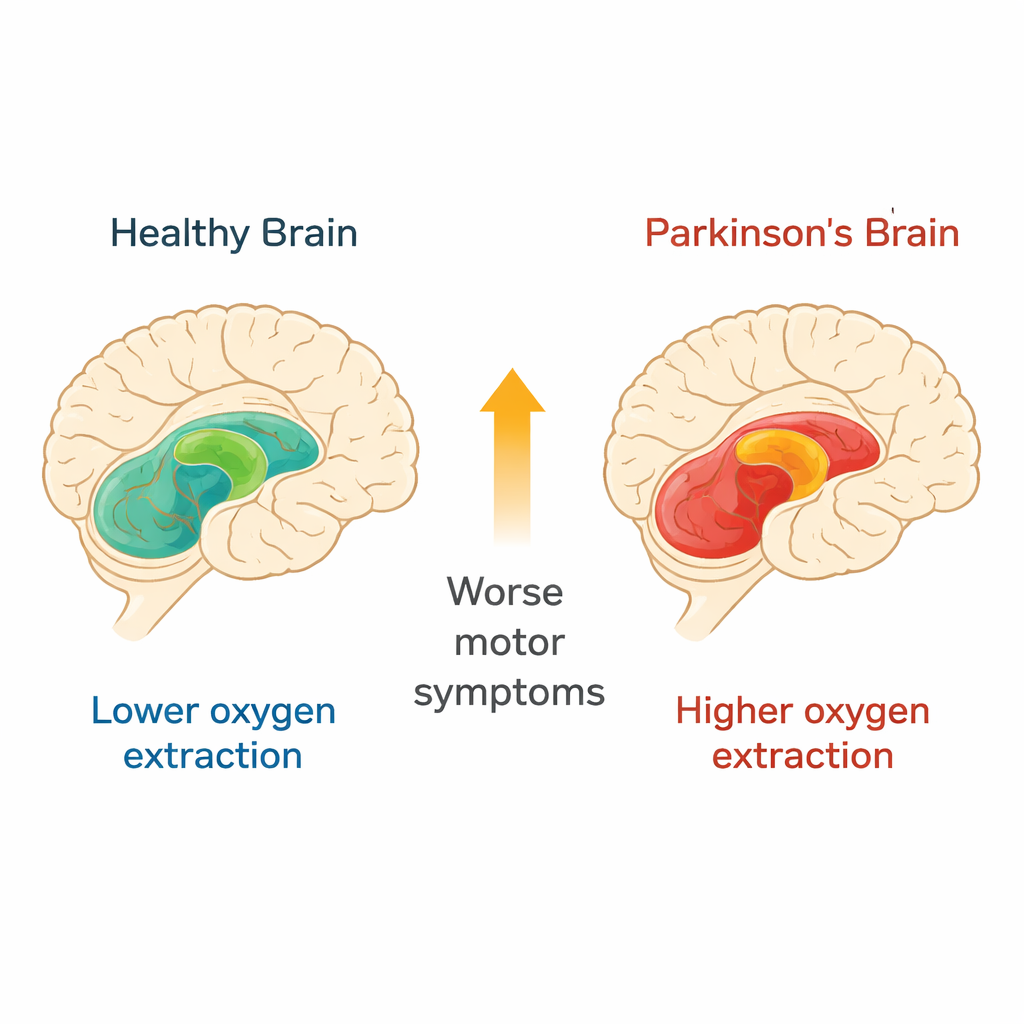
Het koppelen van hersenzuurstofgebruik aan bewegingsproblemen
Verder dan eenvoudige groepsverschillen volgden OEF-niveaus de mate van functiebeperking bij patiënten. Een hogere OEF in de substantia nigra, nucleus ruber, globus pallidus en in het witte stof hing samen met slechtere scores op een standaard beoordelingsschaal voor beweging. Voor elke toename van 10 punten in de motorische symptoomscore steeg de OEF in deze regio’s met ongeveer 1,6 procent. Dit patroon bleef bestaan nadat er rekening was gehouden met leeftijd, en het weerspiegelde eerdere bevindingen dat de bloedstroom naar dezelfde structuren ook toeneemt naarmate de symptomen verergeren. Gezamenlijk suggereren deze resultaten dat de aangetaste circuits zich in een staat van metabole belasting bevinden—ofwel compenseren voor verloren zenuwcellen door harder te werken, ofwel weerspiegelen ze veranderingen in hoe de bloedvaten deze gebieden van bloed voorzien.
Wat dit betekent voor patiënten en de toekomst
De studie laat zien dat een relatief eenvoudige MRI-gebaseerde maat—hoeveel zuurstof de hersenen uit het bloed halen—in de diepe bewegingscentra toeneemt bij mensen met vroeg- tot middenstadium Parkinson en toeneemt met de ernst van hun motorische symptomen. Hoewel OEF op zichzelf niet nauwkeurig genoeg is om Parkinson individueel te diagnosticeren, biedt het een veelbelovende inkijk in hoe de ziekte het energiegebruik van de hersenen verstoort. Met verdere verfijning, en door het te combineren met andere metingen zoals bloedstroom en structurele veranderingen, zou OEF-mapping een hulpmiddel kunnen worden om ziekteprogressie te volgen, nieuwe behandelingen te testen en beter te begrijpen waarom hersencellen bij Parkinson zo kwetsbaar worden.
Bronvermelding: Candan, H.E., Lee, D., Lee, H. et al. Elevated cerebral oxygen extraction fraction in Parkinson’s disease correlates with motor impairment severity. Sci Rep 16, 5673 (2026). https://doi.org/10.1038/s41598-026-36435-z
Trefwoorden: Ziekte van Parkinson, hersen zuurstofgebruik, MRI-biomarkers, motorische symptomen, basaal ganglia