Clear Sky Science · nl
Urinefragmenten van complement C3 en hun klinische relevantie bij MPO‑ANCA‑geassocieerde vasculitis
Waarom urine verborgen ontsteking kan onthullen
Artsen die bepaalde auto‑immuunziekten van de bloedvaten behandelen staan voor een grote uitdaging: ze moeten weten wanneer de ziekte in de nieren opvlamt, maar de duidelijkste tests vereisen vaak een naaldbiopsie. Deze studie stelt een ogenschijnlijk simpele vraag met grote gevolgen voor patiënten: kan een gewone urinemonster in real time laten zien hoeveel schadelijke immuunactiviteit in de nieren smeult bij mensen met MPO‑ANCA‑geassocieerde vasculitis?
Een stille maar ernstige aanval op kleine bloedvaten
ANCA‑geassocieerde vasculitis is een zeldzame auto‑immuunziekte waarbij het eigen afweersysteem per ongeluk kleine bloedvaten door het hele lichaam aanvalt, met name in de nieren. Veel patiënten ontwikkelen nierontsteking die deze organen stilletjes kan beschadigen totdat de functie ernstig verslechtert. Traditioneel werd deze nierschade als “pauci‑immuun” bestempeld, wat betekent dat er onder de microscoop weinig immuunafzettingen worden gezien. De afgelopen tien jaar hebben wetenschappers echter ingezien dat een krachtige immuuncascade, het complementsysteem, en dan vooral de alternatieve route, een cruciale rol speelt bij het veroorzaken van deze schade. De vraag is hoe dat proces te monitoren zonder herhaaldelijk nierweefsel te moeten afnemen.
Het volgen van immuunvoetafdrukken in urine
Het complementsysteem werkt een beetje als een rijvallende dominostenen: eenmaal geactiveerd worden grotere componenten in kleinere fragmenten geknipt die helpen immuuncellen te lokken en aan te sturen. Een van de centrale spelers is een eiwit dat C3 heet. Wanneer C3 wordt gesplitst, ontstaan een reeks fragmenten – C3a, C3b, iC3b, C3c en C3d – die als boodschappers en als merkers van activiteit fungeren. De onderzoekers redeneerden dat als de nieren een belangrijke plek zijn van deze immuunreactie, sommige van deze C3‑fragmenten in de urine terecht zouden kunnen komen en als een “vloeibare biopsie” van nierontsteking zouden kunnen dienen. Om dit te testen verzamelden zij eenmalige urinemonsters van 22 patiënten met myeloperoxidase (MPO)‑ANCA‑vasculitis en van 20 gezonde leeftijdsgenoten, en gebruikten gevoelige labtests om de niveaus van elk C3‑fragment te meten. De resultaten werden gecorrigeerd voor urineconcentratie door vergelijking met creatinine, een afvalproduct dat normaal door de nieren wordt uitgescheiden.
Duidelijke verschillen tussen patiënten en gezonde vrijwilligers
Het contrast tussen patiënten en gezonde vrijwilligers was opvallend. Elk gemeten C3‑fragment in urine — C3a, C3b, iC3b, C3c en C3d — was aanzienlijk hoger bij mensen met vasculitis, zelfs na correctie voor verschillen in urineconcentratie. Binnen de patiëntengroep correleerden hogere fragmentniveaus sterk met verschillende tekenen van actieve ziekte. Ze stegen samen met de Birmingham Vasculitis Activity Score, een gestandaardiseerde klinische schaal die symptomen en orgaanbetrokkenheid vastlegt, en met twee belangrijke urinevondsten: eiwit in de urine en bloed in de urine. In statistische modellen die meerdere factoren tegelijk in rekening brachten bleef de algehele ziekteactiviteit de sterkste onafhankelijke voorspeller van fragmentniveaus, en eiwitverlies uit de nieren droeg voor de meeste fragmenten aanvullend bij. Opvallend was dat deze immuunmarkers niet samenhingen met serumcreatinine, een veelgebruikte bloedtest voor nierfiltratie, wat suggereert dat ze lokale immuunactiviteit detecteren en niet alleen verlies van nierfunctie.
Wat deze bevindingen zeggen over immuunactiviteit in de nieren
Het patroon dat in de studie werd waargenomen ondersteunt het idee dat complementactivatie bij deze ziekte in de nier plaatsvindt en niet louter uit het bloed wordt gefilterd. Er is bewijs dat niercellen complementeiwitten kunnen produceren, en wanneer de kleine vaten ontstoken zijn, kan meer C3 ter plaatse in actieve fragmenten worden gesplitst. Die fragmenten kunnen vervolgens in de urine verschijnen en bieden daarmee een venster op de lopende immuunaanval. Eén fragment, iC3b, was bijzonder interessant: het weerspiegelde sterk de algemene ziekteactiviteit maar steeg en daalde niet in samenhang met de hoeveelheid eiwit in de urine, wat suggereert dat het mogelijk nauwer verbonden is met immuunsignaleringsmechanismen dan met structureel lekkage van de filtratiebarrière.
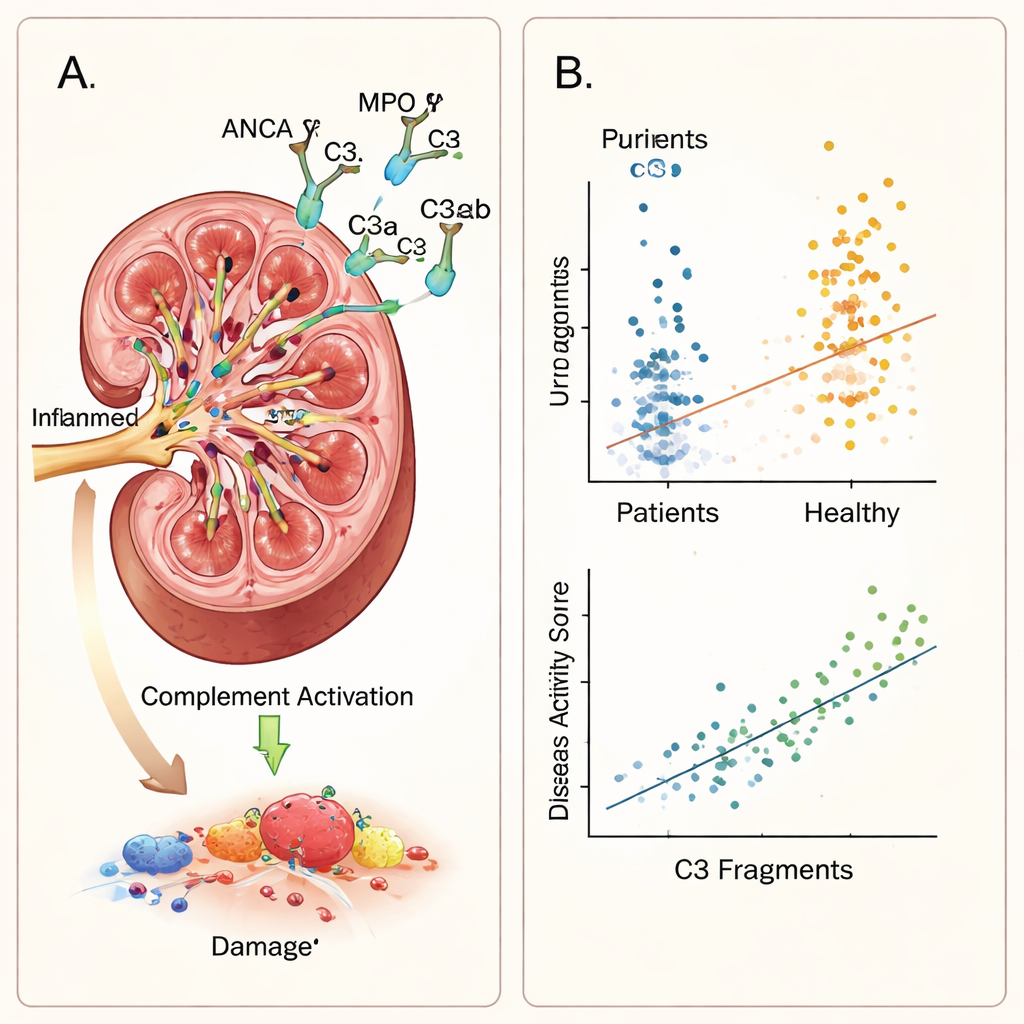
Van naaldbiopsies naar “vloeibare biopsies”?
De studie kent belangrijke beperkingen: zij werd uitgevoerd in één ziekenhuis, omvatte slechts 22 patiënten en hield elke persoon op één tijdstip vast. Niet alle deelnemers ondergingen nierbiopten, wat gedetailleerde vergelijkingen met weefselbevindingen beperkt. Toch levert het werk overtuigend vroeg bewijs dat een eenvoudige urinetest voor complement C3‑fragmenten kan weerspiegelen hoe actief MPO‑ANCA‑vasculitis in de nieren is, onafhankelijk van traditionele nierfunctietests. Voor patiënten en clinici roept dit de mogelijkheid op dat in de toekomst zorgvuldig ontworpen urinetests kunnen helpen bij het volgen van opvlammingen, het sturen van behandelintensiteit en mogelijk bij de evaluatie van nieuwe geneesmiddelen die het complementsysteem doelgericht remmen — met veel minder afhankelijkheid van invasieve procedures.
Bronvermelding: Hu, Y., Shi, M., Huang, Q. et al. Urinary complement C3 fragment levels and their clinical relevance in MPO-ANCA-associated vasculitis. Sci Rep 16, 5643 (2026). https://doi.org/10.1038/s41598-026-36417-1
Trefwoorden: vasculitis, auto-immuun nierziekte, complementsysteem, urine-biomarkers, ANCA