Clear Sky Science · nl
Van in-silico QSAR-modellering tot in-vitro MTT-assay: experimentele validatie van nieuwe uPAR-leads voor triple-negatieve borstkanker (TNBC) en huidkanker
Waarom dit onderzoek ertoe doet
Kankers zoals triple‑negatieve borstkanker en bepaalde vormen van huidkanker zijn berucht moeilijk te behandelen omdat ze snel uitzaaien en vaak resistent zijn tegen standaardtherapieën. Deze studie onderzoekt een veelbelovend nieuw doelmolecuul aan het oppervlak van kankercellen — uPAR — en laat zien hoe de combinatie van computergebaseerd geneesmiddelenontwerp en laboratoriumexperimenten nieuwe kandidaat-geneesmiddelen kan opleveren die de verspreiding van deze agressieve tumoren mogelijk kunnen vertragen of stoppen.
Een poort die helpt bij de verspreiding van kanker
Om een tumor dodelijk te laten worden, moeten de cellen zich losmaken van hun oorspronkelijke locatie, het omliggende weefsel afbreken, in de bloedbaan komen en zich in verre organen vestigen. uPAR speelt een sleutelrol in dit proces. Het zit op het celoppervlak van kankercellen en werkt samen met partnerproteïnen om enzymen te activeren die de omliggende steunstructuur oplossen, waardoor cellen gemakkelijker kunnen bewegen en binnendringen. uPAR komt in bijzonder hoge concentraties voor in triple‑negatieve borstkankercellen en in bepaalde huidkankercellen, en de hoeveelheden ervan worden in verband gebracht met snellere groei, grotere invasiviteit en slechtere patiëntuitkomsten. Daardoor is uPAR een aantrekkelijk — maar tot nu toe onderbenut — doelwit voor antikankermiddelen.
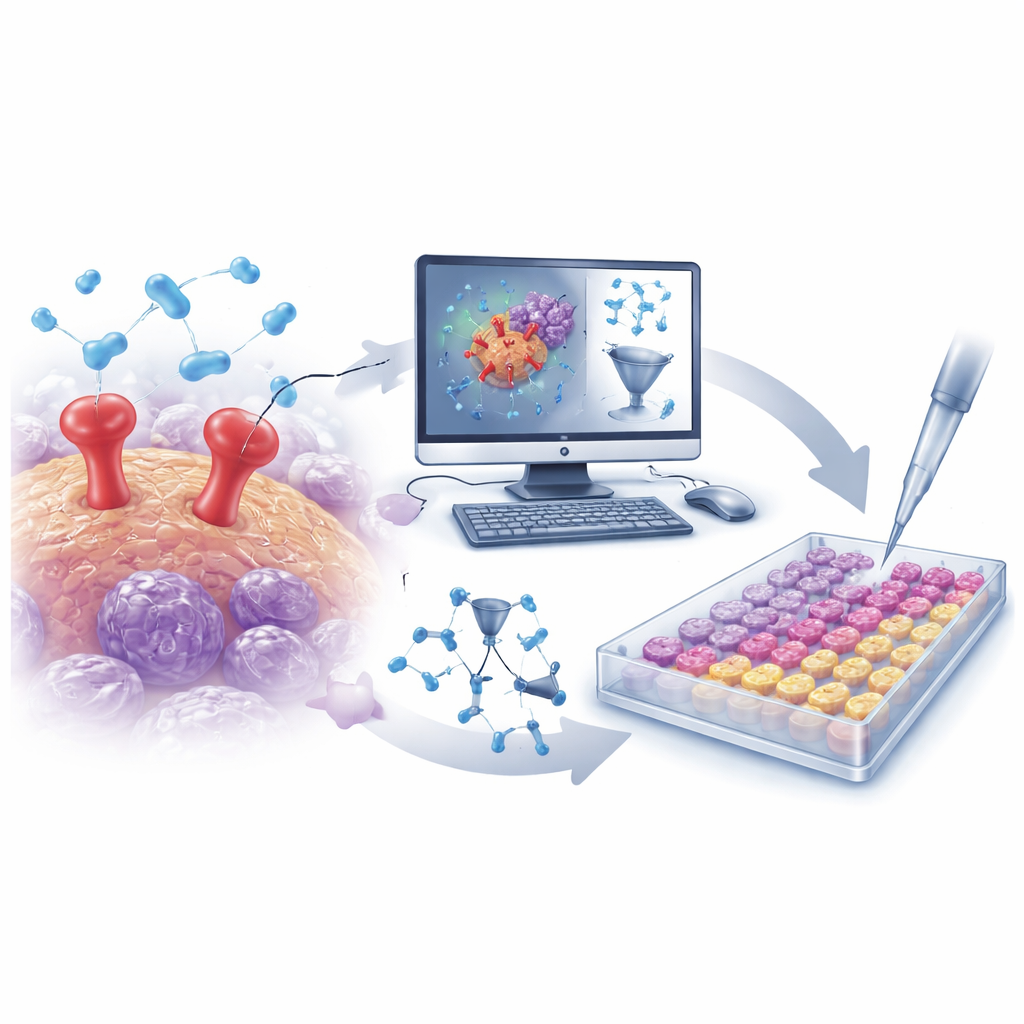
Grote chemische datasets doorzoeken met slimme algoritmen
De onderzoekers begonnen met het samenstellen van een grote verzameling van meer dan 500 bekende uPAR‑blokkerende moleculen uit een publieke database. De structuur van elk molecuul werd omgezet in duizenden numerieke descriptoren die eigenschappen vastleggen zoals grootte, vorm, ladingsverdeling en flexibiliteit. Met deze data bouwde het team een QSAR-model (quantitative structure–activity relationship) — een wiskundig hulpmiddel dat leert welke structurele kenmerken er doorgaans voor zorgen dat een molecuul een sterkere uPAR-remmer wordt. Na zorgvuldige validatie om overfitting te vermijden, toonde het model een hoge voorspellende waarde op onbekende verbindingen en bracht het verschillende sleutelkenmerken in kaart die uPAR-blokkering versterken of verzwakken. Deze inzichten begeleidden de zoektocht naar nieuwe, beter ontworpen moleculen.
Van virtuele screens naar echte reageerbuizen
Gewapend met het getrainde QSAR-model screende het team in silico een gerichte bibliotheek van ongeveer 30.000 proteaserichte moleculen. Het model beperkte deze enorme verzameling snel tot een kleine set waarschijnlijke uPAR-remmers. Tegelijkertijd werden computerdocking-simulaties gebruikt om te bekijken hoe goed elk kandidaat mogelijk in de uPAR-bindingsplaats zou passen, en moleculaire dynamicasimulaties testten of deze gedockte complexen over tijd stabiel zouden blijven. Uit deze gecombineerde in-silico campagne kwamen twee opvallende moleculen naar voren: D685‑0061, door het QSAR-model aangeduid als zeer potent, en C878‑1660, door docking en simulatie gemarkeerd als het vormen van bijzonder stabiele interacties met uPAR.
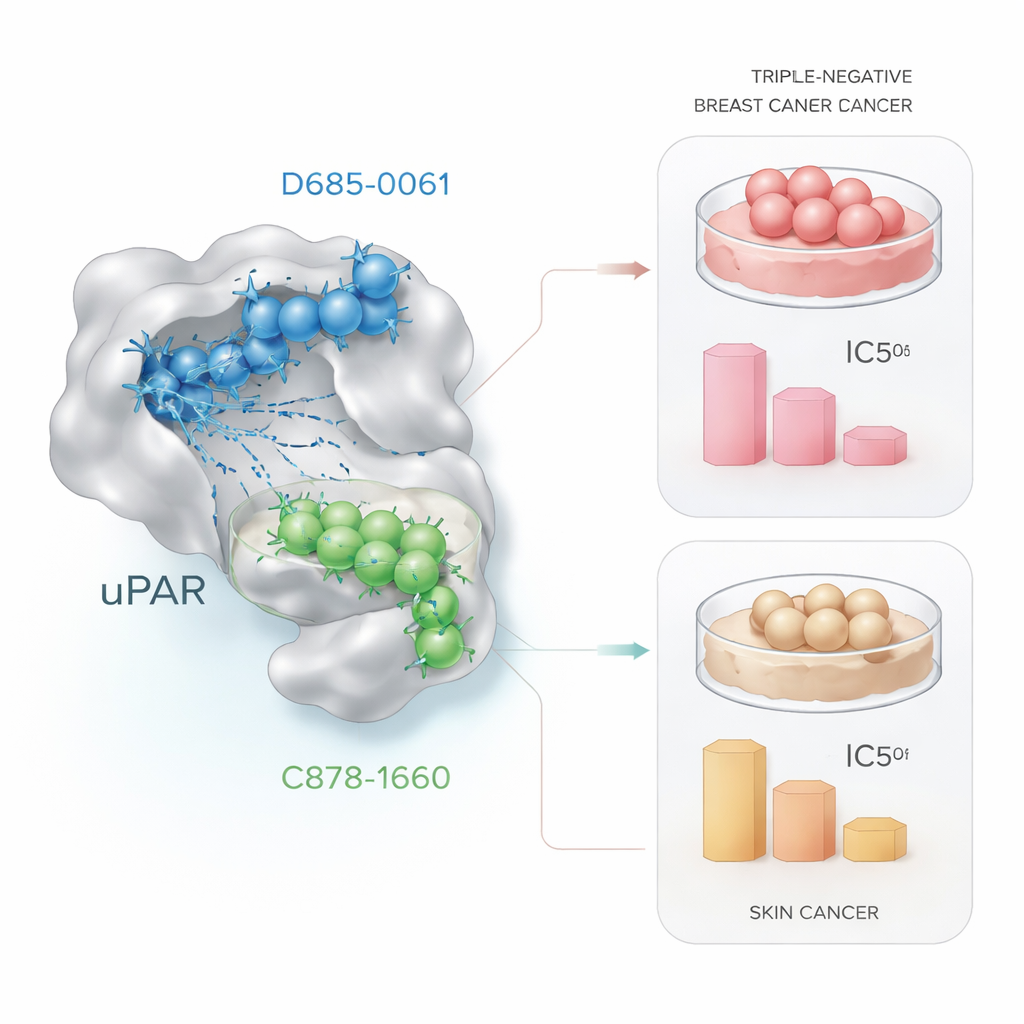
De kandidaten testen in kankercellen
Computationale veelbelovende resultaten zijn alleen relevant als ze zich vertalen naar echte biologische effecten. Om dit te testen, brachten de onderzoekers levende kankercellen in contact met oplopende doses van de twee lead-moleculen en bepaalden ze de celoverleving met een standaard laboratoriummethode genaamd de MTT-assay. In triple‑negatieve borstkankercellen (MDA‑MB‑231) doodde D685‑0061 cellen efficiënter en halveerde het de levensvatbaarheid rond 21 micromol, terwijl C878‑1660 ongeveer vier keer die hoeveelheid nodig had. Onder de microscoop vertoonden cellen die met D685‑0061 waren behandeld duidelijke tekenen van geprogrammeerde celdood, zoals ronding, loslating van het oppervlak en fragmentatie. In tegenstelling daarmee was in huidkankercellen (A431) C878‑1660 de sterkere doder, met ongeveer 50% celdood rond 19 micromol vergeleken met circa 28 micromol voor D685‑0061, wederom met zichtbaar dosisafhankelijk beschadiging.
Wat dit betekent voor toekomstige kankerbehandelingen
Dit werk levert geen direct nieuw geneesmiddel op, maar wel twee veelbelovende uitgangspunten en, even belangrijk, een krachtig stappenplan om er meer te vinden. Door big-data‑modellering, 3D-simulaties en zorgvuldige celgebaseerde experimenten te koppelen, laat de studie zien dat uPAR selectief kan worden gericht met kleine moleculen die agressieve borst- en huidkankercellen beschadigen. D685‑0061 en C878‑1660 dienen nu als leadverbindingen die scheikundigen kunnen verfijnen om potentie te verhogen, veiligheid te verbeteren en farmacokinetische eigenschappen te optimaliseren. Op de lange termijn zouden geneesmiddelen die op deze aanpak zijn gebaseerd de verspreiding van uPAR‑gedreven kankers kunnen blokkeren en sommige van de huidige meest gevaarlijke tumoren beter hanteerbaar kunnen maken.
Bronvermelding: Badukle, H., Jawarkar, R.D., Shah, U. et al. From in-silico QSAR modeling to in-vitro MTT assay: experimental validation of novel uPAR leads for triple-negative breast cancer (TNBC) and skin cancer. Sci Rep 16, 5786 (2026). https://doi.org/10.1038/s41598-026-36406-4
Trefwoorden: uPAR-remmers, triple-negatieve borstkanker, huidkanker, computerondersteunde geneesmiddelenontdekking, MTT-celviabiliteitsassay