Clear Sky Science · nl
Een studie met dichtheidsfunctionaaltheorie van de adsorptie van cyclofosfamide en purinethol op een covalent triazine‑framework (CTF-2) voor geneesmiddelbezorgingstoepassingen
Waarom slimere chemotherapie ertoe doet
Chemotherapie redt levens, maar werkt vaak als een zoeklicht in plaats van een spotlight—gezonde cellen worden mee aangevallen naast de kankercellen. Dat kan leiden tot ernstige bijwerkingen, van vermoeidheid en infecties tot orgaanschade. De hier besproken studie onderzoekt een ultradun, zeer poreus materiaal genaamd covalent triazine‑framework (CTF-2) als een “slimme spons” die twee al lang gebruikte antikankermiddelen—cyclofosfamide en purinethol—veiliger en efficiënter naar de plaats van bestemming kan vervoeren en ze vervolgens onder tumorachtige omstandigheden kan loslaten.
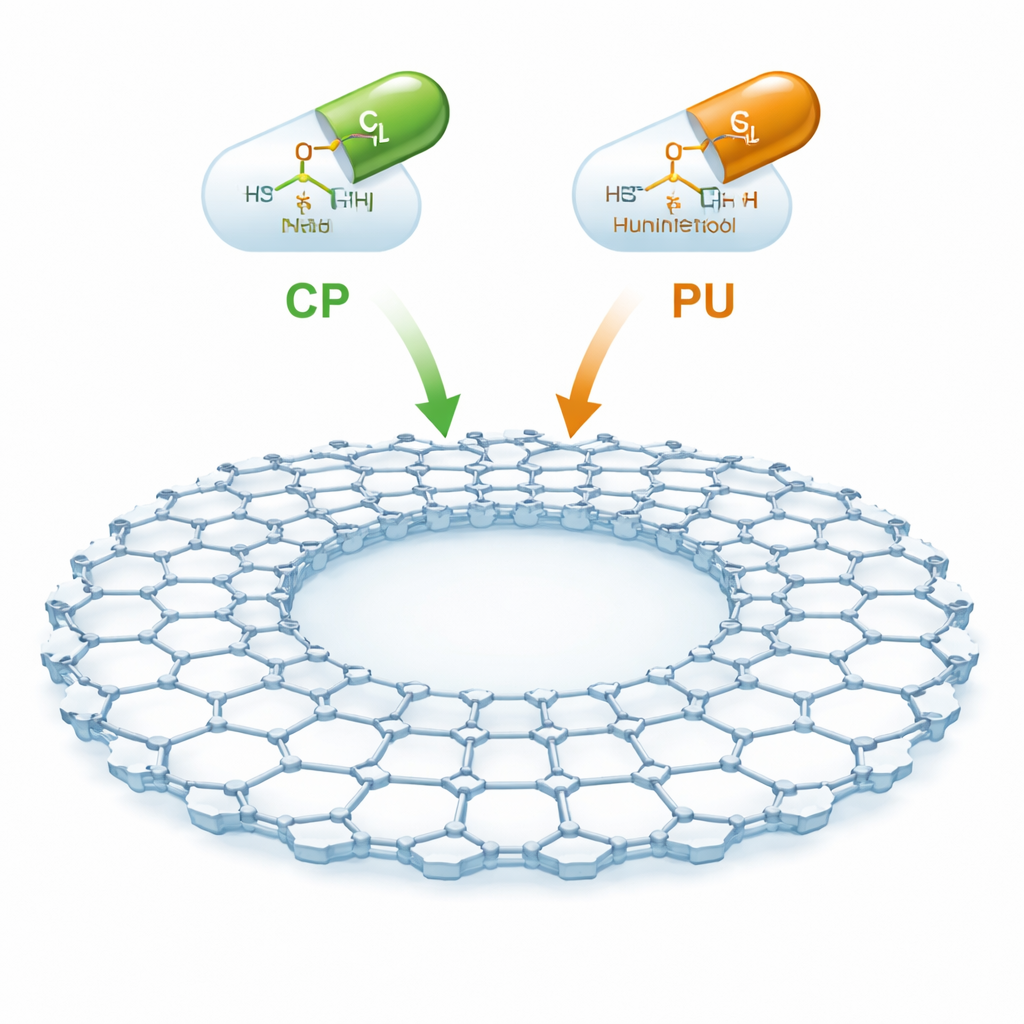
Een nieuw soort moleculaire spons
CTF-2 is een synthetisch materiaal opgebouwd uit ringen van koolstof en stikstof die verbonden zijn tot een vlak, velachtig netwerk met een grote centrale holte en veel open ruimte. Omdat het dun, stabiel en poreus is, biedt het een enorm interne oppervlak om geneesmiddelmoleculen vast te houden. De auteurs richtten zich op twee belangrijke kankergeneesmiddelen: cyclofosfamide, veel gebruikt bij bloedkankers en solide tumoren, en purinethol (ook wel mercaptopurine genoemd), toegepast bij leukemieën en sommige ontstekingsdarmziekten. Het idee is deze middelen zachtjes op het CTF-2‑oppervlak te laten docken zodat ze via de bloedbaan vervoerd kunnen worden en selectiever worden vrijgegeven, waardoor schade aan gezond weefsel vermindert.
Het onzichtbare onderzoeken met computerexperimenten
In plaats van in een nat laboratorium te werken, gebruikte het team geavanceerde kwantumniveau‑berekeningen (dichtheidsfunctionaaltheorie en gerelateerde methoden) om te onderzoeken hoe sterk elk geneesmiddel aan CTF-2 zou kleven en wat de complexen bijeenhoudt. Ze optimaliseerden de vormen van CTF-2 plus elk geneesmiddel, maten de afstanden tussen de atomen waar ze contact maken, en berekenden hoeveel energie vrijkomt wanneer een geneesmiddel aan het raamwerk hecht. Voor cyclofosfamide werd een berekende adsorptie‑energie van ongeveer −1,04 elektronvolt gevonden, iets sterker dan de −0,82 elektronvolt voor purinethol. Deze waarden, die gunstig blijven zelfs na correctie voor technische artefacten en na simulatie van water als oplosmiddel, duiden erop dat beide middelen sterk genoeg binden om geladen te worden maar niet zo stevig dat ze later niet vrijgegeven kunnen worden.
Zachte krachten die belangrijk werk verrichten
De studie toont aan dat de “lijm” tussen geneesmiddelen en CTF-2 geen harde covalente binding is, maar een web van zachte, niet‑covalente krachten. Met gespecialiseerde analyses van elektronendichtheid—in wezen kaarten van waar de gedeelde elektronen zich bevinden—vonden de onderzoekers dat van der Waals‑aantrekkingen (dezelfde zwakke krachten die gekko’s laten klimmen) en milde elektrostatische interacties dominant zijn. Deze interacties vinden plaats op korte maar niet‑bindende afstanden tussen waterstof-, stikstof-, zuurstof-, zwavel‑ en koolstofatomen van de geneesmiddelen en van het raamwerk. Aanvullende berekeningen die de totale aantrekkingskracht in verschillende componenten splitsen bevestigden dat elektrostatische en dispersie‑ (van der Waals‑) krachten het grootste deel van de stabiliserende aantrekking leveren, terwijl afstotende krachten voorkomen dat het geneesmiddel te diep indringt of irreversibel bindt.
Signaleren van stabiele lading en instelbare vrijgave
Het team onderzocht ook hoe elektronen verschuiven wanneer de geneesmiddelen op CTF-2 rusten en hoe dit de basiselektrische eigenschappen verandert. Ze observeerden kleine maar duidelijke ladingsoverdrachten tussen elk geneesmiddel en het raamwerk en een lichte vernauwing van de energiebandgap die gevulde en lege elektronische toestanden scheidt. Dit impliceert dat de reactiviteit en geleiding van het materiaal subtiel worden bijgesteld bij belading, een nuttige eigenschap voor eventuele toekomstige sensor‑ of theranostische toepassingen. Cruciaal is dat, wanneer ze de zuurdere omgeving nabij tumoren nabootsten door extra protonen toe te voegen, de berekende binding verzwakte en de contactafstanden toenamen. In eenvoudige bewoordingen suggereren de simulaties dat CTF-2 de geneesmiddelen onder normale bloedachtige omstandigheden kan vasthouden, maar ze in tumorachtige, zure omgevingen eerder zal loslaten—precies het gewenste gedrag voor gerichte toediening.
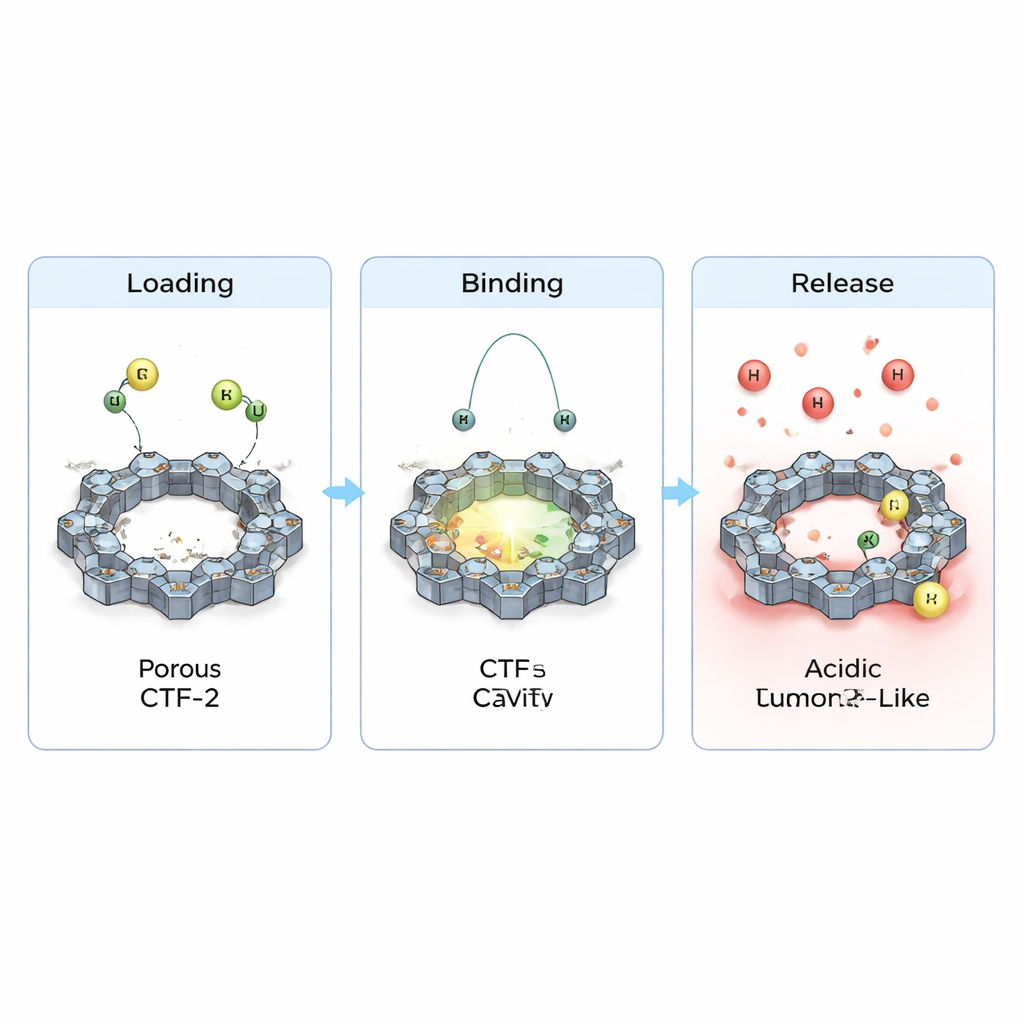
Wat dit betekent voor toekomstige kankerbehandelingen
Samengevoegd schetsen deze berekeningen CTF-2 als een veelbelovende drager voor cyclofosfamide en purinethol: het kan ze op zijn poreuze oppervlak stabiel opslaan, beschermen tijdens circulatie en vervolgens vrijgeven wanneer de lokale chemie rondom een tumor verandert. Hoewel het werk theoretisch is en experimentele bevestiging nodig zal hebben, suggereert het dat fijn ontworpen, stikstofrijke raamwerken zoals CTF-2 kunnen helpen om oude maar effectieve chemotherapeutica om te vormen tot slimmer medicijngebruik—krachtige doses afleveren waar ze het meest nodig zijn en tegelijk de collaterale schade aan gezonde cellen verminderen.
Bronvermelding: Tariq, T., Yar, M., Bayach, I. et al. A density functional theory study of cyclophosphamide and purinethol adsorption on a covalent triazine framework (CTF-2) for drug delivery applications. Sci Rep 16, 6125 (2026). https://doi.org/10.1038/s41598-026-36405-5
Trefwoorden: nanodrager, geneesmiddelbezorging, kankerchemotherapie, covalent triazine‑framework, computationele modellering