Clear Sky Science · nl
Een interactieve cascaderende deep learning‑oplossing met deskundige verfijning voor nauwkeurige segmentatie van striatale subregio’s
Waarom het in kaart brengen van kleine hersengebieden ertoe doet
Het striatum, een kleine structuur diep in de hersenen, speelt een centrale rol bij beweging en motivatie en wordt sterk aangetast bij aandoeningen zoals de ziekte van Parkinson. Artsen gebruiken vaak PET‑ en MRI‑scans om chemische veranderingen in dit gebied te meten, maar het striatum bestaat uit vele kleine subregio’s die moeilijk zichtbaar te maken en precies af te bakenen zijn. Dit artikel introduceert een nieuwe computerondersteunde methode, StriaSeg‑iARM genoemd, die specialisten helpt deze grenzen nauwkeuriger en efficiënter te tekenen, zelfs bij mensen wiens hersenen door veroudering of ziekte veranderd zijn.
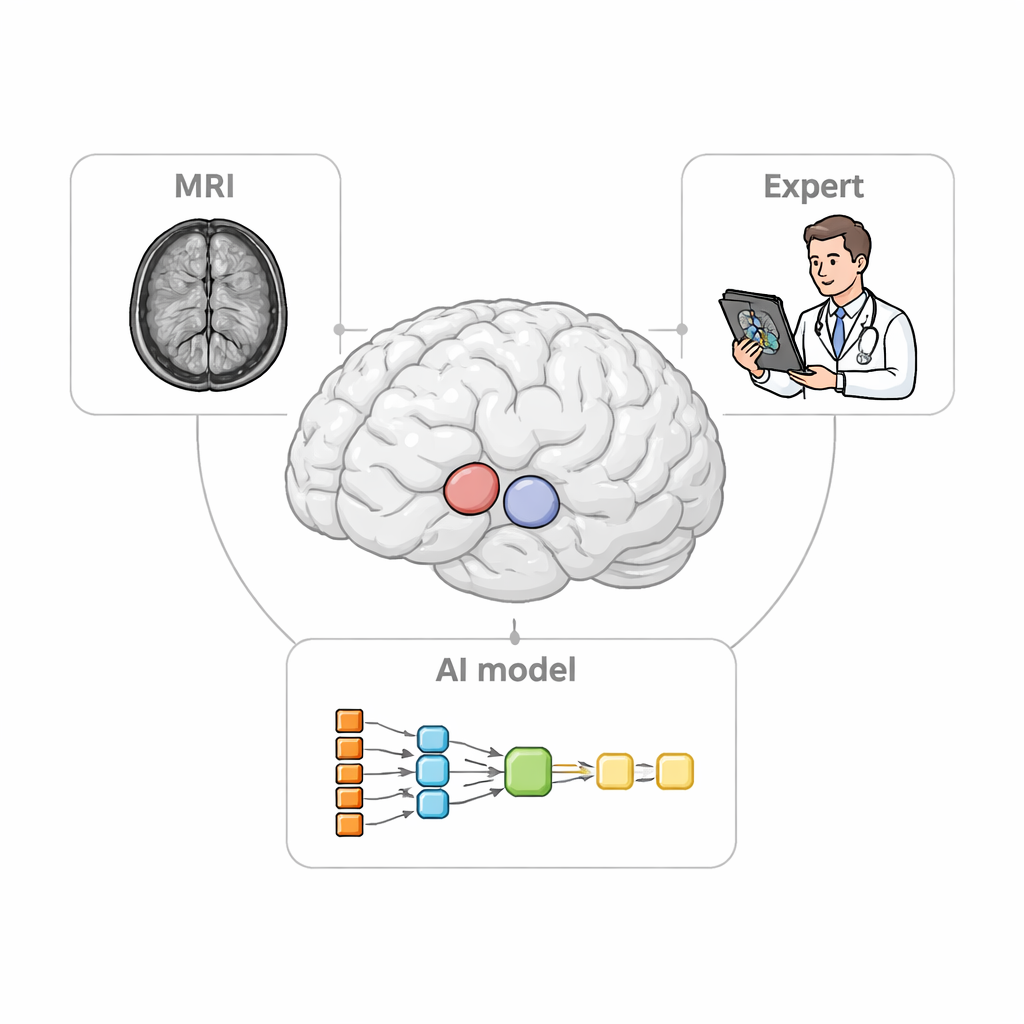
Het klinische probleem in het volle zicht
Wanneer neurologen aandoeningen als de ziekte van Parkinson beoordelen, vertrouwen ze op PET‑scans om te volgen hoe dopaminerelateerde signalen variëren tussen verschillende delen van het striatum. Om dit correct te doen moeten ze eerst kleine driedimensionale “regionen van belang” op MRI definiëren, die als meetbekers voor de PET‑gegevens dienen. Het handmatig omlijnen van deze regio’s is traag en eentonig werk en kan tussen experts uiteenlopen. Bestaande software lokaliseert vaak alleen de grotere structuren en heeft moeite bij patiënten met verschrompelde of vervormde hersenen, een veelvoorkomend beeld bij gevorderde neurodegeneratieve ziekten. Deze tekortkomingen kunnen het werkelijke beschadigingspatroon vervagen en de diagnostische waarde van beeldvorming verminderen.
Een slimmer hulpmiddel in twee stappen
De onderzoekers ontwierpen StriaSeg‑iARM als een tweefasig deep learning‑systeem dat direct in de individuele hersenruimte werkt in plaats van de scan naar een standaardtemplate te dwingen. In de eerste fase vindt het programma het algemene striatum op een driedimensionale MRI. In de tweede fase verdeelt het deze structuur in 12 anatomisch gedefinieerde subregio’s aan beide zijden van de hersenen. Tussen deze twee fasen zit de belangrijkste innovatie: een interactieve stap waarin een expert snel het ruwe omlijnde resultaat van de eerste fase kan controleren en, indien nodig, corrigeren voordat de fijnere onderverdeling wordt uitgevoerd. Deze aanpak combineert de snelheid van automatisering met het beoordelingsvermogen van een getrainde waarnemer.
Getraind en getest in echte hersenen
Om het systeem te leren wat het moest zoeken, verzamelde het team honderden MRI‑scans van meerdere ziekenhuizen en scantypes, en maakte nauwkeurige handmatige omlijningen van de 12 striatale subregio’s. Ze testten het model vervolgens op twee externe datasets die zowel MRI als dopaminerelateerde PET‑scans bevatten: één van relatief vroege Parkinson‑patiënten en gezonde vrijwilligers, en een andere van een oudere, ernstiger getroffen klinische groep met duidelijke hersenatrofie en gemengde diagnoses. In deze uitdagende gevallen benaderde StriaSeg‑iARM consequent de handmatige expertomlijningen beter dan traditionele atlasgebaseerde methoden en een eenvoudiger eendaagse deep learning‑model, met grotere overlap, nauwkeurigere grenzen en stabiele volumemetingen.
Scherpere metingen voor chemische hersenscans
Aangezien het uiteindelijke doel is om PET‑signalen te kwantificeren, onderzochten de auteurs ook hoe verschillende segmentatiemethoden PET‑uitkomsten beïnvloedden. Met behulp van een standaardscore voor tracerbinding in elke subregio vergeleken ze automatische resultaten met die op basis van handmatige omlijningen. De atlasmethode neigde ertoe de binding te onderschatten, vooral bij patiënten met ernstigere afwijkingen, terwijl het basale deep learning‑model nog steeds merkbare vertekening in sommige regio’s liet zien. Daarentegen produceerden de cascaderende modellen — vooral wanneer de interactieve correctiestap werd gebruikt — PET‑waarden die nauw volgden wat de experts aangaven, met minimale bias en spreiding. Het team liet verder zien dat een eenvoudige onzekerheidsscore uit de eerste fase ongeveer een kwart van de moeilijkste gevallen kan signaleren waarin deskundige verfijning echt nodig is, terwijl de rest volledig automatisch kan blijven.
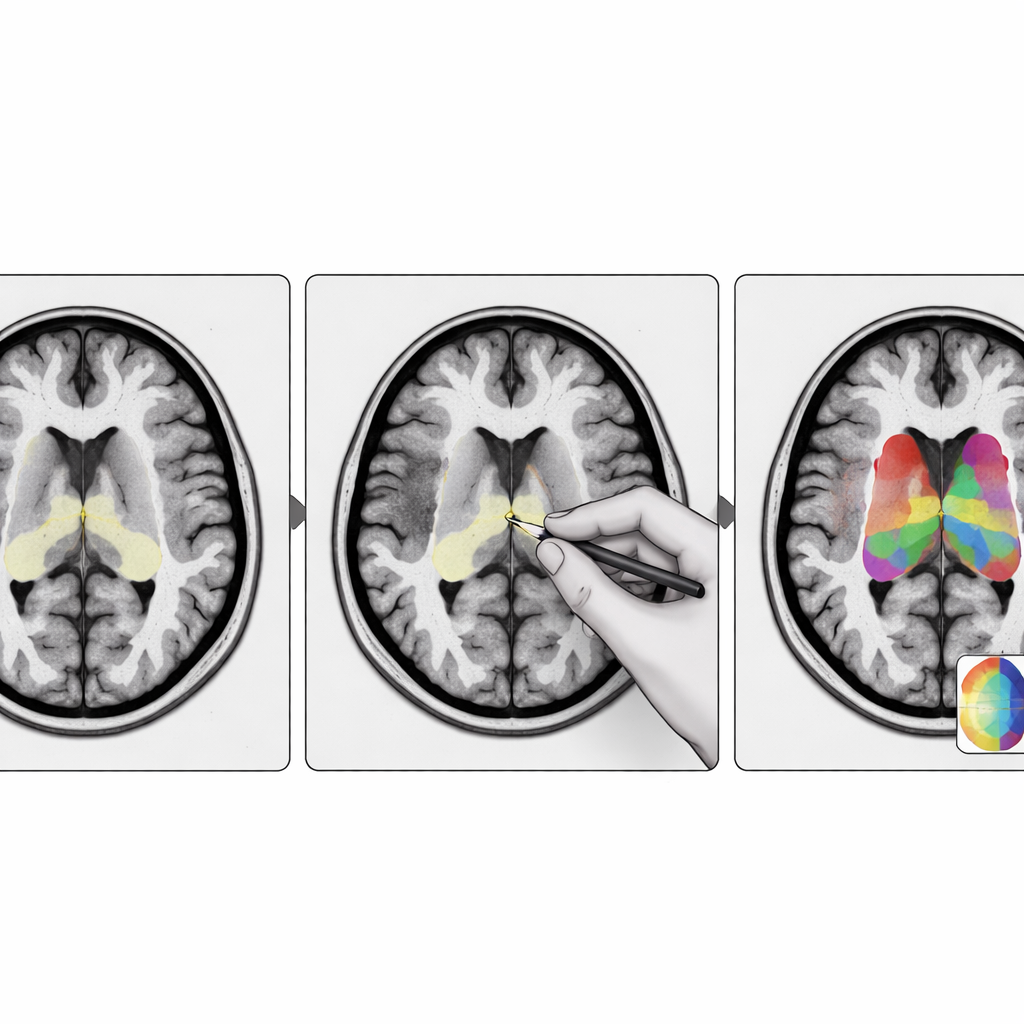
Wat dit betekent voor patiënten en clinici
Voor niet‑specialisten is de kernboodschap dat betere digitale kaarten van kleine hersengebieden chemische hersenscans betrouwbaarder kunnen maken. StriaSeg‑iARM biedt een flexibel kader waarin een deep learning‑model het grootste deel van het werk doet, maar specialisten toch kunnen ingrijpen om lastige gevallen te corrigeren zonder het systeem opnieuw te trainen. Deze combinatie van automatisering en deskundige supervisie verbetert de precisie van metingen die worden gebruikt om aandoeningen als de ziekte van Parkinson te diagnosticeren en te volgen, en het kan worden aangepast aan andere organen en ziekten waarin kleine, moeilijk zichtbare structuren belangrijke aanwijzingen bevatten.
Bronvermelding: Kim, J., Kim, D., Kim, S. et al. An interactive cascaded deep learning framework with expert refinement for accurate striatal subregion segmentation. Sci Rep 16, 6550 (2026). https://doi.org/10.1038/s41598-026-36399-0
Trefwoorden: beeldvorming bij de ziekte van Parkinson, striatale segmentatie, deep learning in radiologie, hersen PET MRI, neurodegeneratieve biomarkers