Clear Sky Science · nl
Staphylococcus capitis-stam die twee bacteriocinen produceert, capidermicine en micrococcine P1, vertoont breedspectrum-antimicrobiële activiteit
Waarom kleine huidbacteriën belangrijk zijn voor superbug-dreigingen
Infecties met antibioticaresistente bacteriën nemen wereldwijd toe en artsen raken steeds meer zonder betrouwbare middelen. Een veelbelovende benadering is om onze eigen “goede” microben in te zetten tegen de schadelijke soorten. Deze studie richt zich op een veelvoorkomende huidbacterie, Staphylococcus capitis, en toont aan dat een specifieke stam, HBC3 genoemd, van nature twee krachtige kiemdodende moleculen produceert. Samen kunnen deze moleculen gevaarlijke ziekenhuispathogenen onderdrukken, waaronder methicilline-resistente Staphylococcus aureus (MRSA), wat suggereert dat vriendelijke huidbacteriën zelf in de toekomst tot infectiebestrijdingsmiddelen ontwikkeld zouden kunnen worden.
Een huidbewoner met verborgen vuurkracht
S. capitis leeft normaal gesproken geruisloos op onze huid, vooral op de hoofdhuid, en is meestal onschadelijk. De onderzoekers screenenden 18 S. capitis-stammen die uit neuzen van mensen waren verzameld om te zien of er een stam MRSA kon remmen, een belangrijke oorzaak van moeilijk te behandelen infecties. Eén stam, HBC3, sprong eruit. In laboratoriumtests onderdrukte zij sterk een grote verscheidenheid aan Gram-positieve bacteriën, waaronder MRSA, vancomycine-resistente enterokokken (VRE), Streptococcus pyogenes, Listeria monocytogenes en Bacillus- en Clostridium-soorten die ernstige ziekten kunnen veroorzaken. Opmerkelijk was dat er geen effect werd gezien op meerdere veelvoorkomende Gram-negatieve bacteriën zoals Escherichia coli en Klebsiella pneumoniae, wat wijst op een gerichte maar krachtige werking in plaats van ongerichte doding. 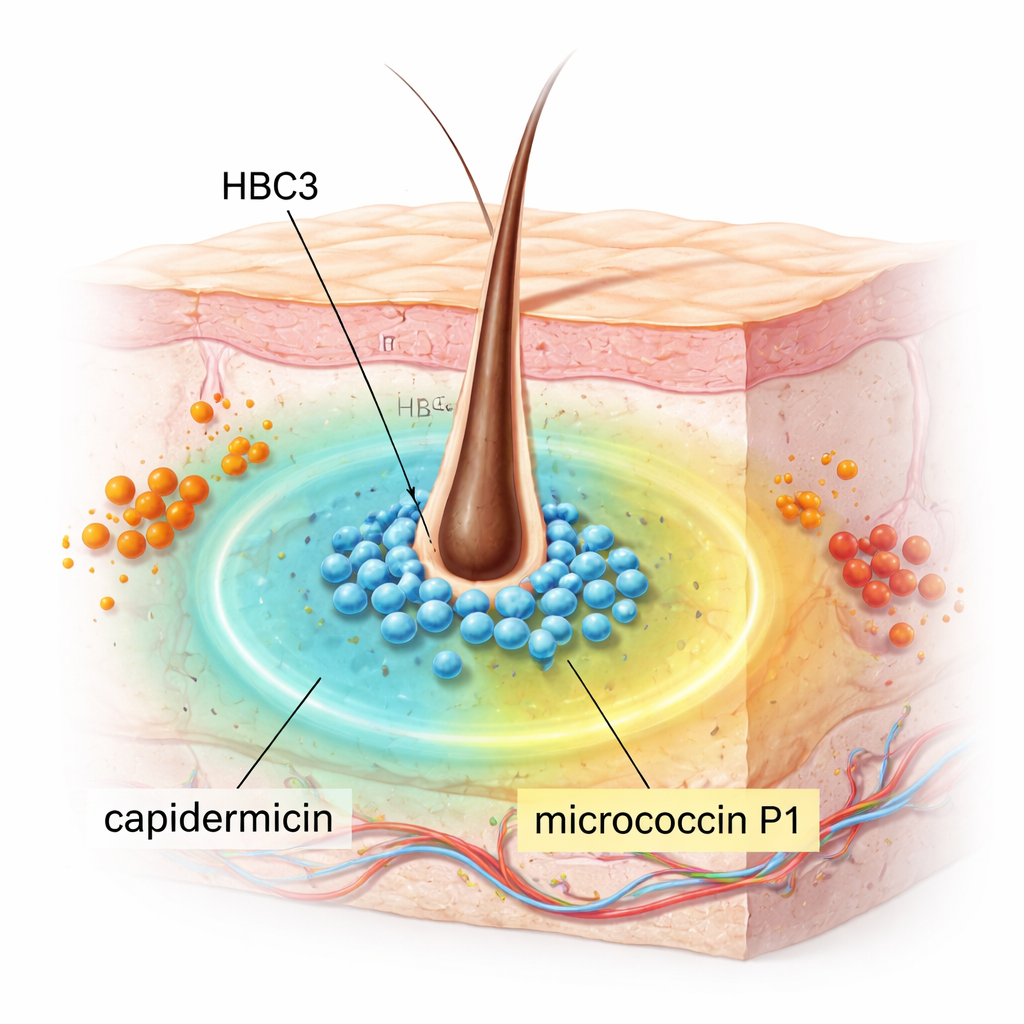
Twee natuurlijke antibiotica op één klein genetisch “mini-chromosoom”
Om te ontdekken hoe HBC3 deze brede antimicrobiële slagkracht verkrijgt, decodeerde het team het volledige genoom. Ze identificeerden een klein circulair DNA-element, een plasmide genaamd pHBC3_1, dat de volledige instructies bevat voor het maken van twee verschillende bacteriocinen—natuurlijke, antibioticumachtige peptiden die door bacteriën worden geproduceerd. De ene is capidermicine, een klein positief geladen peptide dat eerder in andere S. capitis-stammen is gezien. De andere is micrococcine P1 (MP1), een thiopeptide dat de eiwitsynthese in doelbacteriën blokkeert en tot nu toe niet was gerapporteerd in S. capitis. Toen deze plasmide uit HBC3 werd verwijderd, verloor de stam volledig haar antibacteriële activiteit, wat bevestigt dat deze genen essentieel zijn voor haar verdedigingsvermogen.
Verschillende doelen, gedeeld doel
Door elk bacteriocine afzonderlijk te zuiveren, testten de wetenschappers hoe goed ze verschillende microben remden. MP1 toonde brede en sterke activiteit tegen veel Gram-positieve kokken, waaronder MRSA en enterokokken, bij lage concentraties. Capidermicine daarentegen was het meest effectief tegen staafvormige Gram-positieve bacteriën zoals Bacillus coagulans en Listeria, maar had zwakke of geen werking op staphylokokken onder de gebruikte condities. Toen het team beide peptiden combineerde tegen B. coagulans, zagen ze een additief effect: lagere doses samen bereikten sterkere groeiremming dan elk peptide afzonderlijk. Deze complementaire targeting betekent dat HBC3 een bredere reeks concurrenten kan onderdrukken door twee verschillende moleculaire wapens in te zetten die zijn afgestemd op verschillende bacterievormen en celoppervlakken. 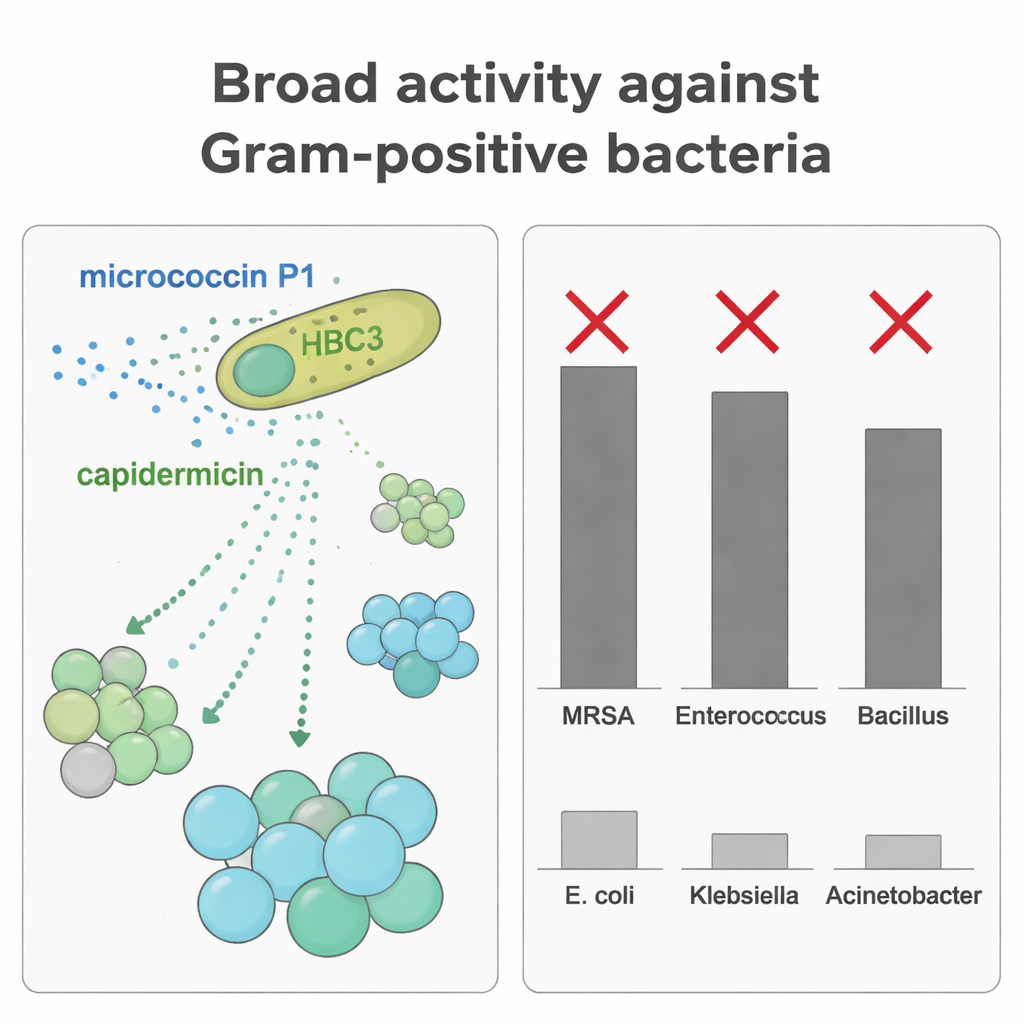
Ruimte winnen in druk bezette microbieel buurten
Om competitie uit de praktijk na te bootsen, co-kweekten de onderzoekers HBC3 met MRSA, VRE en B. coagulans op dezelfde platen. De normale HBC3-stam elimineerde deze pathogenen bijna volledig uit de gemengde gemeenschappen, terwijl een versie zonder plasmide hen liet gedijen. Genetische vergelijkingen suggereren dat de dubbel-bacteriocine-plasmide waarschijnlijk is ontstaan door vroegere fusie en herschikking van afzonderlijke plasmiden, geholpen door mobiele DNA-elementen die genclusters tussen bacteriën kunnen verplaatsen. Deze samengestelde plasmide geeft HBC3 een duidelijk voordeel in drukke omgevingen zoals huid of slijmvliezen, waar veel microben om voedingsstoffen en ruimte concurreren.
Van huidbondgenoot naar toekomstige probiotica?
De studie concludeert dat S. capitis HBC3 is uitgerust met een zeldzame combinatie van twee verschillende bacteriocinen op één plasmide, waardoor het in staat is meerdere klinisch belangrijke Gram-positieve pathogenen sterk te remmen, waaronder antibioticaresistente stammen. Omdat HBC3 zelf geen bekend risicogerelateerd lijnageonderdeel is en geen detecteerbare geneesmiddelresistentiegenen draagt, kan het een kandidaat zijn voor ontwikkeling als een gericht probioticum of decolonisatiemiddel—ontworpen om bijvoorbeeld selectief S. aureus op de huid of in de neus terug te dringen terwijl meer goedaardige buren worden gespaard. Voordat zulke toepassingen werkelijkheid kunnen worden, zullen veiligheid, effectiviteit bij dieren en mensen en de langetermijninvloed op de normale microbiota zorgvuldig moeten worden getest, maar het werk benadrukt hoe onze eigen microben kunnen helpen de aanhoudende superbug-crisis te bestrijden.
Bronvermelding: Ohdan, K., Suzuki, Y., Kawada-Matsuo, M. et al. Staphylococcus capitis strain producing dual bacteriocins, capidermicin and micrococcin P1, shows broad-spectrum antimicrobial activity. Sci Rep 16, 6835 (2026). https://doi.org/10.1038/s41598-026-36393-6
Trefwoorden: bacteriocinen, Staphylococcus capitis, micrococcine P1, capidermicine, antibioticaresistentie