Clear Sky Science · nl
Inzetten van high-throughput virtuele screening (HTVS) voor het identificeren van nieuwe lactaatdehydrogenase (LDH)-remmers met antikanker-eigenschappen
Waarom dit onderzoek belangrijk is voor kankerbehandeling
Kankercellen herprogrammeren vaak hun energiehuishouding, en die verschuiving kan worden benut om slimmere, selectievere geneesmiddelen te ontwikkelen. Deze studie onderzoekt een sleutelenzym in het metabolisme, lactaatdehydrogenase (LDH), dat tumoren helpt te gedijen onder moeilijke omstandigheden en resistentie tegen behandeling kan bevorderen. Met behulp van geavanceerde computergebaseerde screening en laboratoriumtests identificeerden de onderzoekers twee nieuwe kleine moleculen die LDH blokkeren en veelbelovende antikankereffecten laten zien in prostaatkankercellijnen.
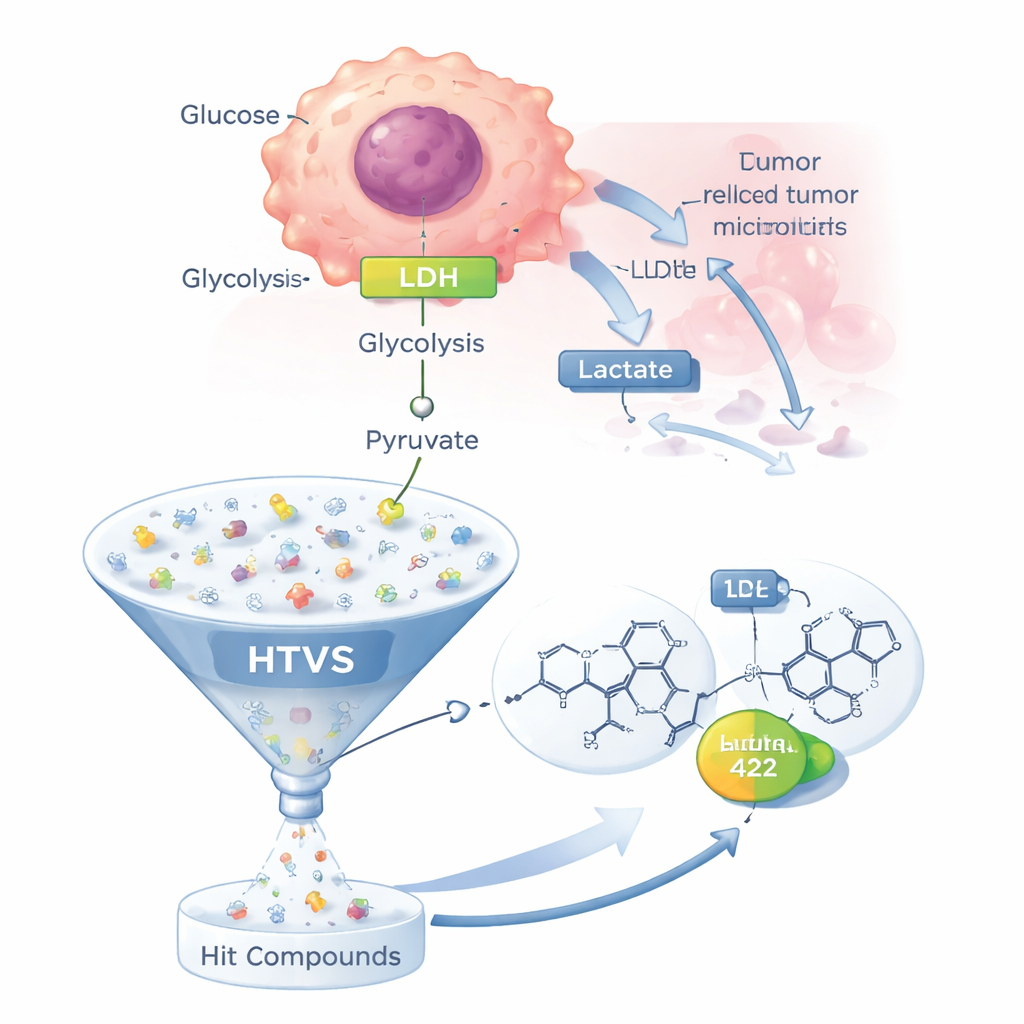
Het vreemde metabolisme van kankercellen
De meeste gezonde cellen gebruiken zuurstof efficiënt in hun mitochondriën om energie te produceren. Veel kankercellen vertrouwen echter sterk op een minder efficiënte route, glycolyse, zelfs wanneer er voldoende zuurstof is — een verschijnsel dat bekendstaat als het Warburg-effect. In deze versnelde route wordt glucose afgebroken tot pyruvaat, dat door LDH wordt omgezet in lactaat in plaats van naar de mitochondriën te gaan. Het lactaat wordt uit de cel gepompt, waardoor de omgeving van de tumor verzuurt, wat kankercellen helpt om celdood te ontlopen, de immuunaanval te verzwakken en zelfs de werking van veel chemotherapieën te verminderen. Omdat LDH centraal staat in dit veranderde metabolisme en er nog geen LDH-gerichte geneesmiddelen zijn goedgekeurd, is het een prioriteitsdoel geworden voor nieuwe antikankertherapieën.
Computers gebruiken om door een half miljoen moleculen te zoeken
In plaats van potentiële middelen één voor één in het lab te testen, gebruikte het team een high-throughput virtuele screening (HTVS)-strategie. Ze begonnen met 28 LDH-remmende moleculen die al in de wetenschappelijke literatuur waren gerapporteerd en destilleerden daaruit een „farmacofore” — een abstract 3D-patroon van kenmerken die elk goed LDH-remmend middel waarschijnlijk deelt. Ze pasten dit model vervolgens toe op een commerciële bibliotheek van ongeveer 500.000 geneesmiddelachtige moleculen om te bepalen welke kandidaten de essentiële kenmerken vertoonden. Ongeveer 110.000 moleculen slaagden voor dit eerste filter, en verdere selectie op basis van standaardregels voor „drug-likeness” verkleinde de lijst tot 2.337 realistischer kandidaten voor docking in het LDH-enzym.
Inzoomen op de beste binders
De volgende stap was inschatten hoe stevig deze kandidaten in het actieve centrum van LDH konden passen. Met meerdere niveaus van computationele docking berekenden de onderzoekers hoe elk molecuul mogelijk met specifieke aminozuren in het enzymenzakje zou interageren. Dit meerstapsproces beperkte de pool geleidelijk van duizenden kandidaten tot slechts 59 veelbelovende moleculen, en vervolgens tot vijf duidelijke „hits” met bijzonder sterke voorspelde binding. Twee daarvan, aangeduid als verbindingen 15 en 422, staken er uit omdat moleculaire dynamicasimulaties op de computer suggereerden dat ze over tijd ongewoon stabiele complexen met LDH vormen, waarbij ze sleutelcontacten met kritieke residuen in het actieve centrum behouden en tegelijkertijd een redelijke algehele eiwitstructuur bewaren.
Van de screening naar echte kankercellen
Om te onderzoeken of deze hits relevant waren in levende systemen, kochten de wetenschappers verbindingen 15 en 422 en testten ze in prostaatkankercellijnen DU-145 en PC-3. Beide moleculen remden LDH-activiteit in cellen in nanomolaire concentraties en remden ook direct de activiteit van een gezuiverd LDH-enzym, hoewel ze iets minder potent waren dan een bekende experimentele remmer genaamd GNE‑140. In groeiproeven verminderden de verbindingen de overleving van kankercellen bij lage micromolaire doses, wederom naderend tot de prestatie van GNE‑140. Aanvullende experimenten toonden aan dat de behandelingen licht verhoogde oxidatieve stress veroorzaakten, de mitochondriale membraanpotentiaal verstoorden — een teken van aangetaste energiecentrales — en geprogrammeerde celdood (apoptose) induceerden in DU‑145-cellen, waarbij verbinding 15 van de twee de meer actieve was.
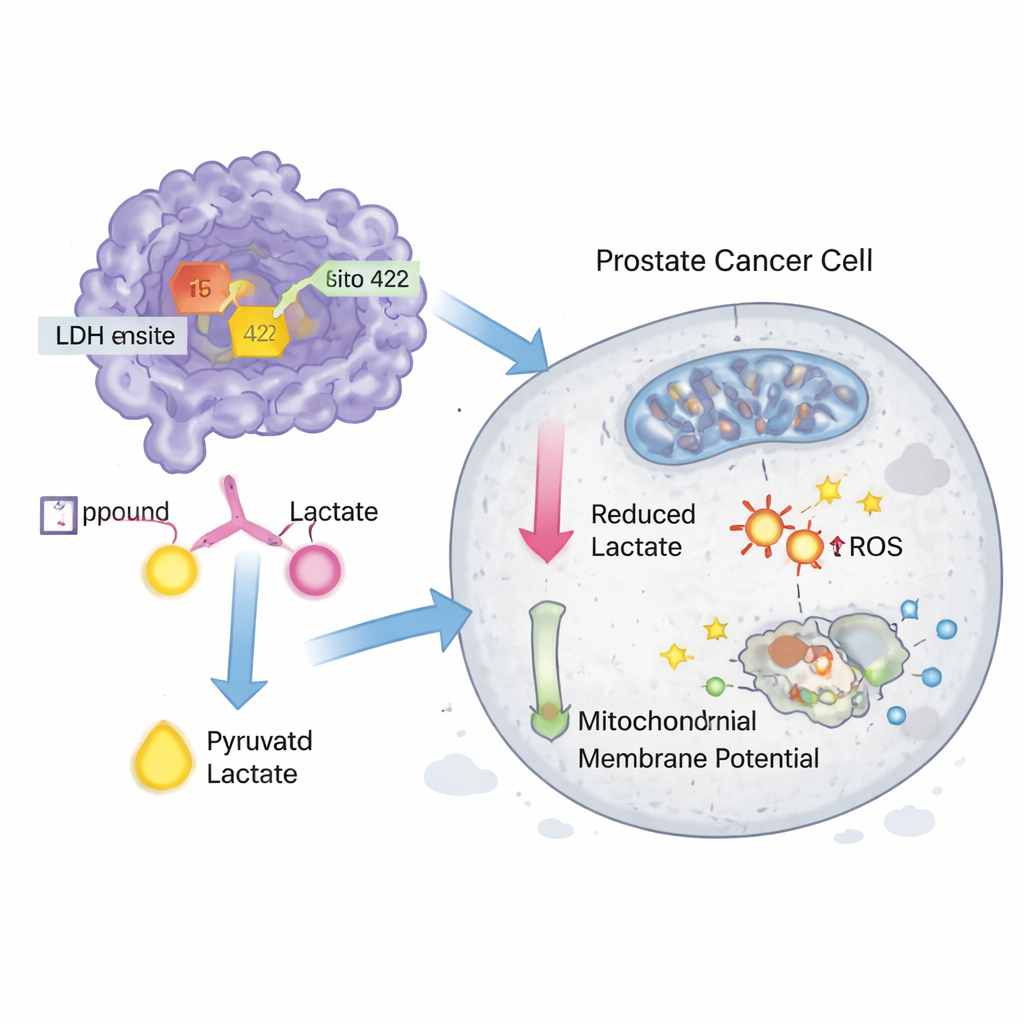
Wat dit kan betekenen voor toekomstige kankergeneesmiddelen
Hoewel deze moleculen geen kant-en-klare geneesmiddelen zijn, vormen ze waardevolle uitgangspunten voor geneesmiddelontwerp. Zowel verbinding 15 als 422 beschikken over chemische eigenschappen die wijzen op betere oplosbaarheid, permeabiliteit en algemene „drug-likeness” dan sommige bestaande LDH-remmers, waardoor ze aantrekkelijke leads zijn voor verdere optimalisatie. De studie toont aan hoe grootschalige computergestuurde screening, geleid door bekende structurele kenmerken, nieuwe LDH-remmers kan aan het licht brengen die kankercellen verzwakken door hun veranderde energievoorziening uit te putten. Met vervolgwerk om hun structuren te verfijnen, directe binding strikter te testen en hun gedrag in diermodellen te bestuderen, zouden deze verbindingen kunnen bijdragen aan een nieuwe klasse antikankermiddelen die tumoren aanvallen via hun unieke metabole kwetsbaarheden.
Bronvermelding: Huang, Y., Benni, S., Yadav, U.P. et al. Deploying the high-throughput virtual screening (HTVS) approach for the identification of new lactate dehydrogenase (LDH) inhibitors with anticancer assets. Sci Rep 16, 5921 (2026). https://doi.org/10.1038/s41598-026-36385-6
Trefwoorden: lactaatdehydrogenaseremmers, kankermetabolisme, virtuele screening, prostaatkanker, ontdekking van antikankergeneesmiddelen