Clear Sky Science · nl
Opregulatie van MGMT bemiddelt Temozolomide‑resistentie die afhankelijkheid van USP5 veroorzaakt
Waarom sommige hersentumoren ophouden te reageren op een belangrijk medicijn
Voor mensen met de agressieve hersenkanker glioblastoom is temozolomide een van de hoofdbehandelingen waarop artsen vertrouwen. Aanvankelijk kan deze chemotherapie de ziekte vertragen, maar tumoren leren vaak hoe ze het middel kunnen negeren. Deze studie stelt een praktische vraag met levens‑of‑doodgevolgen: wat maakt het precies dat kankercellen aan het middel ontsnappen, en kunnen we nieuwe zwakke plekken vinden om aan te vallen zodat de behandeling weer werkt?
Een medicijn dat eerst helpt en daarna vervaagt
Temozolomide werkt door het DNA van snel delende tumorcellen te beschadigen en zo hun dood af te dwingen. Veel glioblastomen produceren echter een reparatie‑eiwit genaamd MGMT dat deze schade kan herstellen. Patiënten van wie de tumoren MGMT inschakelen, hebben doorgaans een slechtere prognose omdat het effect van het middel teniet wordt gedaan. Artsen kunnen de respons deels inschatten door te bepalen of het MGMT‑gen chemisch is uitgeschakeld (gemethyleerd) of aangeschakeld (ongemethyleerd), maar dat verklaart niet volledig waarom resistentie zich ontwikkelt of hoe MGMT‑niveaus in tumorcellen in de loop van de tijd hoog blijven.
Verborgen helpers die het reparatie‑eiwit beschermen
De auteurs bekeken een andere regellaag: de moleculaire “opruimploegen” die bepalen welke eiwitten worden afgebroken en welke worden gespaard. Cellen labelen versleten eiwitten normaal gesproken voor afbraak, terwijl een groep enzymen, de deubiquitinerende enzymen (DUBs), eiwitten van die bestemming kan redden. Door grote publieke kankerdatabases te analyseren en resistentie‑lijnen van glioblastoomcellen in het lab te bestuderen, spitste het team zich toe op twee van die enzymen, USP5 en USP8. In tumourmonsters van honderden patiënten gingen hogere USP5‑niveaus vaak samen met hogere MGMT‑niveaus, en patiënten wiens tumoren beide genen sterk tot expressie brachten, overleden over het algemeen eerder.
Resistentie opbouwen in het lab
Om na te bootsen wat bij patiënten gebeurt, stelden de onderzoekers twee veelgebruikte glioblastoomcelijnen langzaam bloot aan toenemende doses temozolomide totdat de cellen resistent werden. In deze geharde cellen stegen meerdere DUBs, maar USP5, USP8, USP10 en het reparatie‑eiwit MGMT waren bijzonder verhoogd. Toen het team kleine RNA‑moleculen gebruikte om USP5 of USP8 te dempen, werden de resistente cellen plotseling kwetsbaar: ze activeerden zelfvernietigingsprogramma’s, waaronder apoptose en een door stress gedreven zelf‑afbraakproces dat bekendstaat als autophagie. Tegelijkertijd daalden MGMT‑niveaus sterk, en ook een ander resistentie‑gerelateerd eiwit, USP10, nam af, wat suggereert dat deze enzymen zich hoog in een overlevingsnetwerk bevinden.
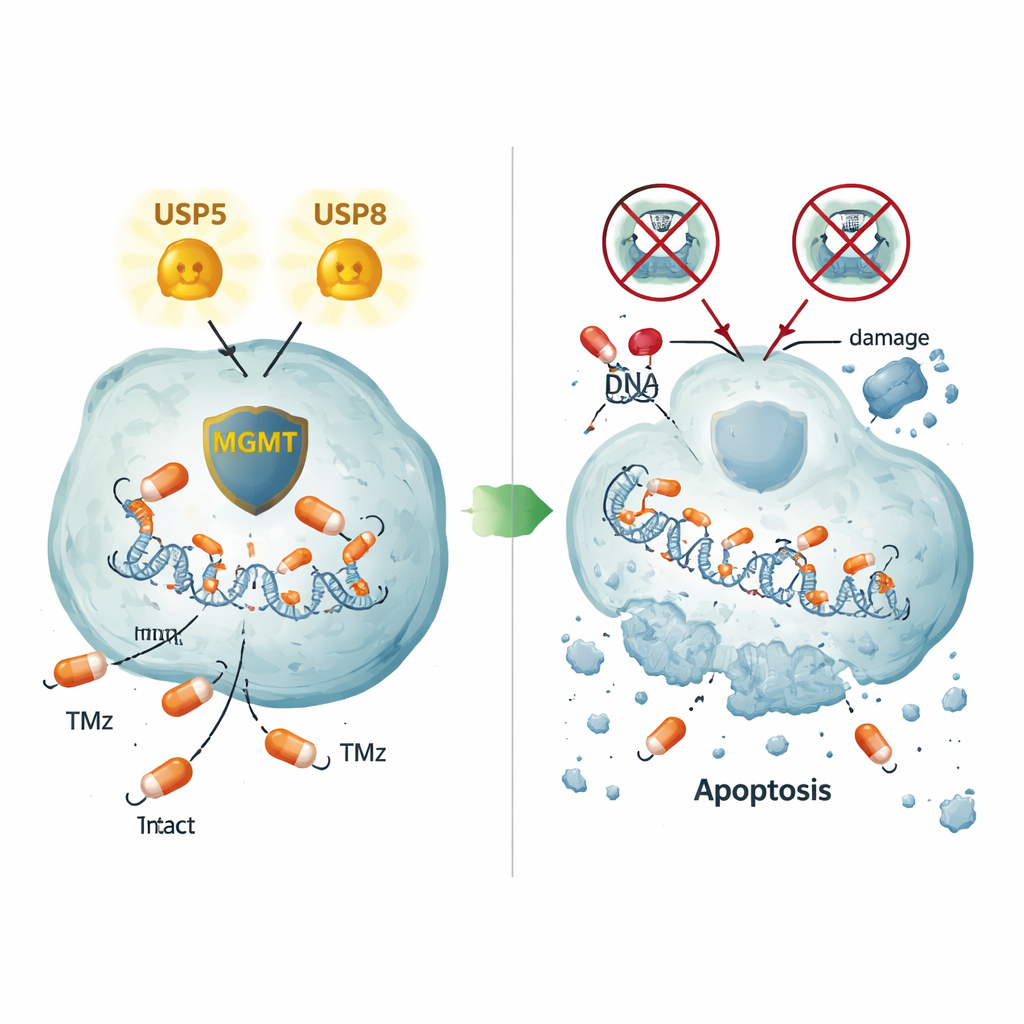
Twee verschillende manieren om MGMT in leven te houden
Gedetailleerde beeldvorming van tumorcellen en menselijk tumormateriaal toonde aan dat USP5 en MGMT vaak samen in dezelfde celregio’s zitten, vooral in het cytoplasma. Het blokkeren van USP5 verlaagde niet alleen MGMT maar zorgde er ook voor dat MGMT door het eiwit‑vermalende machinaal van de cel werd afgebroken, een proces dat omkeerbaar bleek met het middel bortezomib, dat het proteasoom remt. Overexpressie van USP5 in anderszins MGMT‑negatieve cellen was voldoende om MGMT‑eiwitniveaus te verhogen, zelfs in een niet‑hersencellijn, wat een direct stabiliserend effect bevestigt. USP8 bleek anders te werken: het omlaagbrengen ervan verminderde ook MGMT, maar zonder USP5 zelf te veranderen, wat een tweede, USP5‑onafhankelijke route onthult die helpt MGMT te handhaven. Zelfs in een resistente cellijn die helemaal geen MGMT produceerde, leidde het uitschakelen van USP5 of USP8 nog steeds tot uitgebreide celdood, wat wijst op aanvullende resistentie‑routes die door deze enzymen worden geregeld.
Verbonden met het immuunsysteem en nieuwe behandelideeën
Voorbij de medicijnresistentie koppelt de studie USP5 aan de interactie tussen glioblastoom en het immuunsysteem. Analyse van genomische gegevens suggereerde dat veranderingen in USP5‑niveaus en genkopie‑aantallen de balans van verschillende immuuncellen rond de tumor verschuiven, waaronder cytotoxische T‑cellen en regulerende T‑cellen. Eerder werk heeft ook aangetoond dat USP5 PD‑L1 kan stabiliseren, een eiwit dat tumoren gebruiken om aanvallende T‑cellen uit te schakelen. Samen suggereren de bevindingen dat USP5 tumoren zowel kan helpen chemotherapie te overleven als immuunaanvallen te ontlopen, waardoor het een bijzonder aantrekkelijke doelfactor voor geneesmiddelen is.
Wat dit betekent voor toekomstige therapie van hersenkanker
Simpel gezegd identificeren deze resultaten USP5 en USP8 als belangrijke bodyguards die het MGMT‑reparatie‑eiwit beschermen en glioblastoomcellen helpen resistent te zijn tegen temozolomide. Door deze bodyguards uit te schakelen konden de auteurs in het laboratorium medicijnresistente cellen doden en MGMT‑niveaus verlagen, zelfs in gevallen waarin MGMT‑gebaseerde resistentie niet het enige probleem was. Dat wekt de hoop dat toekomstige medicijnen gericht op USP5 of USP8, mogelijk in combinatie met bestaande chemotherapie en immuuntherapieën, hardnekkige hersentumoren opnieuw gevoelig kunnen maken en patiënten meer tijd kunnen geven.
Bronvermelding: Bhardwaj, S., Sanjay, Sharma, D. et al. MGMT upregulation mediates Temozolomide resistance conferred USP5 dependency. Sci Rep 16, 6118 (2026). https://doi.org/10.1038/s41598-026-36379-4
Trefwoorden: glioblastoom, resistentie tegen temozolomide, MGMT, USP5, deubiquitinerende enzymen