Clear Sky Science · nl
Ontsluiering van COPD-pathogenese: een multi-omics-benadering om metabolieten en genetische koppelingen te identificeren
Waarom longziekte en lichaamssamenstelling verbonden zijn
Chronische obstructieve longziekte (COPD) staat vooral bekend als een rokersziekte van de longen, maar deze studie toont aan dat wat er in onze bloedchemie gebeurt net zo belangrijk kan zijn als wat we inademen. Door grote genetische datasets te combineren met gedetailleerde metingen van kleine moleculen in het bloed en laboratoriumexperimenten op menselijke luchtwegcellen, onthullen de onderzoekers hoe verstoorde vetverwerking in het lichaam COPD kan bevorderen — en hoe een bekend inhalatiemiddel, Salbutamol, op een verrassende manier zou kunnen helpen.
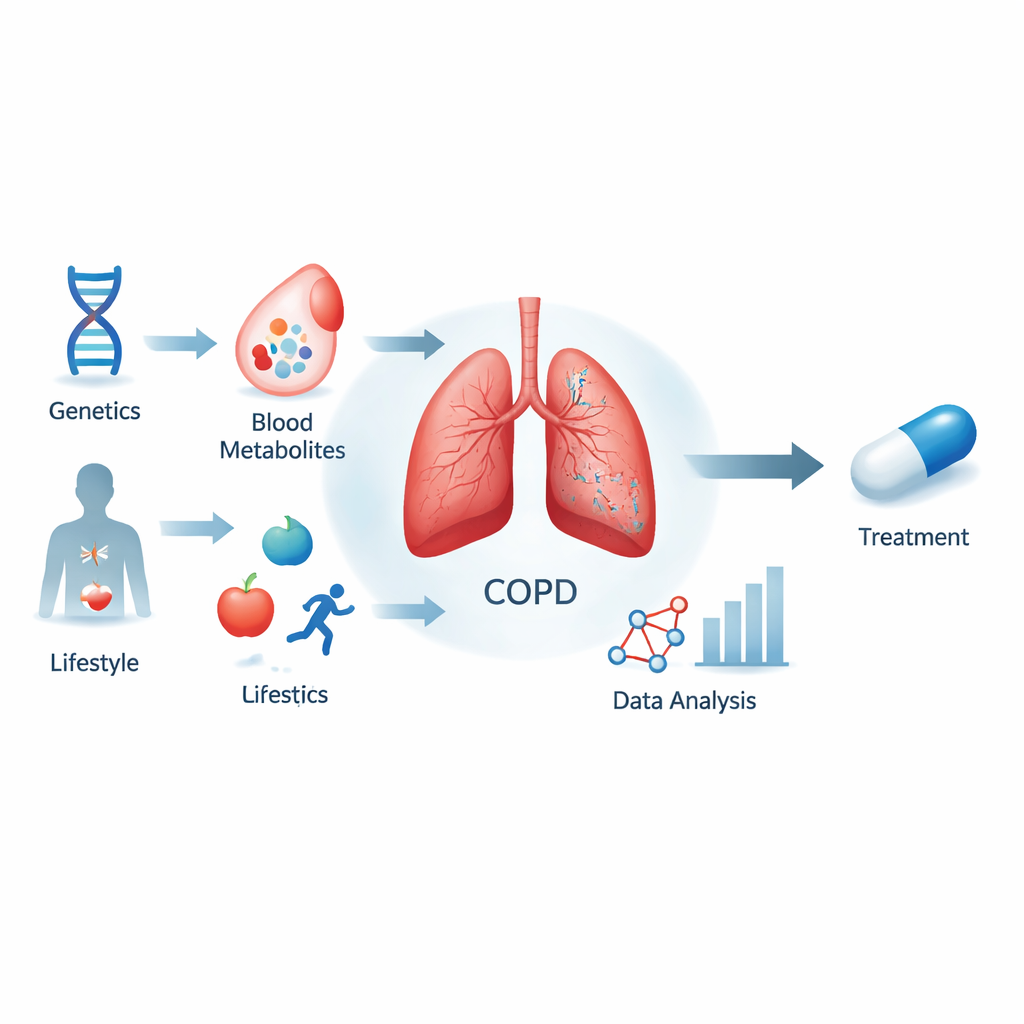
Dieper kijken in COPD voorbij roken
COPD treft honderden miljoenen mensen wereldwijd en zal naar verwachting de derde belangrijkste doodsoorzaak worden. Hoewel roken en luchtvervuiling belangrijke oorzaken zijn, verklaren ze niet volledig wie COPD krijgt of hoe snel het vordert. Het team achter dit werk vroeg zich af of specifieke bloedmoleculen, metaboleten genoemd, niet alleen schade aanwijzen maar ook actieve spelers in de ziekte zijn. Ze concentreerden zich op meer dan 1.400 metaboleten gemeten in grote Europese onderzoeken en koppelden deze aan het risico op COPD door gebruik te maken van genetische verschillen tussen mensen als een soort natuurlijk experiment.
Genen gebruiken om oorzaak en gevolg te testen
Om verder te gaan dan simpele correlatie gebruikten de onderzoekers een techniek die Mendeliaanse randomisatie heet. Simpel gezegd volgden ze of mensen die worden geboren met genvarianten die bepaalde metaboleten verhogen of verlagen, ook hogere of lagere kansen hebben om COPD te ontwikkelen. Deze aanpak helpt echte oorzaken te scheiden van levensstijlfactoren die het beeld kunnen vertroebelen, zoals koffie drinken of roken. Van de 1.400 metaboleten sprongen er aanvankelijk zes uit als gekoppeld aan COPD-risico. Een tweede, strengere genetische toets liet echter zien dat slechts twee — Carnitine C14 en 3-hydroxyoleoylcarnitine — hetzelfde onderliggende genetische signaal delen als COPD zelf. Beide hebben te maken met de verwerking van langeketenvetzuren, wat suggereert dat vetmetabolisme, niet alleen ontsteking en luchtstroom, centraal staat in COPD.
Van moleculen naar sleutelregelpunten
Nadat de twee betrouwbare metaboleten waren geïdentificeerd, volgden de onderzoekers de metabole “wegen” waarlangs ze lopen. Deze wegen kwamen samen in het vetzuurmetabolisme en wezen op een set enzymen die als verkeerslichten fungeren en bepalen hoeveel vet wordt opgebouwd of afgebroken — in het bijzonder de enzymen ACACA en ACACB. Door bestaande geneesmiddelen- en eiwitinteractiedatabases te doorzoeken, ontdekten ze dat deze enzymen in hetzelfde netwerk zitten als ADRB2, het eiwitdoelwit van Salbutamol, een veelgebruikt reddingsinhalatiemiddel voor COPD. Analyses van longweefsel van patiënten toonden dat ACACA en ACACB omhooggereguleerd waren, terwijl ADRB2 omlaaggereguleerd was, wat consistent is met een toestand van vetzuuroverbelasting in zieke longen.
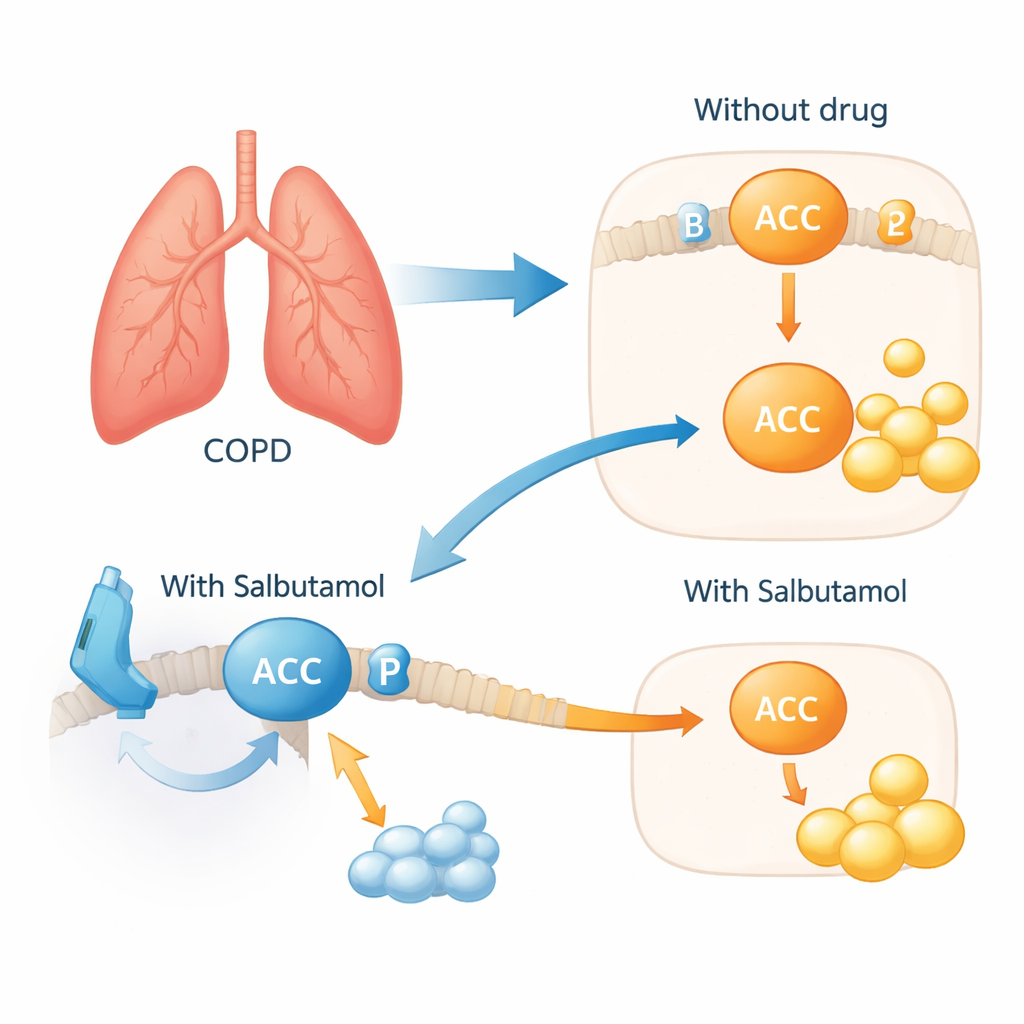
Een inhalator die ook uit de hand lopend vet kalmeert
Om te testen of dit netwerk relevant is in levende cellen, brachten de wetenschappers menselijke bronchiale cellen in contact met extract van sigarettenrook om COPD-achtige stress na te bootsen. De cellen reageerden door ACACA en ACACB op te voeren en een beschermende chemische markering op ACACA te verminderen die normaal vetproductie in bedwang houdt. Toen Salbutamol werd toegevoegd, keerde dit schadelijke patroon om: de beschermende markering op ACACA werd hersteld en tekenen van overmatige vetsynthese namen af. In eenvoudige bewoordingen leek het geneesmiddel de rem erop te zetten wat betreft het vetopbouwende mechanisme binnen luchtwegcellen, via de ADRB2-"schakelaar" aan het celoppervlak. Genetische analyses gerelateerd aan levensstijl ondersteunden verder het idee dat de twee sleutelmetaboleten verbonden zijn met onderliggende biologie en niet alleen met gewoonten zoals koffiedrinken, wat verschillende andere kandidaatmoleculen verklaarde.
Wat dit betekent voor patiënten en toekomstige behandelingen
Voor niet-specialisten is de kernboodschap dat COPD deels kan worden aangedreven door een metabole verkeersopstopping in hoe longcellen vetten verwerken, en dat een veelgebruikt bronchodilatormiddel mogelijk ook stilletjes helpt die opstopping op te ruimen. Carnitine C14 en 3-hydroxyoleoylcarnitine komen naar voren als sterke bloedmarkers die op een dag kunnen helpen mensen met verhoogd risico te signaleren of de ziekteprogressie te volgen. De enzymen ACACA en ACACB, die op sleutelposities in het vetmetabolisme zitten en gekoppeld zijn aan het Salbutamol-doelwit ADRB2, bieden nieuwe aanknopingspunten voor medicijnontwikkelaars. Hoewel meer werk in diverse populaties en diepgaande metabolische studies nodig is, ontsluit deze multi-omics-benadering een route naar COPD-behandelingen die meer doen dan luchtwegen openen — ze kunnen ook een gezonder brandstofgebruik in de longen herstellen.
Bronvermelding: Zeng, M., Liu, J., Cao, X. et al. Unraveling COPD pathogenesis: a multi-omics approach to identify metabolites and genetic links. Sci Rep 16, 6013 (2026). https://doi.org/10.1038/s41598-026-36368-7
Trefwoorden: COPD, vetzuurmetabolisme, Salbutamol, carnitine-biomarkers, multi-omics