Clear Sky Science · nl
Rol van MNX1-gemedieerde histonmodificaties en de PBX-genfamilie bij MNX1-geïnduceerde leukemogenese
Waarom een klein genetisch foutje belangrijk is voor zieke kinderen
De meeste kinderkankers van het bloed zijn tegenwoordig behandelbaar, maar een zeldzame vorm, namelijk infantiele acute myeloïde leukemie (AML), blijft bijzonder dodelijk. Veel van deze zuigelingen delen hetzelfde genetische voorval: twee chromosomen wisselen stukken uit, waardoor een normaal stilstaand ontwikkelingsgen, MNX1, overactief wordt. Deze studie stelt een eenvoudige maar cruciale vraag: zodra MNX1 hoger wordt uitgedrukt, wat doet het dan precies in jonge bloedcellen om ze richting kanker te duwen — en is dat proces te onderbreken?
Van normale babybloedcellen naar onbeheerst groeien
Leukemie ontstaat wanneer onrijpe bloedcellen stoppen met rijpen en zich ongecontroleerd gaan vermenigvuldigen. Bij zuigelingen met de t(7;12)-chromosoomwissel wordt MNX1 abnormaal actief in heel vroege bloedvormende cellen die in de foetale lever en het beenmerg voorkomen. De onderzoekers bouwden een muismodel dat deze situatie nabootst: zij zetten menselijke MNX1 aan in foetale bloedstamcellen, transplantenden deze in muizen en volgden hoe de dieren van een pre-leukemische staat naar volledige leukemie gingen. Door cellen in deze verschillende stadia te vergelijken met gezonde controles konden zij traceren hoe MNX1 in de loop van de tijd de interne controlesystemen van de cel herbedraad.
Hoe MNX1 het instructieboek van de cel herschrijft
MNX1 is een transcriptiefactor, een eiwit dat op DNA zit en regelt welke genen aan- of uitgaan. Het team combineerde meerdere krachtige methoden — massaspectrometrie, RNA-sequencing en chromatineprofilering — om te zien met welke partners MNX1 samenwerkt en welke genen het verandert. Ze vonden dat MNX1 samenwerkt met enzymen die chemische merktekens aan histoneiwitten toevoegen, de spoelachtige structuren waar DNA omheen gewikkeld zit. In het bijzonder versterkt MNX1 een "AAN"-merkteken genaamd H3K4me3 en vermindert het een "UIT"-merkteken genaamd H3K27me3 op bepaalde plekken in het genoom. Deze veranderingen versoepelen de lokale DNA-structuur en maken het gemakkelijker voor sleutelgenen die groei stimuleren om aan te gaan.
Een korte duw tegen een kritisch regelgen
Onder de vele beïnvloede genen viel er één op: Pbx1, onderdeel van de PBX-familie van DNA-bindende eiwitten die al lange tijd met leukemie worden geassocieerd. De studie toont aan dat MNX1 direct bindt aan de controleomgeving van het Pbx1-gen, het AAN-merkteken verhoogt en het UIT-merkteken daar weghaalt. Dit zet de expressie van Pbx1 vroeg aan, wanneer cellen nog alleen pre-leukemisch zijn. Verrassend genoeg is MNX1 later — zodra leukemie is vastgesteld — zelf niet langer sterk gebonden op die plek, maar blijft het Pbx1-gen aangeschakeld en blijven de histonmerken in de pro-groeiconfiguratie. Dit suggereert een "hit-and-run"-mechanisme: MNX1 bezoekt kort sleutelregio's van chromatine, laat duurzame epigenetische merktekens achter en kan vervolgens wegtrekken terwijl de veranderde toestand de ziekte blijft voeden.
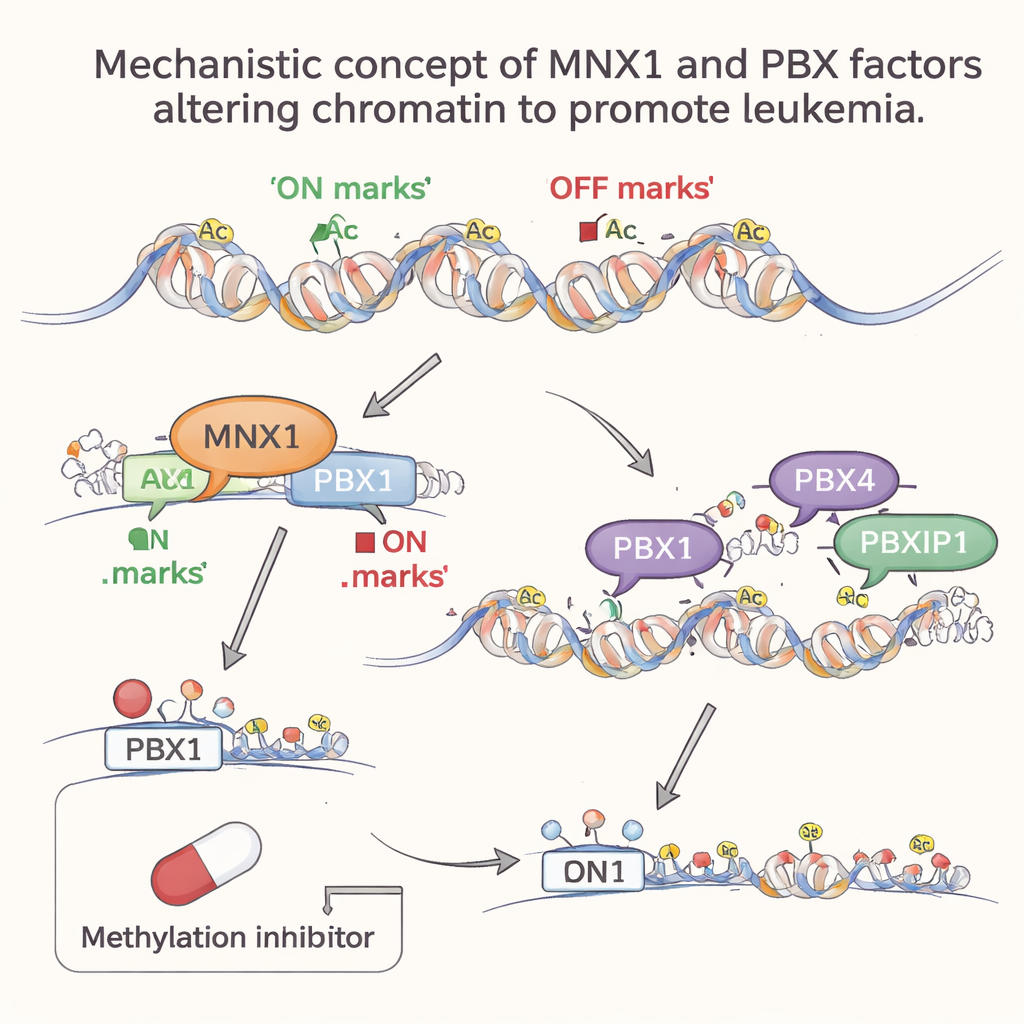
Latere hulpjes doen mee om de kankerstand vast te zetten
Als de leukemie vordert, worden andere PBX-familieleden, PBX4 en PBXIP1, actiever, maar alleen in dit latere stadium. Genoomwijde analyses lieten zien dat hun geprefereerde DNA-motieven sterk verrijkt zijn in regio's van open, actief chromatine die zijn gemodelleerd na MNX1-activiteit. Met andere woorden: MNX1 hervormt eerst het chromatinelandschap en schakelt Pbx1 in; daarna verplaatsen PBX4 en PBXIP1 zich naar deze nieuw-toegankelijke regio's om abnormale genprogramma's te versterken die celdeling stimuleren, normale bloedvorming blokkeren en DNA-reparatie aantasten. Deze stapsgewijze betrokkenheid wijst op een taakverdeling: PBX1 fungeert als een MNX1-afhankelijke vroege schakel, terwijl PBX4 en PBXIP1 helpen het leukemische programma te onderhouden.
Het blokkeren van de chemische merktekens die leukemie voeden
Aangezien MNX1 werkt via enzymen die methylgroepen aan histonen toevoegen, testte het team of een brede methyltransferaseremmer, Sinefungin, deze keten van gebeurtenissen kon verstoren. In pre-leukemische foetale bloedcellen die MNX1 tot expressie brachten, verminderde Sinefungin sterk de Pbx1-niveaus, in overeenstemming met het blokkeren van de promotor-specifieke methylatie waarop MNX1 vertrouwt. Daarentegen veranderden PBX4- en PBXIP1-niveaus nauwelijks, wat past bij hun latere, indirecte activatie tijdens ziekteprogressie. Samen onderbouwen deze resultaten sterk dat infantiele AML met t(7;12) niet alleen wordt aangedreven door een defect gen, maar door een cascade van duurzame epigenetische veranderingen die MNX1 in gang zet.
Wat dit betekent voor toekomstige behandelingen
Voor niet-specialisten is de kernboodschap dat deze studie een kettingreactie in kaart brengt: een overactief MNX1-gen herbedraadt de chemische merktekens op DNA-verpakkende eiwitten, schakelt PBX1 vroeg in en effent het pad voor PBX4 en PBXIP1 om cellen in een leukemische staat vast te zetten. Omdat deze stappen afhangen van specifieke histonmethylatiepatronen, bieden ze duidelijke, toetsbare doelwitten voor geneesmiddelen die die merktekens verstoren. Op de lange termijn zouden therapieën gericht op de MNX1–PBX-as of de enzymen die deze epigenetische labels plaatsen, kunnen helpen de foutieve instructies uit te schakelen die deze agressieve leukemie bij zuigelingen aandrijven, en zo de kans op duurzame genezing vergroten.
Bronvermelding: Malmhäll-Bah, E., Östlund, A., Nilsson, T. et al. Role of MNX1-mediated histone modifications and PBX gene family in MNX1-induced leukemogenesis. Sci Rep 16, 2593 (2026). https://doi.org/10.1038/s41598-026-36367-8
Trefwoorden: infant acute myeloid leukemia, MNX1, PBX1 PBX4 PBXIP1, epigenetic histone methylation, t(7;12) chromosoomtranslocatie