Clear Sky Science · nl
Translationele evaluatie van BUB1B als precisiegeneesmiddel-biomarker voor hepatocellulair carcinoom
Waarom een gen voor celdeling van belang is bij leverkanker
De meeste mensen denken bij kanker aan zichtbare tumoren op scans, maar diep in die gezwellen werken microscopische regelsystemen die bepalen hoe en wanneer cellen delen. Deze studie richt zich op één zo’n regelaar, een gen genaamd BUB1B, en laat zien hoe het artsen kan helpen voorspellen welke leverkankerpatiënten het slecht zullen doen, wie mogelijk op bepaalde medicijnen reageert, en waarom sommige tumoren het immuunsysteem te slim af zijn. Door een basale celcyclusregulator om te vormen tot een soort ‘dashboard’ voor het gedrag van leverkanker, wijst het werk op mogelijkheden voor meer precieze en geïndividualiseerde behandeling.
Een veelvoorkomende leverkanker heeft betere richtlijnen nodig
Hepatocellulair carcinoom, de meest voorkomende vorm van primaire leverkanker, wordt vaak laat ontdekt, wanneer symptomen optreden en behandelopties beperkt zijn. Bestaande bloedtesten en weefselmarkers, zoals alfa-fetoproteïne of Ki-67, zijn onvolmaakt: ze vangen vroeg ziekte niet altijd betrouwbaar of sturen op maat gemaakte therapieën. De auteurs zochten daarom naar een ander type marker—een die het interne bedrading van kankercellen weerspiegelt in plaats van alleen hun aanwezigheid. Ze concentreerden zich op BUB1B, een eiwit dat helpt verzekeren dat chromosomen correct worden verdeeld wanneer cellen splitsen. Als dit systeem ontspoort, hoopt genetische schade zich op, wat agressieve tumoren kan aanwakkeren.
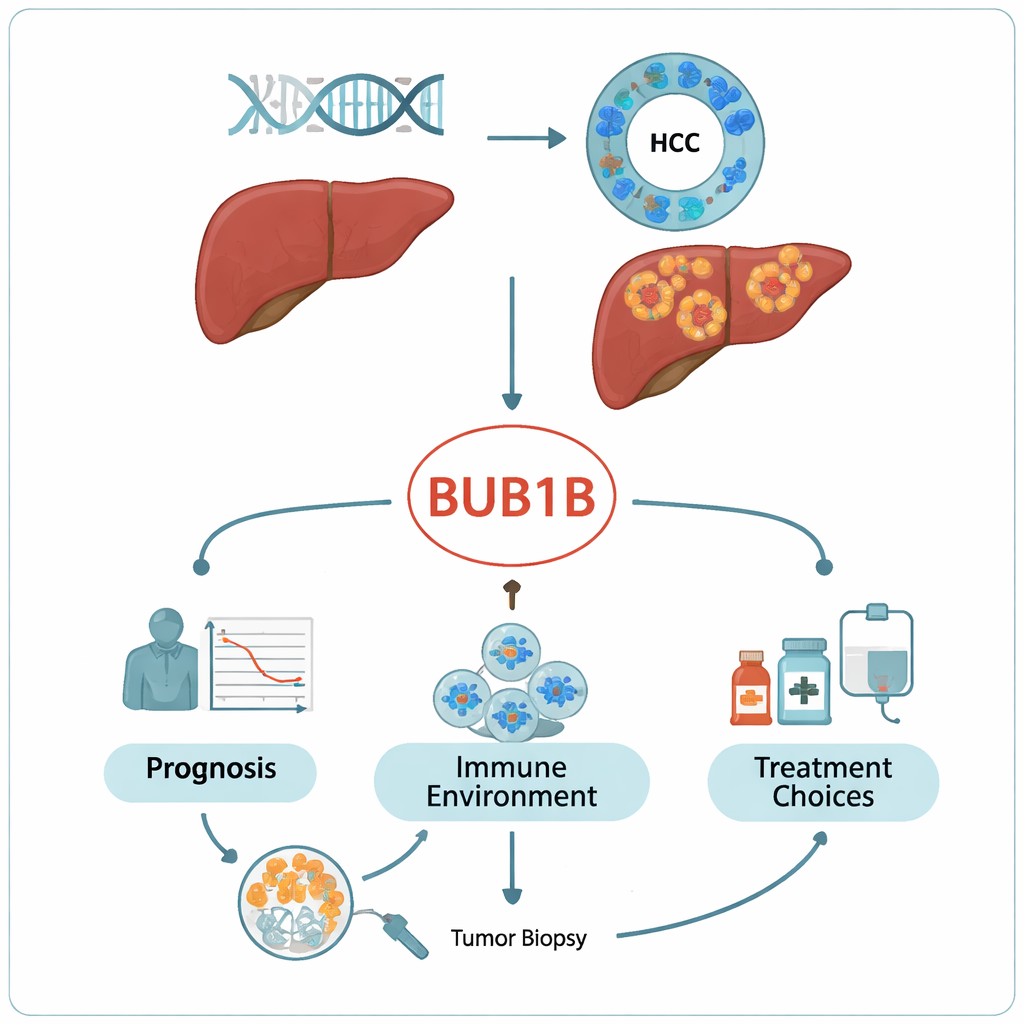
BUB1B volgen in diverse kankers en echte patiënten
Met grote openbare kankerdatabanken, waaronder The Cancer Genome Atlas, bekeken de onderzoekers eerst de activiteit van BUB1B in veel tumortypen. Ze vonden dat het in 19 verschillende kankers op hogere niveaus aan stond, met name sterke overactiviteit in levertumoren vergeleken met aangrenzend gezond weefsel. Patiënten van wie de leverkankers meer BUB1B hadden, leefden over het algemeen korter, zelfs na correctie voor het stadium van hun kanker, waardoor BUB1B een onafhankelijke waarschuwingsfactor werd. Een diepte-analyse van 50 leverkankerpatiënten die in hun eigen ziekenhuis waren behandeld bevestigde het patroon: tumoren toonden intense BUB1B-kleuring onder de microscoop, vooral in het celcytoplasma, en hoge niveaus gingen samen met grotere tumoren, gevorderder stadium en slechtere overleving.
Genetische chaos, geneesmiddelrespons en een verward immuunsysteem
Hoge BUB1B-niveaus duidden niet alleen op een gevaarlijke tumor; ze waren gekoppeld aan diepere instabiliteit in het DNA van de kanker. Tumoren met meer BUB1B vertoonden meer tekenen van defecte DNA-reparatie en subtiele vormen van microsatellietinstabiliteit, kenmerken van genomische chaos die zowel snelle evolutie kunnen aansturen als de reactie op behandeling vormgeven. Computermodellen die genpatronen koppelden aan medicijntests suggereerden dat BUB1B-rijke levertumoren mogelijk kwetsbaarder zijn voor bepaalde middelen, waaronder het gerichte medicijn sorafenib en klassieke chemotherapieën zoals paclitaxel en doxorubicine, terwijl ze relatief resistent leken tegen middelen die op de EGFR-route mikken. Tegelijk bevatten deze tumoren veel immuuncellen, vooral T-cellen, maar scoorden ze toch hoog op maatstaven voor immuun dysfunctie en uitsluiting—wat betekent dat het immuunsysteem aanwezig maar effectief uitgeschakeld was, en minder waarschijnlijk zou reageren op gangbare immunotherapieën die PD-1 of PD-L1 blokkeren.
Hoe BUB1B groeisignalen binnen kankercellen aanwakkert
Om verder te gaan dan statistische verbanden, testte het team wat er gebeurt wanneer BUB1B chemisch wordt geblokkeerd in in het laboratorium gekweekte leverkankercellen. Het remmen van dit gen zette een hele keten van groeisignalen stil die vaak onder de MAPK-pathways worden geschaard. Belangrijke spelers op verschillende niveaus—including RAS, bepaalde leden van de RAF-familie, ERK, en meerdere p38 en andere gerelateerde kinasen—werden sterk verminderd. Omdat deze routes fungeren als een relais dat kankercellen vertelt door te blijven delen en bestendig te zijn tegen stress, suggereert het terugbrengen ervan dat BUB1B niet slechts een passieve marker is maar een actieve drijver die helpt de interne bedrading van de kanker te onderhouden. Sommige componenten lieten onverwachte terugslagen zien, wat wijst op ingebouwde feedbacklussen, maar het algemene effect was een brede verzwakking van pro-groeisignalering.
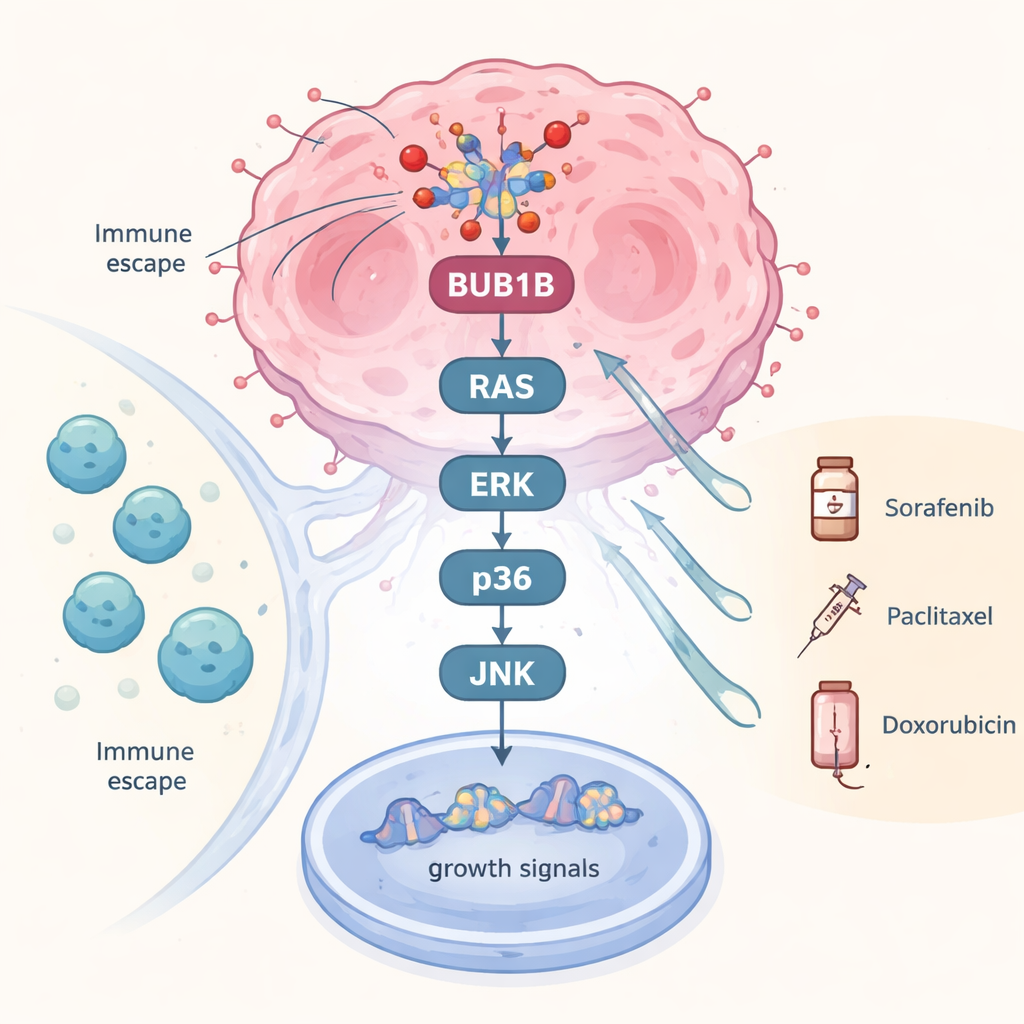
Wat dit betekent voor patiënten en toekomstige zorg
Voor niet-specialisten is de conclusie dat één enkel gen voor celdeling, BUB1B, lijkt te liggen op het kruispunt van drie cruciale eigenschappen van leverkanker: hoe instabiel het tumor-DNA is, hoe het communiceert met het immuunsysteem, en hoe het reageert op meerdere belangrijke geneesmiddelen. Het meten van BUB1B in tumormonsters kan artsen helpen patiënten in risicogroepen te verdelen, de overleving nauwkeuriger in te schatten en behandelingen te kiezen die de zwaktes van de kanker uitbuiten—terwijl wordt onderkend wanneer standaard immunotherapie waarschijnlijk niet effectief is. Omdat levertumoren afhankelijk lijken van BUB1B om hun groeisignalen en stressreacties draaiende te houden, kunnen medicijnen die dit eiwit targeten, alleen of in combinatie met bestaande therapieën, nieuwe wegen openen naar meer precieze en effectieve behandeling van hepatocellulair carcinoom.
Bronvermelding: Sun, Cy., Yu, X., Deng, Lq. et al. Translational evaluation of BUB1B as a precision medicine biomarker for hepatocellular carcinoma. Sci Rep 16, 5301 (2026). https://doi.org/10.1038/s41598-026-36364-x
Trefwoorden: hepatocellulair carcinoom, BUB1B, biomarker, MAPK-signalering, precisie-oncologie