Clear Sky Science · nl
Downregulatie van CDC25C remt HCC-groei via mitokondriale stress-geïnduceerde autofagie en apoptose
Waarom deze leverkankerstudie ertoe doet
Leverkanker behoort tot de dodelijkste kankersoorten wereldwijd, en veel patiënten worden te laat gediagnosticeerd voor chirurgie of standaardbehandelingen effectief zijn. Deze studie onderzoekt één cellulaire "schakelaar", een eiwit genaamd CDC25C, dat lijkt bij te dragen aan de groei van leverkanker terwijl het minder cruciaal is voor gezonde levercellen. Door deze schakelaar omlaag te brengen, ontdekten de onderzoekers dat ze kankercellen konden belasten en uiteindelijk doden via de eigen schoonmaak- en zelfdestructiesystemen van de cel, wat wijst op een veelbelovende en meer selectieve behandelstrategie.
Een groeischakelaar in levertumoren
Elke cel moet beslissen wanneer hij deelt en wanneer hij stopt. CDC25C is een van de sleutelproteïnen die cellen door de delingscyclus duwt. In leverkanker lijkt deze schakelaar vaak in de "aan"-stand vast te zitten, wat tumoren helpt groeien en verspreiden. Het team gebruikte muisleverkankercellen en normale muislevercellen, evenals tumordragende muizen, om kunstmatig het CDC25C-gehalte te verlagen. Ze bevestigden met standaard genetische en eiwittests dat CDC25C sterk werd gereduceerd in hun experimentele groep vergeleken met controles, en creëerden daarmee een degelijk model om te bestuderen wat er gebeurt wanneer deze groeischakelaar wordt teruggedraaid.
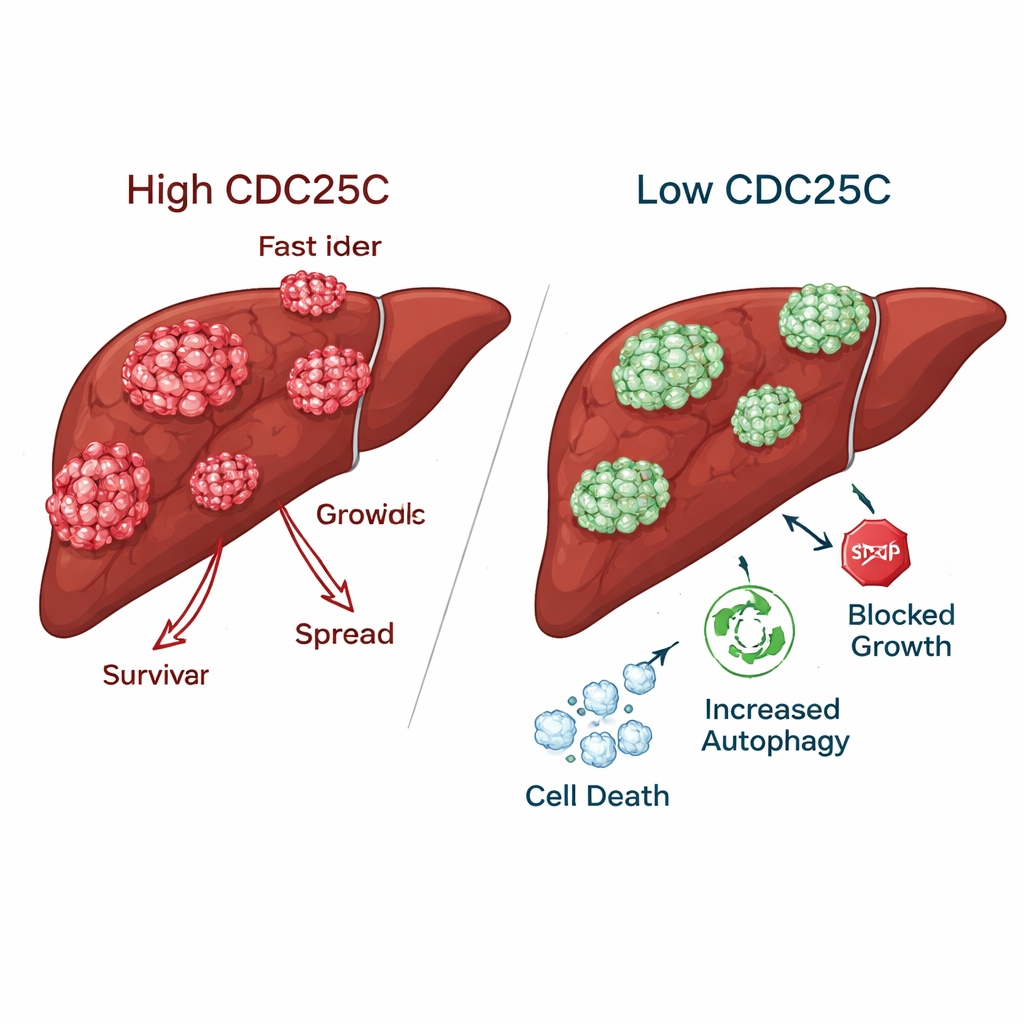
Kanker vertragen terwijl gezonde levercellen gespaard blijven
Wanneer CDC25C werd verlaagd in leverkankercellen, verloren de tumoren veel van hun agressieve eigenschappen. Kankercellen vormden veel minder kolonies, migreerden langzamer over kunstmatige "wonden" en waren minder in staat door barrières te bewegen en te invaseren in laboratoriumtests. Daarentegen toonden normale levercellen juist betere groei en beweging wanneer CDC25C werd verlaagd, wat suggereert dat gezond weefsel CDC25C-remming kan verdragen of er zelfs baat bij heeft. Bij muizen lieten tumoren met verlaagd CDC25C lagere niveaus van dit eiwit zien in zowel gen- als eiwitmetingen, wat bevestigt dat hetzelfde effect in levende dieren optrad.
Stress in de energiecentrales en het schoonmaakteam van de cel
Bij onderzoek van de cellen met elektronenmicroscopie zagen de onderzoekers dat kankercellen met laag CDC25C gezwollen, beschadigde mitochondriën bevatten—de kleine energiecentrales van de cel—samen met blaasachtige structuren genaamd autofagosomen die activatie van het intracellulaire recyclingsysteem, autofagie, aangeven. Ze maten vervolgens belangrijke tekenen van mitochondriale stress: calciumniveaus en reactieve zuurstofsoorten (ROS), die beide verhoogd waren in kankercellen na verlaging van CDC25C. Merkers van de mitochondriale stressrespons, waaronder hulp-eiwitten zoals HSP60 en twee mitochondriale "kwaliteitscontrole"-enzymen, waren ook verhoogd, evenals CHOP, een stressgerelateerd factor die mitochondriale problemen koppelt aan bredere cellulaire reacties. Opmerkelijk genoeg bewogen deze stresssignalen in de tegenovergestelde richting in normale levercellen, wat het idee versterkt dat kankercellen en gezonde cellen zeer verschillend reageren op verlies van CDC25C.
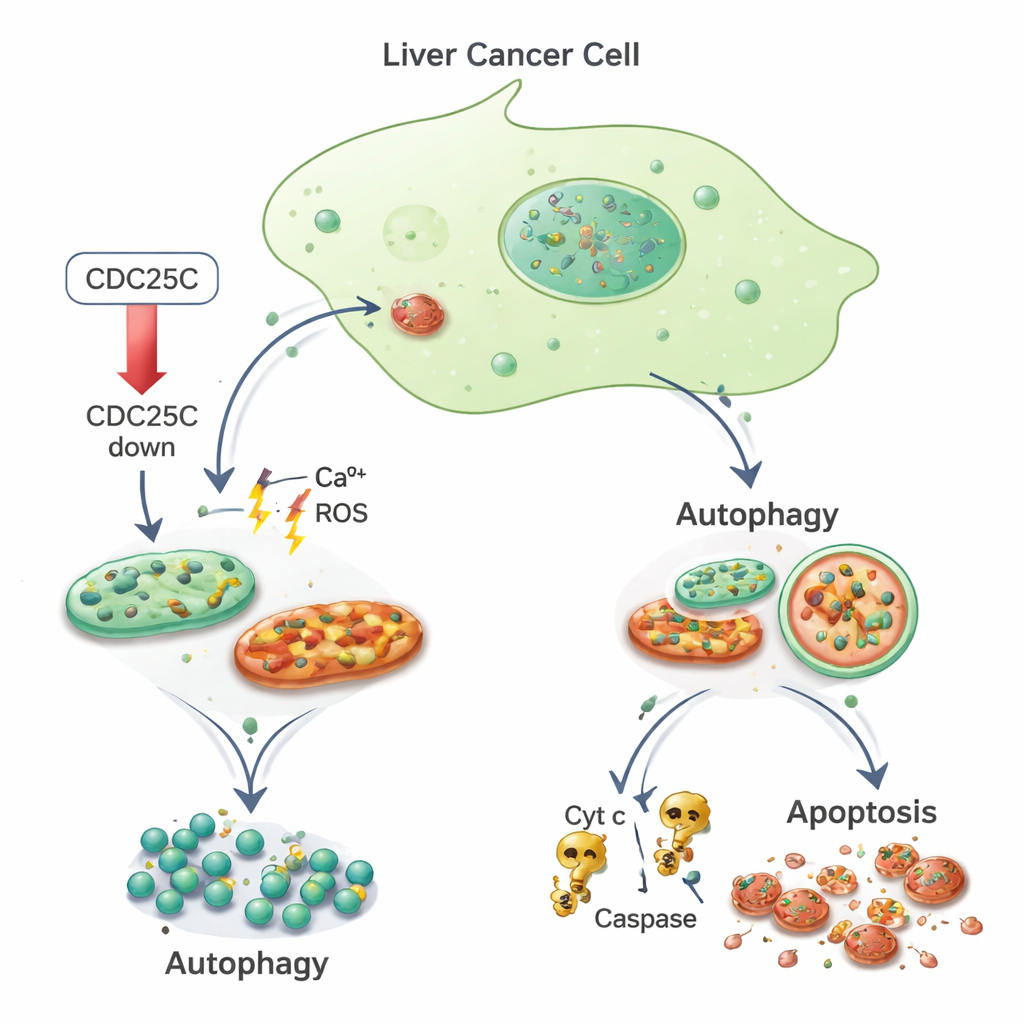
Van stress naar zelfvertering en celdood
Het team vroeg vervolgens hoe deze gestreste kankercellen ermee omgingen. Ze vonden dat merkers van autofagie verhoogd waren in zowel kankercellen als normale levercellen wanneer CDC25C werd verlaagd. Eiwitten zoals LC3 en p62, die de vorming en activiteit van autofagosomen weerspiegelen, namen in niveau toe, wat aangeeft dat cellen hun schoonmaakmechanismen opschroefden. Tegelijkertijd leek bij kankercellen alleen mitochondriale schade de cellen verder voorbij herstel te duwen en in geprogrammeerde celdood te leiden. Met behulp van fluorescente kleurstoffen en flowcytometrie zagen de onderzoekers meer kankercellen met gefragmenteerde, felgekleurde kernen—een kenmerk van apoptose—en een verlaagde mitochondriale membraanpotentiaal. Ze vonden ook verhoogde niveaus van cytochroom c en de enzymen Caspase-3 en Caspase-9, klassieke componenten van de mitochondriale gedreven doodspad. Normale levercellen vertoonden daarentegen minder apoptose onder dezelfde CDC25C-verlagende omstandigheden.
Wat dit kan betekenen voor toekomstige behandelingen
Voor een niet-specialistische lezer is de kernboodschap dat het verlagen van CDC25C lijkt te mikken op de kwetsbaarheden van leverkankercellen: het overbelast hun energiecentrales, zet hun recyclingsystemen op volle toeren en veroorzaakt uiteindelijk nette zelfdestructie—terwijl normale levercellen grotendeels gespaard blijven. De auteurs concluderen dat CDC25C meer is dan een eenvoudige groeischakelaar; het bepaalt ook hoe cellen omgaan met stress, opruiming en dood. Omdat kankercellen sterk afhankelijk zijn van CDC25C en reageren op het verlies ervan met dodelijke mitochondriale stress en apoptose, zouden geneesmiddelen die dit eiwit of de downstream stressroutes targeten mogelijk op termijn een selectievere manier kunnen bieden om leverkanker te behandelen met minder schade aan gezond leverweefsel.
Bronvermelding: Miao, X., Zheng, F., Mo, X. et al. CDC25C downregulation suppresses HCC growth via mitochondrial stress-induced autophagy and apoptosis. Sci Rep 16, 5631 (2026). https://doi.org/10.1038/s41598-026-36351-2
Trefwoorden: hepatocellulair carcinoom, CDC25C, mitochondriale stress, autofagie, apoptose