Clear Sky Science · nl
TET1 remt de progressie van hepatocellulair carcinoom door modulatie van de PI3K/Akt-signaalroutes
Waarom een leverenzym van belang is bij kanker
Primaire leverkanker, met name een vorm die hepatocellulair carcinoom wordt genoemd, behoort tot de dodelijkste kankers wereldwijd. Veel patiënten worden te laat gediagnosticeerd voor een kuratieve operatie en bestaande geneesmiddelen helpen slechts een deel van hen. Deze studie onderzoekt een molecule genaamd TET1, een enzym dat chemische labels op DNA bewerkt, om een eenvoudige maar cruciale vraag te stellen: bevordert TET1 de groei van levertumoren, en zou het een nieuw behandeldoel kunnen worden?
Een verborgen redacteur in ons DNA
Onze genen worden niet alleen door de DNA-code zelf gereguleerd, maar ook door chemische merken die genen aan- of uitzetten. Een veelvoorkomend merkje is DNA-methylatie, dat fungeert als een dimmer op genactiviteit. TET1 maakt deel uit van een familie enzymen die deze merken wissen of herschikken, waardoor cellen op hun omgeving kunnen reageren en normale functies kunnen behouden. Wanneer dit systeem ontspoort, kunnen cellen in ziektetoestanden glijden, waaronder kanker. Eerder onderzoek liet zien dat TET1 tumorgroei afhankelijk van het weefsel zowel kan vertragen als versnellen, maar zijn precieze rol bij menselijke leverkanker bleef onduidelijk en fel bediscussieerd.
TET1-niveaus pieken in levertumoren
Om te achterhalen wat TET1 in leverkanker doet, raadpleegten de onderzoekers eerst grote openbare genendatabases en daarna patiëntmonsters. In meerdere kankersoorten waren TET1-niveaus ongewoon hoog in verschillende tumoren, waaronder leverkanker. Gericht op levertumoren vergeleken ze tumormateriaal met nabijgelegen niet-kankerachtig leverweefsel van dezelfde patiënten. In acht gematchte paren was TET1-eiwit consequent hoger in de tumor. Openbare datasets van honderden patiënten vertelden hetzelfde verhaal op RNA-niveau: leverkankers bevatten meer TET1 dan gezonde lever of lever met alleen littekenvorming. Patiënten van wie de tumoren hogere TET1-waarden toonden, hadden vaker een gevorderd ziektebeeld en kortere algehele en ziektevrije overleving, wat suggereert dat TET1 samenhangt met zowel tumoragressiviteit als een slechtere prognose.
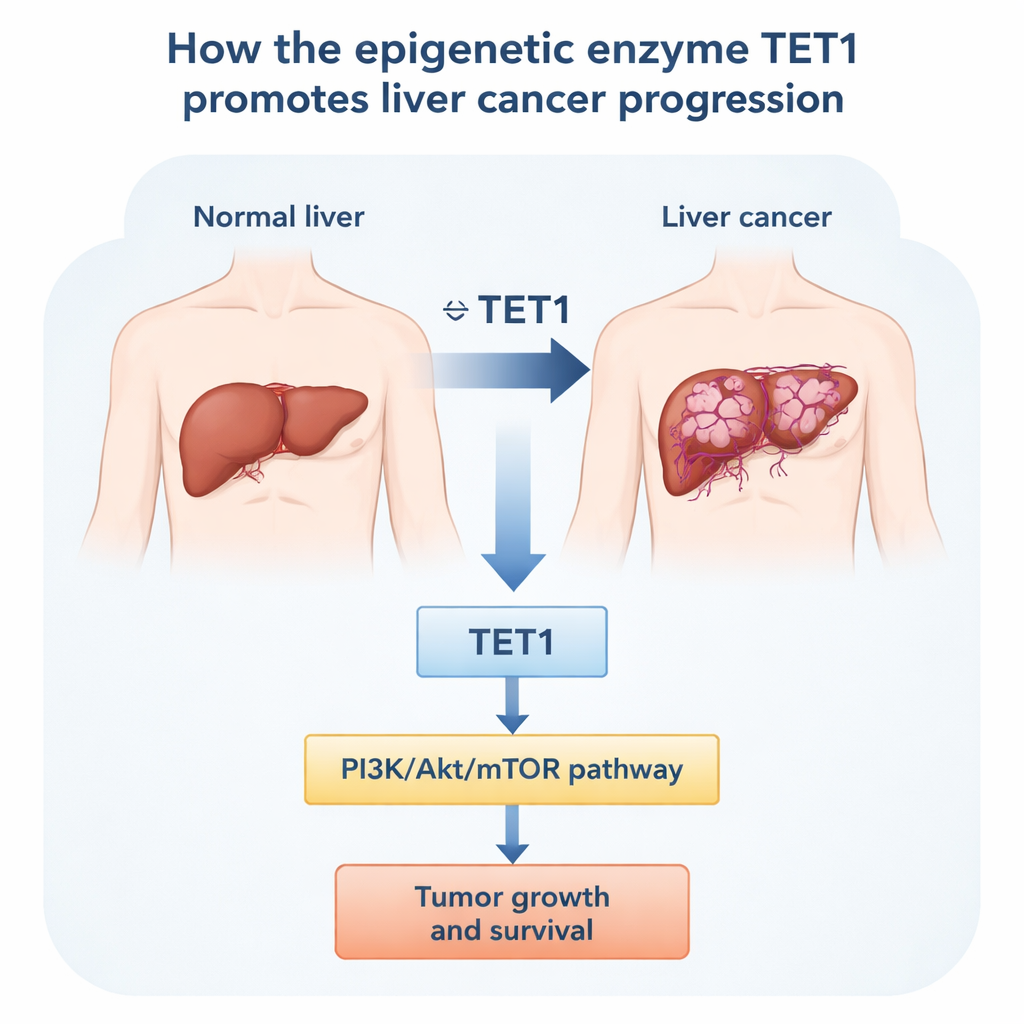
Het terugdraaien van TET1 vertraagt tumorcellen
Vervolgens vroegen de onderzoekers wat er gebeurt als TET1 in leverkankercellen die in het laboratorium gekweekt worden, naar beneden wordt gebracht. Met kleine stukjes RNA om het TET1-gen te onderdrukken, reduceerden ze TET1-niveaus drastisch in meerdere menselijke leverkankercellijnen, inclusief lijnen met hepatitis B-virusgerelateerde veranderingen. Zodra TET1 werd onderdrukt, deelden de cellen zich langzamer, vormden ze minder kolonies en vertoonden ze duidelijke stresssignalen. Flowcytometrie-experimenten lieten zien dat meer cellen vastliepen in de vroege G1-fase van de celcyclus in plaats van door te gaan naar celdeling. Tegelijkertijd nam het aandeel cellen dat geprogrammeerde celdood (apoptose) onderging sterk toe. Deze effecten traden op in zowel typische leverkankercellen als in een HBV-positieve lijn, wat aangeeft dat TET1 bijdraagt aan het in stand houden van overleving en voortdurende groei in verschillende contexten van leverkanker.
Een groeipad onder controle van TET1
Om te ontdekken hoe TET1 deze invloed uitoefent, bepaalden de onderzoekers welke genen verschilden tussen normale levercellen en kankercellen. Duizenden genen waren anders, en velen groepeerden zich in bekende groeien overlevingsroutes. Één route stak er bovenuit: PI3K/Akt/mTOR, een centraal signaaltraject dat veel cancers gebruiken om hun metabolisme op te voeren, apoptose te weerstaan en therapieën te ontlopen. Databaseanalyses toonden dat TET1-niveaus parallel opliepen met kerncomponenten van dit traject en tegenovergesteld waren aan PTEN, een natuurlijke rem op PI3K/Akt-activiteit. Toen TET1 in leverkankercellen werd stilgelegd, daalden de geactiveerde, gefosforyleerde vormen van PI3K, Akt en vooral mTOR. Behandeling van cellen met een chemische remmer die de activiteit van TET-familie-enzymen blokkeert, verminderde evenzo de fosforylering van Akt en mTOR. Deze resultaten suggereren dat de enzymatische activiteit van TET1 — zijn vermogen om DNA-merken te herschikken — inwerkt op de PI3K/Akt/mTOR-cascade en zo de balans kantelt richting groei en overleving in plaats van remming.
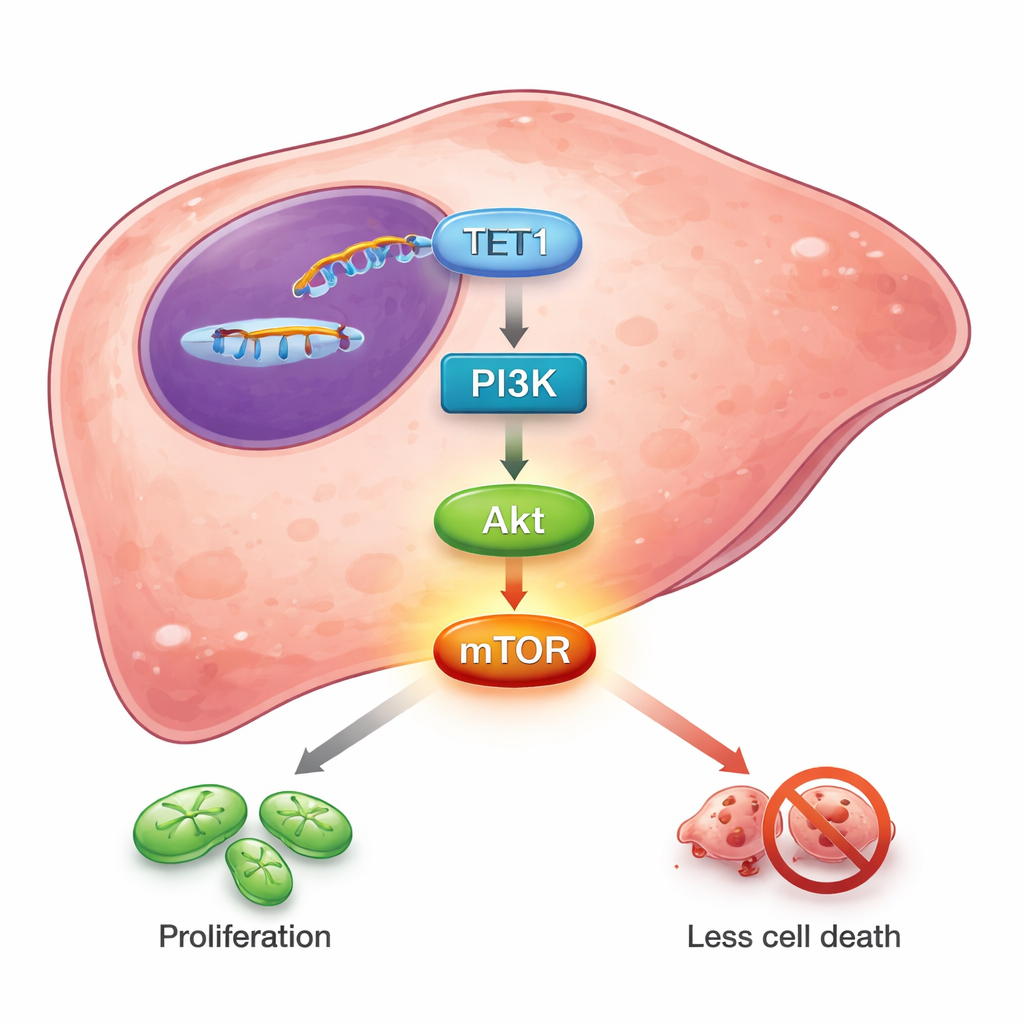
Van moleculair inzicht naar mogelijke behandelingen
Gezamenlijk schetst dit werk TET1 als een belangrijke bondgenoot van levertumoren in plaats van als een beschermer ertegen. Hoog TET1 helpt leverkankercellen prolifereren en apoptose te vermijden, deels door het PI3K/Akt/mTOR-pad ingeschakeld te houden. Bij patiënten gaat meer TET1 in tumoren hand in hand met gevorderde ziekte en slechtere uitkomsten. Voor de lezer zonder medische achtergrond is de boodschap dat een enzym dat stilletjes chemische labels op DNA bewerkt, sterk kan bepalen of leverkankercellen overleven of sterven. Door geneesmiddelen te ontwerpen die TET1 remmen, of door zulke middelen te combineren met bestaande therapieën gericht op PI3K/Akt, zouden toekomstige behandelingen een cruciale ondersteuningslijn voor levertumoren kunnen doorknippen en de overleving van mensen met deze uitdagende ziekte kunnen verbeteren.
Bronvermelding: Qi, S., Chen, M., Ding, Z. et al. TET1 suppresses hepatocellular carcinoma progression by modulating the PI3K/Akt signaling pathways. Sci Rep 16, 5791 (2026). https://doi.org/10.1038/s41598-026-36334-3
Trefwoorden: leverkanker, TET1, epigenetica, PI3K Akt mTOR, hepatocellulair carcinoom