Clear Sky Science · nl
Fecale microbiota voorspelt behandelrespons na start van semaglutide of empagliflozine
Waarom uw darmbacteriën de diabetesbehandeling kunnen beïnvloeden
Mensen met type 2 diabetes krijgen steeds vaker nieuwere middelen zoals semaglutide (vaak bekend van reclame voor gewichtsverlies) en empagliflozine, die helpen de bloedsuiker en het lichaamsgewicht te verlagen. Niet iedereen reageert echter even goed. Deze studie stelt een eenvoudige maar krachtige vraag: kunnen de biljoenen bacteriën in ons darmkanaal helpen verklaren wie het meest profiteert van deze medicijnen, en zouden ze ooit kunnen helpen bij meer gepersonaliseerde diabeteszorg?
Wat er precies werd onderzocht en gemeten
Onderzoekers volgden 20 volwassenen met type 2 diabetes die al metformine gebruikten en obesitas hadden. Hun artsen voegden op medische indicatie ofwel semaglutide ofwel empagliflozine toe. Gedurende een heel jaar leverden deelnemers vier keer ontlastingsmonsters en drie keer bloed- en urinemonsters aan. De ontlastingsmonsters werden gebruikt om het darmmicrobioom te profilen, terwijl de bloed- en urinetests belangrijke gezondheidsmarkers volgden zoals langetermijnbloedsuiker (HbA1c), lichaamsgewicht, nierfunctie en signalen van ontsteking. Dit ontwerp maakte het mogelijk zowel te zien hoe de medicijnen de gezondheid beïnvloedden als of het beginnende darmmicrobioom die veranderingen kon voorspellen. 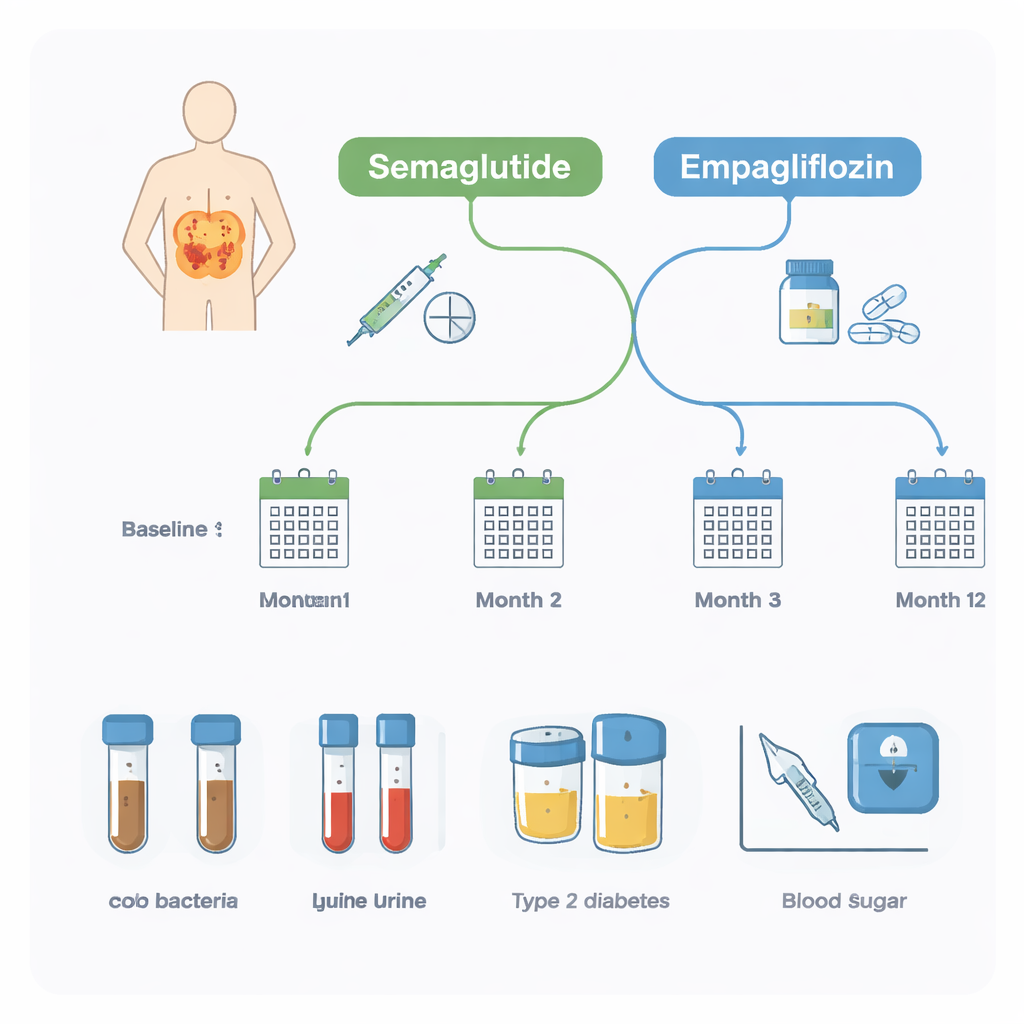
Hoe de medicijnen gezondheid en darmgemeenschappen beïnvloedden
Klinisch verbeterden beide geneesmiddelen de bloedsuikercontrole al in de derde maand van behandeling, en semaglutide leidde in het bijzonder tot duidelijke en blijvende gewichtsafname over 12 maanden. Toen het team naar de diversiteit van darmbacteriën keek — hoeveel verschillende typen aanwezig waren en hoe gelijkmatig ze verdeeld waren — zagen ze geen duidelijke algemene verschuiving na de start van een van beide geneesmiddelen. Evenmin bleven de meeste schijnbare veranderingen in brede patronen van bacteriegroepen statistisch robuust nadat strikte correcties voor meervoudige testen werden toegepast. Sommige bacteriegroepen en voorspelde metabolische paden leken te veranderen tussen maand 3 en 12, maar die patronen waren bescheiden en weerspiegelden waarschijnlijk indirecte effecten van verbeterde stofwisseling of veranderde levensstijl in plaats van een direct effect van de medicijnen zelf.
Darmbacteriën als potentiële voorspellers van succes
De meest intrigerende bevindingen kwamen voort uit het bekijken van het microbioom vóór de behandeling en de vraag of dit kon voorspellen wie het meest zou verbeteren. Bij mensen die semaglutide kregen, liet honderden baseline-microbiële kenmerken nominale verbanden zien met latere veranderingen in klinische markers, vooral witte bloedcellen en een maat voor ontsteking die bekendstaat als de neutrofiel-tot-lymfocyten-ratio. Na strikte statistische filtering bleef één bacteriegroep genaamd Alistipes significant geassocieerd: individuen met meer van deze bacterie bij aanvang hadden de neiging een grotere daling van ontstekingscellen te vertonen. Verschillende bacteriegenera en microbiële paden bij aanvang correleerden ook met hoeveel HbA1c tegen de derde maand daalde, wat suggereert dat de beginnende darmgemeenschap kan beïnvloeden hoe sterk semaglutide de bloedsuiker verlaagt. In de empagliflozine-groep hadden ook tal van bacteriën en paden verbanden met veranderingen in HbA1c en maatstaven voor nierfunctie, maar geen van die verbanden doorstond de meest conservatieve statistische toetsen, deels omdat de studie klein was.
Wat de bevindingen wel en niet betekenen
Belangrijk is dat dit werk niet beweert dat semaglutide of empagliflozine op zichzelf het darmmicrobioom dramatisch herstructureren, noch dat een specifieke bacterie succes of falen garandeert. Het suggereert eerder dat subtiele kenmerken van iemands bestaande darmgemeenschap mogelijk gekoppeld zijn aan hoe het lichaam reageert — niet alleen qua bloedsuiker maar ook qua ontsteking en andere gezondheidsmarkers. Omdat alle deelnemers al metformine gebruikten, wat zelf effect heeft op darmbacteriën, kan een extra invloed van de nieuwere medicijnen moeilijker te detecteren zijn geweest. De bescheiden steekproefgrootte en enkele ontbrekende monsters beperken bovendien hoe zeker individuele bacteriegroepen als echte drijfveren van medicijnrespons kunnen worden aangewezen.
Vooruitblik naar gepersonaliseerde diabeteszorg
Voor een niet-specialist is de kernboodschap dat uw darmbacteriën op een dag artsen kunnen helpen het diabetesmiddel te kiezen dat het beste voor u werkt. In deze vroege studie was de samenstelling van microben in ontlastingsmonsters die voor de behandeling werden genomen gekoppeld aan hoe sterk semaglutide en empagliflozine bloedsuiker en ontsteking verbeterden, terwijl de medicijnen zelf slechts subtiele, langzame verschuivingen in darmgemeenschappen veroorzaakten. Grotere, langere studies zijn nodig om te bevestigen welke microben echt van belang zijn en of het veranderen daarvan de behandelingswerking kan versterken. Als die inspanningen slagen, zou een eenvoudige ontlastingstest deel kunnen uitmaken van gepersonaliseerde diabeteszorg en helpen het juiste medicijn bij het juiste microbioom te passen. 
Bronvermelding: Klemets, A., Reppo, I., Krigul, K.L. et al. Fecal microbiome predicts treatment response after the initiation of semaglutide or empagliflozin uptake. Sci Rep 16, 6126 (2026). https://doi.org/10.1038/s41598-026-36318-3
Trefwoorden: darmmicrobioom, type 2 diabetes, semaglutide, empagliflozine, gepersonaliseerde geneeskunde