Clear Sky Science · nl
Fenomenen rond Candida albicans-biofilmresistentie ontrafelen via azool–sophorolipide-synergie
Waarom hardnekkige schimmelinfecties ertoe doen
Iemand die ooit een aanhoudende gistinfectie heeft gehad, een centraal infuus in het ziekenhuis draagt of een medisch implantaat heeft gekregen, loopt mogelijk risico op infectie door Candida albicans — een veelvoorkomende schimmel die gevaarlijk kan worden als ze zich organiseert in moeilijk te behandelen gemeenschappen, de zogenoemde biofilms. Deze slijmerige laagjes beschermen de microben tegen veel van onze beste antischimmelmiddelen, waardoor infecties kunnen aanhouden en soms levensbedreigend worden. De hier beschreven studie zoekt naar een nieuwe manier om die verdediging te doorbreken door bestaande medicijnen te combineren met een natuurlijke, zeepachtige molecule die door gist wordt geproduceerd.
Een verborgen schild op medische oppervlakken
Candida albicans kan zich hechten aan weefsels en medische apparaten en zich vervolgens ophopen tot gestructureerde biofilms — dichte cel-lagen samengehouden door een zelfgemaakte matrix van suikers, eiwitten en DNA. Binnen dit bolwerk verlaagt de schimmel haar stofwisseling en pompt ze medicijnen weer naar buiten, waardoor middelen die vrij rondzwemmende cellen gemakkelijk doden, biofilmcellen nauwelijks raken. Azoolmiddelen zoals fluconazol en itraconazol vormen een hoeksteen van de antischimmeltherapie, maar tegen rijpe biofilms zijn vaak veel hogere doseringen nodig, wat bijwerkingen kan veroorzaken en toch niet altijd tot volledige uitroeiing leidt. Klinische teams staan steeds vaker voor infecties die zowel biofilm-gerelateerd als resistent zijn, wat de noodzaak benadrukt voor hulpstoffen die de biofilm zelf kunnen verzwakken.
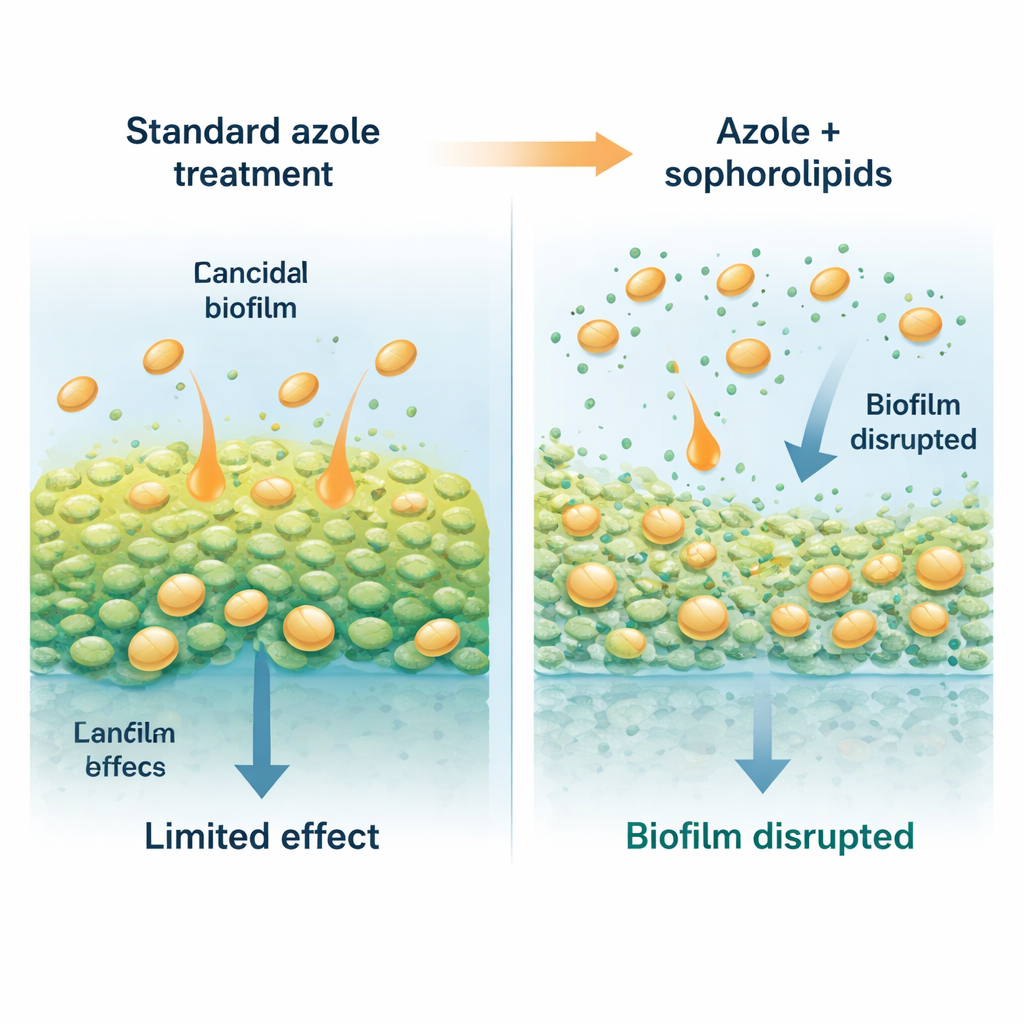
Zeepachtige helpers van een vriendelijke gist
De onderzoekers richtten zich op sophorolipiden: natuurlijke, biologisch afbreekbare oppervlakteactieve stoffen — moleculen die zich een beetje gedragen als zeer milde detergenten — geproduceerd door bepaalde niet-pathogene gisten. Deze moleculen hebben een waterminnende suikerkop en een vettige staart, waardoor ze zich op oppervlakken en grensvlakken nestelen. In deze studie werd de gist Starmerella riodocensis gebruikt om een mengsel van sophorolipiden te produceren, dat vervolgens werd gezuiverd en geanalyseerd. Op zichzelf doodden deze sophorolipiden geen vrij zwevende Candida-cellen, zelfs niet bij hoge doses, maar ze verstoorden sterk het vermogen van de schimmel om biofilms te vormen en in stand te houden. Jonge, net gevormde biofilms waren bijzonder gevoelig, en zelfs gevestigde 24 uur oude biofilms konden worden verdund en verzwakt na blootstelling aan gezuiverde sophorolipiden.
Samenwerking met bestaande antischimmelmiddelen
De centrale vraag was of sophorolipiden standaard azoolmiddelen effectiever konden maken. Het team testte combinaties van sophorolipiden met drie veelgebruikte azolen: fluconazol, itraconazol en ketoconazol. Bij blootstelling van biofilms aan deze mengsels bleek dat sommige combinaties meer deden dan hun afzonderlijke effecten optellen — ze werkten synergistisch, wat betekent dat de combinatie krachtiger was dan verwacht op basis van elk component alleen. De opvallende combinatie was itraconazol plus sophorolipiden. Tegen hardnekkige, reeds gevormde biofilms daalde de hoeveelheid itraconazol die nodig was om de biofilm voor de helft te verminderen tot wel zestien keer minder, terwijl de vereiste sophorolipidendosis ook meerdere keren lager was vergeleken met het gebruik van sophorolipiden alleen. Combinaties met fluconazol en ketoconazol lieten meer bescheiden winst zien, wat aangeeft dat de chemische aard van elk middel bepaalt in welke mate het profiteert van de oppervlakteactieve "assistent".
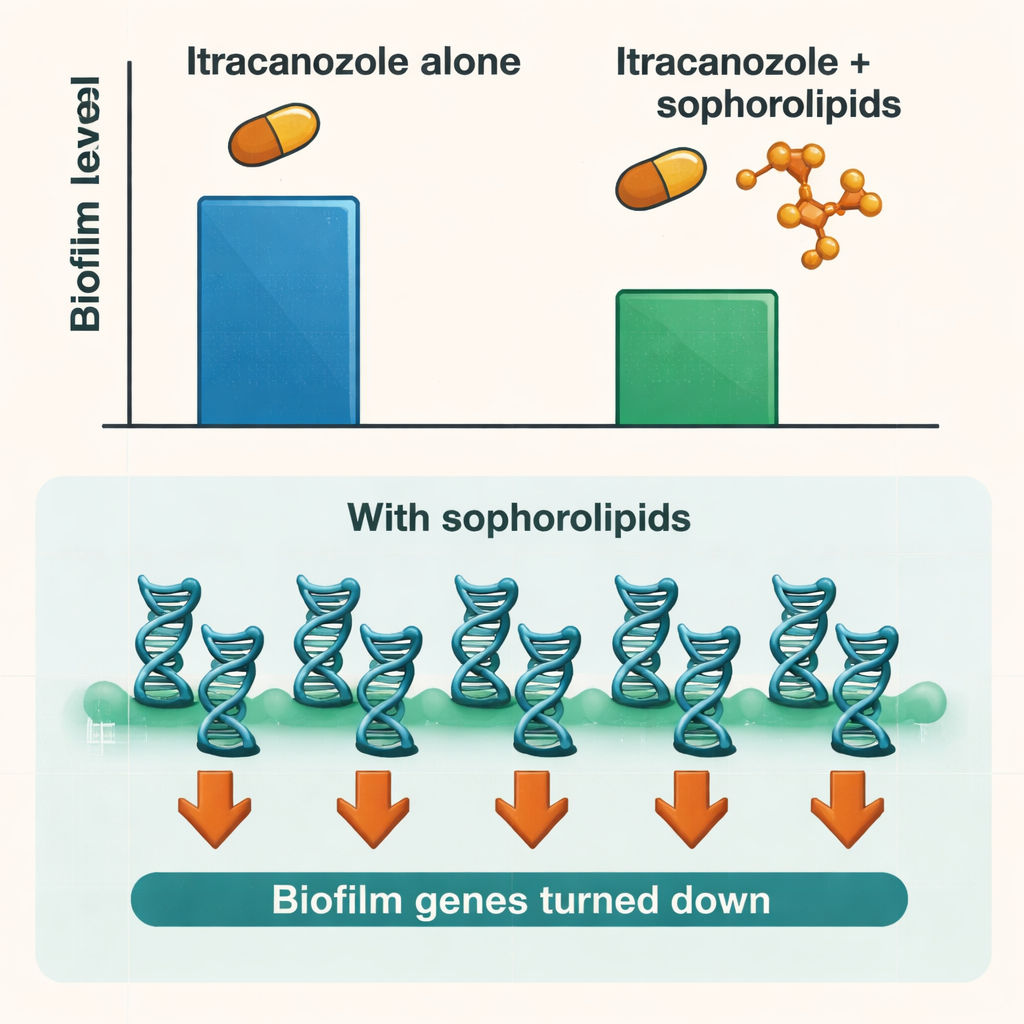
Het stilleggen van het biofilmprogramma van de schimmel
Om te begrijpen wat er in de schimmelcellen gebeurde, onderzochten de onderzoekers de activiteit van sleutelgenen van Candida die betrokken zijn bij hechting aan oppervlakken, groei als filamenten en opbouw van de biofilmmatrix. Behandeling met alleen sophorolipiden zette veel van deze genen naar beneden, met name die welke de vroegste adhesiestappen en de overgang van gistachtige naar filamentvormen reguleren. Wanneer cellen werden gesynchroniseerd in een specifieke fase van de celcyclus die biofilmvorming bevordert, waren de genonderdrukkende effecten nog sterker. Dit duidt erop dat sophorolipiden niet eenvoudigweg de biofilm wegwassen; ze verstoren ook het biologische programma van de schimmel voor het bouwen en onderhouden van haar beschermende gemeenschap.
Belofte voor zachtere, effectievere behandelingen
De studie concludeert dat sophorolipiden uit Starmerella riodocensis kunnen fungeren als veilige, biofilmgerichte partners voor azoolmiddelen, waarbij de combinatie itraconazol–sophorolipiden bijzonder krachtig is. Omdat sophorolipiden een lage toxiciteit in zoogdiercellen laten zien en vooral de biofilmstructuur en bijbehorende gen-netwerken verzwakken in plaats van de schimmel direct te vergiftigen, zouden ze artsen in staat kunnen stellen lagere doses conventionele middelen te gebruiken en toch hardnekkige infecties op apparaten en weefsels te verdrijven. Voor patiënten zou dit soort slimme combinatietherapie in de toekomst kunnen leiden tot behandelingen die zowel effectiever zijn tegen resistente Candida-biofilms als vriendelijker voor de rest van het lichaam.
Bronvermelding: Jayasekara, L.C.B., Watchaputi, K., Butkinaree, C. et al. Overcoming Candida albicans biofilm drug resistance via azole-sophorolipid synergy. Sci Rep 16, 5963 (2026). https://doi.org/10.1038/s41598-026-36278-8
Trefwoorden: Candida-biofilm, azool-antischimmelmiddelen, sophorolipiden, medicijnsynergie, antimicrobiële resistentie