Clear Sky Science · nl
Machine learning dat MRI en klinische kenmerken integreert voorspelt vroege terugkeer van hepatocellulair carcinoom na resectie
Waarom vroege terugkeer van kanker ertoe doet
Voor mensen die een operatie ondergaan om leverkanker te verwijderen, is een van de grootste zorgen of de ziekte snel weer terugkomt. Vroege terugkeer van hepatocellulair carcinoom — de meest voorkomende vorm van primaire leverkanker — duidt vaak op een agressieve tumor en een slechtere overleving. Artsen willen bij voorkeur al vóór de operatie weten welke patiënten de grootste kans hebben op een vroege recidief, zodat ze vervolgonderzoek en aanvullende behandelingen kunnen afstemmen. Deze studie onderzoekt of kunstmatige intelligentie (AI) routinematige bloedtests, MRI-scans en weefselbevindingen kan combineren om dat vroege waarschuwingssignaal te geven.
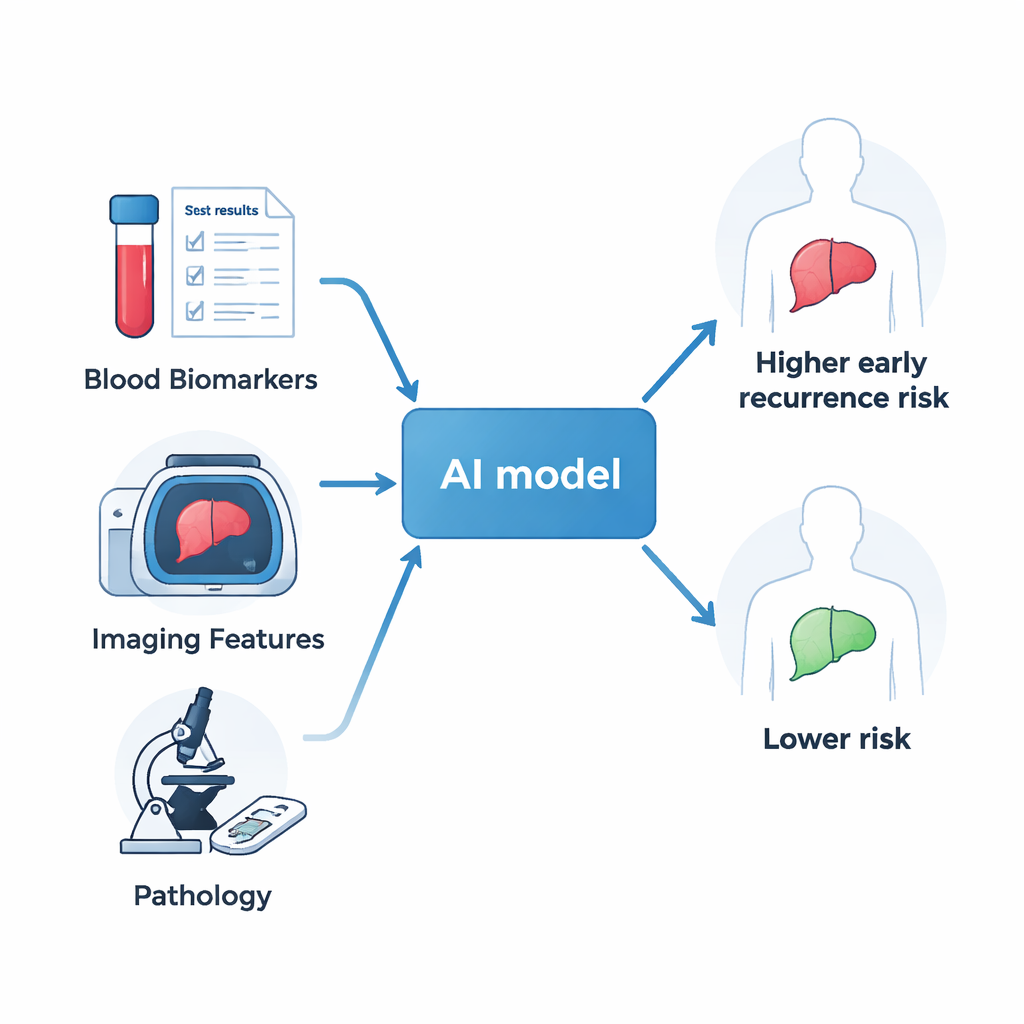
Verschillende aanwijzingen samenbrengen
De onderzoekers analyseerden 240 patiënten met leverkanker die een operatie ondergingen in twee ziekenhuizen in China. Voor hun ingrepen ondergingen alle patiënten standaard contrastversterkte MRI-scans en gangbare bloedonderzoeken, en na de operatie werden hun tumoren onder de microscoop onderzocht. In plaats van één factor tegelijk te bekijken — zoals tumorgrootte of een enkele bloedparameter — voerde het team tientallen van deze metingen in machine-learning-algoritmen. Deze AI-methoden zijn ontworpen om complexe patronen en interacties te herkennen die traditionele statistische technieken mogelijk missen, vooral wanneer de relaties niet eenvoudig zijn als “groter is slechter” of “hoger is beter.”
Hoe de AI-modellen werden opgebouwd
Om het systeem niet te overladen, verkleinden de onderzoekers eerst de lange lijst van kandidaatkenmerken. Ze verwijderden metingen die bijna duplicaten van elkaar waren en gebruikten vervolgens een statistische techniek genaamd LASSO om 14 van de meest informatieve factoren te selecteren. Met deze factoren trainden ze meerdere boomgebaseerde machine-learning-modellen — ExtraTrees, XGBoost, LightGBM en GradientBoosting — om te voorspellen of een patiënt binnen twee jaar na de operatie een recidief zou krijgen. De modellen werden afgestemd op gegevens uit één ziekenhuis en vervolgens getest op een onafhankelijke groep patiënten uit het tweede ziekenhuis, een zwaardere toets die de realistische toepassing beter weerspiegelt.
Hoe goed de modellen presteerden
Drie van de AI-modellen — ExtraTrees, XGBoost en LightGBM — lieten een sterke capaciteit zien om te onderscheiden tussen patiënten met en zonder vroege recidief. In de trainingsgroep varieerden hun prestatiewaarden (gemeten met de oppervlakte onder de ROC-curve, of AUC) van ongeveer 0,82 tot 0,98, waarbij 1,0 perfect is en 0,5 niet beter dan toeval. In de externe testgroep waren de AUC’s iets lager, rond 0,76 tot 0,79, maar ze wezen nog steeds op nuttige voorspellende kracht. Decision-curve-analyse, een methode die inschat of een model artsen daadwerkelijk zou helpen betere beslissingen te nemen, suggereerde dat het gebruik van deze AI-hulpmiddelen meer voordeel kan bieden dan alle patiënten op dezelfde manier behandelen of vertrouwen op toeval. Over het geheel genomen leken de modellen redelijk nauwkeurig en klinisch betekenisvol.
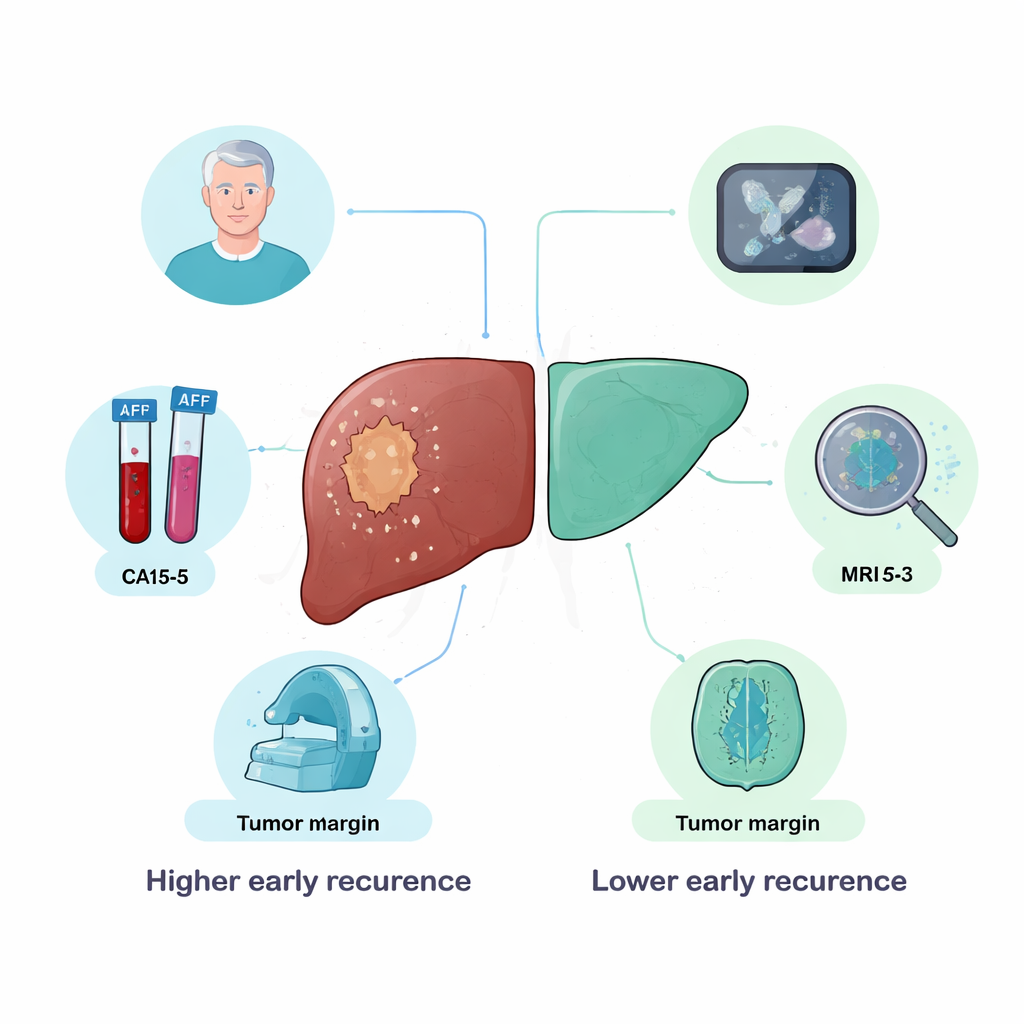
Wat de voorspellingen aanstuurt
Door te onderzoeken op welke invoer de modellen het meest vertrouwden, geeft de studie inzicht in wat belangrijk lijkt voor vroeg recidief. Twee bloedmarkers — AFP, al lang gebruikt in de zorg voor leverkanker, en CA15-3, bekender uit de borstkankerzorg — behoorden consequent tot de meest invloedrijke kenmerken. MRI-tekenen van een onregelmatige, niet-gladde tumorrand waren sterk verbonden met vroege terugkeer, wat eerdere bevindingen weerspiegelt die gekartelde tumorranden koppelen aan invasiever gedrag en verborgen verspreiding binnen de lever. Leeftijd speelde ook een rol, waarbij jongere patiënten verrassend genoeg een grotere kans op vroege recidief hadden, waarschijnlijk doordat tumoren in deze groep biologisch agressiever zijn. Microscopische kenmerken zoals kleine clusters kankercellen in kleine bloedvaten ondersteunden daarnaast de risicoschattingen van de AI.
Wat dit betekent voor patiënten en artsen
Voor iemand die voor een leveroperatie staat, vervangen de in deze studie beschreven modellen niet het oordeel van een arts, maar ze kunnen een extra laag van begeleiding bieden. Door informatie te combineren die al in de routinezorg wordt verzameld — bloedtesten, MRI-bevindingen en standaard pathologie — kunnen de AI-instrumenten patiënten met een hoger risico op vroege terugkeer signaleren. Die personen zouden kunnen profiteren van dichter beeldvormend vervolgonderzoek, frequentere bloedcontroles of overweging van aanvullende behandelingen na de operatie. Omdat de studie retrospectief is en beperkt tot twee centra in één regio, benadrukken de auteurs dat grotere, prospectieve onderzoeken nodig zijn voordat dergelijke modellen standaard worden. Toch wijst het werk op een toekomst waarin AI artsen helpt surveillance en therapie te personaliseren, met als doel terugkerende leverkanker vroeger op te sporen en de langetermijnuitkomsten te verbeteren.
Bronvermelding: Feng, L., Luo, N., Ruan, F. et al. Machine learning integrating MRI and clinical features predicts early recurrence of hepatocellular carcinoma after resection. Sci Rep 16, 5653 (2026). https://doi.org/10.1038/s41598-026-36261-3
Trefwoorden: leverkanker, machine learning, MRI, tumorrecidief, bloedomarkers