Clear Sky Science · nl
Zwak-gesuperviseerde segmentatie van colorectale klieren via zelf-gesuperviseerd leren en aandacht-gebaseerde pseudo-labeling
Waarom dit belangrijk is voor kankerdiagnose
Wanneer een patholoog een colonbiopsie onder de microscoop bekijkt, is een van de belangrijkste aanwijzingen voor de ernst van kanker de vorm en organisatie van kleine buisachtige structuren, klieren genoemd. Het met de hand zorgvuldig omlijnen van elke klier is traag, duur en moeilijk te standaardiseren tussen ziekenhuizen. Deze studie toont aan hoe kunstmatige intelligentie kan leren deze klieren bijna zo goed als menselijke experts te traceren, terwijl veel minder gedetailleerde menselijke annotaties nodig zijn, wat mogelijk de diagnose van colorectale kanker kan versnellen en verfijnen.
De uitdaging van elk klein omtrekje tekenen
Colorectale kanker behoort tot de meest voorkomende en dodelijke vormen van kanker wereldwijd, en de gradatie van de ernst hangt sterk af van het uiterlijk van klieren. In gezond of vroeg stadium weefsel zien klieren eruit als nette, ronde buisjes; in agressieve tumoren worden ze gekarteld, versmolten of nauwelijks herkenbaar. Computers kunnen worden getraind om elke klier te segmenteren, oftewel "inkleuren", zodat automatische metingen mogelijk worden, maar traditionele deep-learning systemen vereisen arbeidsintensieve pixel-voor-pixel omlijningen door deskundige pathologen. In klinische praktijk zijn veel eenvoudiger verkrijgbare labels afbeeldingsniveau-etiketten, zoals of een weefseltegel wel of geen klieren bevat, of dat het goedaardig of kwaadaardig is.
Een AI trainen met ongeëtiketteerde en zwak geëtiketteerde slides
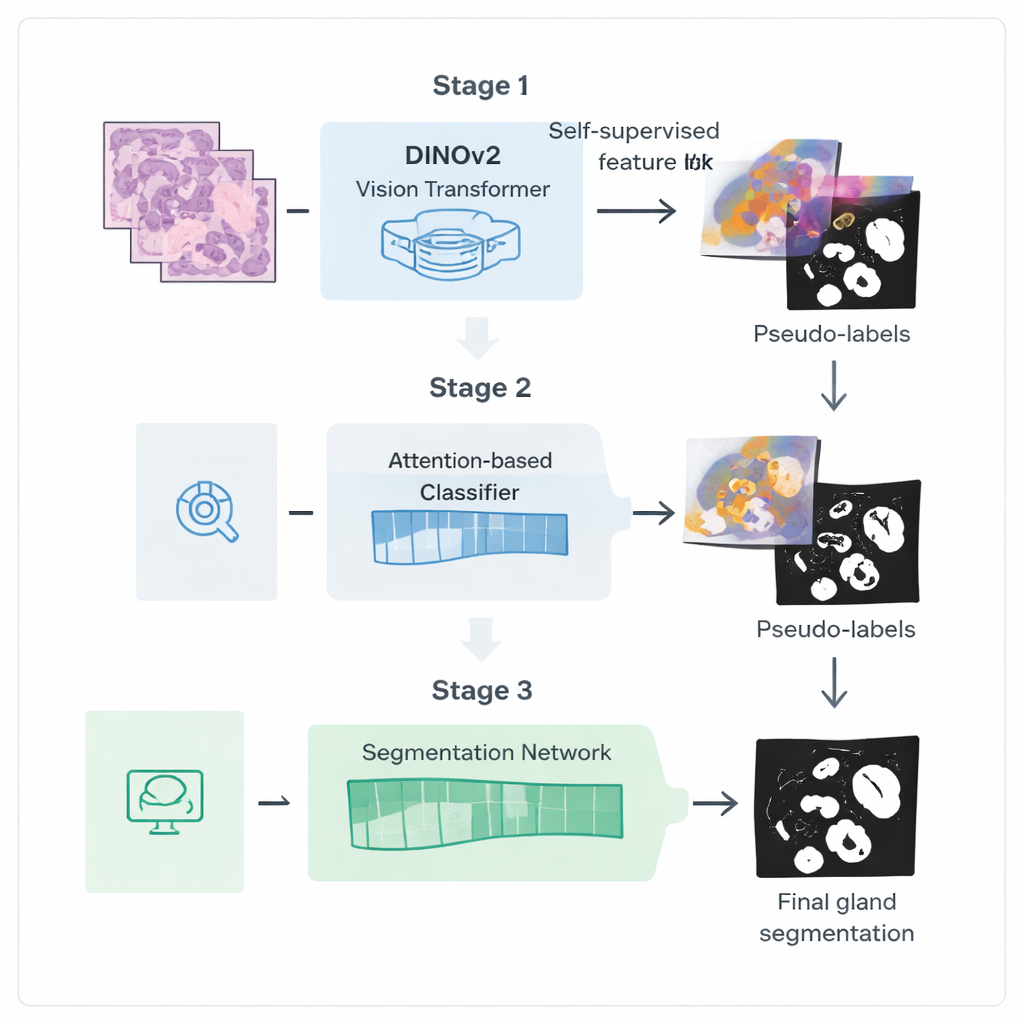
De auteurs introduceren een driedelig trainingsproces dat is ontworpen om meer waarde uit deze zwakkere labels te halen. Eerst beginnen ze met een krachtig vision-model genaamd DINOv2, oorspronkelijk getraind op natuurlijke foto’s, en stellen het bloot aan duizenden ongeëtiketteerde colorectale biopsiebeelden. Door het model verschillende aanzichten van dezelfde weefselpatch op elkaar te laten afstemmen, leert het visuele kenmerken die zijn afgestemd op de kleuren en texturen van histologische slijpen zonder annotaties. Deze stap creëert een gespecialiseerd "encoder" die ruwe beelden omzet in rijke interne representaties die klierachtige structuren vastleggen.
De AI laten zien waar hij naar kijkt
In de tweede fase wordt deze encoder aangesloten op een classificatienetwerk dat alleen afbeeldingsniveau-etiketten nodig heeft, zoals of klieren aanwezig zijn. Een aandachtmechanisme in het netwerk leert hogere gewichten toe te kennen aan de beeldregio’s die het meest van belang zijn voor de beslissing. Deze aandachtkaarten markeren effectief waar het netwerk "gelooft" dat klieren zich bevinden. De onderzoekers zetten deze zachte hittekaarten om in ruwe binaire maskers via mengen en drempelwaardes, en maken ze vervolgens verder schoon met een probabilistische gladstrijktechniek genaamd een Conditional Random Field. Het resultaat is een set verfijnde pseudo-labels: door de computer gegenereerde klieromtrekken die niet perfect zijn, maar goed genoeg om een meer gespecialiseerd segmentatiemodel te sturen.
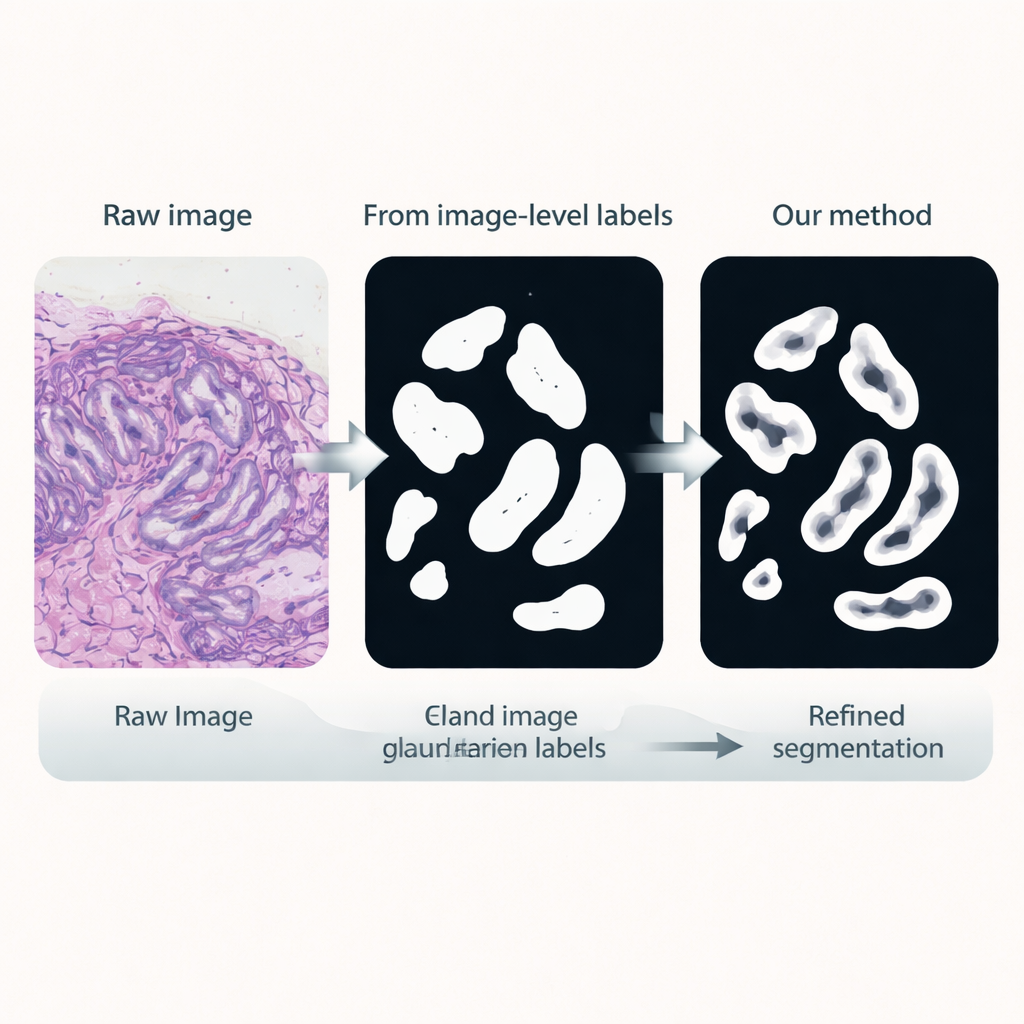
Verscherpen van kliergrenzen
In de derde fase wordt een speciaal segmentatienetwerk getraind met deze pseudo-labels als plaatsvervangers voor handmatige annotaties. Het hergebruikt de fijn-afgestemde encoder maar voegt een lichtgewicht decoder-kop toe die kenmerken omzet in een gedetailleerd kliermasker. Cruciaal is dat de verliesfunctie tijdens training extra aandacht besteedt aan randen: fouten die de klierkanten vervormen worden zwaarder bestraft dan kleine fouten in het interieur. Deze rand-bewuste training stimuleert scherpe, anatomisch realistische omtrekken, die essentieel zijn voor het nauwkeurig meten van kliervorm en scheiding.
Hoe goed werkt het in de praktijk?
Het team testte hun methode op twee standaarddatasets van colorectaal weefsel. Op de GlaS-dataset versloeg hun zwak-gesuperviseerde aanpak niet alleen andere methoden die ook beperkte labels gebruiken, maar in meerdere maatstaven benaderde of overtrof hij klassieke volledig-gesuperviseerde systemen die afhankelijk waren van volledige pixelniveau-annotaties. Op een moeilijkere dataset genaamd CRAG, gevuld met sterk onregelmatige, kwaadaardige klieren, daalde de prestaties voor alle methoden, maar het nieuwe raamwerk presteerde nog steeds beter dan andere zwak-label concurrenten en verkleinde de kloof met volledig-gesuperviseerde modellen. Ablatiestudies toonden aan dat elk component—zelf-gesuperviseerd fijn-afstemmen, aandacht-gebaseerde pseudo-labeling met nabehandeling, en rand-bewuste verliesfunctie—zinvol bijdroeg aan de verbeteringen.
Wat dit betekent voor toekomstige pathologietools
Voor een niet-specialistische lezer is de belangrijkste conclusie dat dit werk wijst op AI-systemen die hoogwaardige, rand-precieze kaarten van microscopische klierstructuren kunnen leveren terwijl ze hoofdzakelijk vertrouwen op eenvoudige slide-niveau-etiketten die al gebruikelijk zijn in ziekenhuisarchieven. Door de afhankelijkheid van tijdrovende handmatige omlijningen te verminderen, zou de aanpak geavanceerde beeldgebaseerde gradatie en kwantitatieve analyse gemakkelijker uitvoerbaar kunnen maken in veel centra, waardoor pathologen colorectale kanker consistenter en efficiënter kunnen diagnosticeren, en mogelijk toepasbaar op andere weefseltypen en structuren in de toekomst.
Bronvermelding: Wen, H., Wu, Y., Huang, D. et al. Weakly supervised colorectal gland segmentation through self-supervised learning and attention-based pseudo-labeling. Sci Rep 16, 5771 (2026). https://doi.org/10.1038/s41598-026-36256-0
Trefwoorden: colorectale kanker, digitale pathologie, kliersegmentatie, zwak-gesuperviseerd leren, zelf-gesuperviseerd vision