Clear Sky Science · nl
Herbestemming van dapagliflozine via polymeer-nanogels voor de behandeling van colorectale kanker
Waarom een middel tegen diabetes kan helpen bij de bestrijding van darmkanker
Colorectale kanker is een van de belangrijkste oorzaken van kankergerelateerde sterfte wereldwijd, en veel patiënten krijgen toch weer terugval ondanks operatie en chemotherapie. Deze studie onderzoekt een onverwachte bondgenoot tegen deze ziekte: dapagliflozine, een veelgebruikt middel voor type 2 diabetes. Door dit middel in zeer kleine, zachte deeltjes te verpakken die in de maag veranderen in een zachte gel, proberen de onderzoekers meer van het middel naar de dikke darm te brengen — waar colongezwellen ontstaan — terwijl de orale dosis vergelijkbaar blijft met bestaande tabletten.
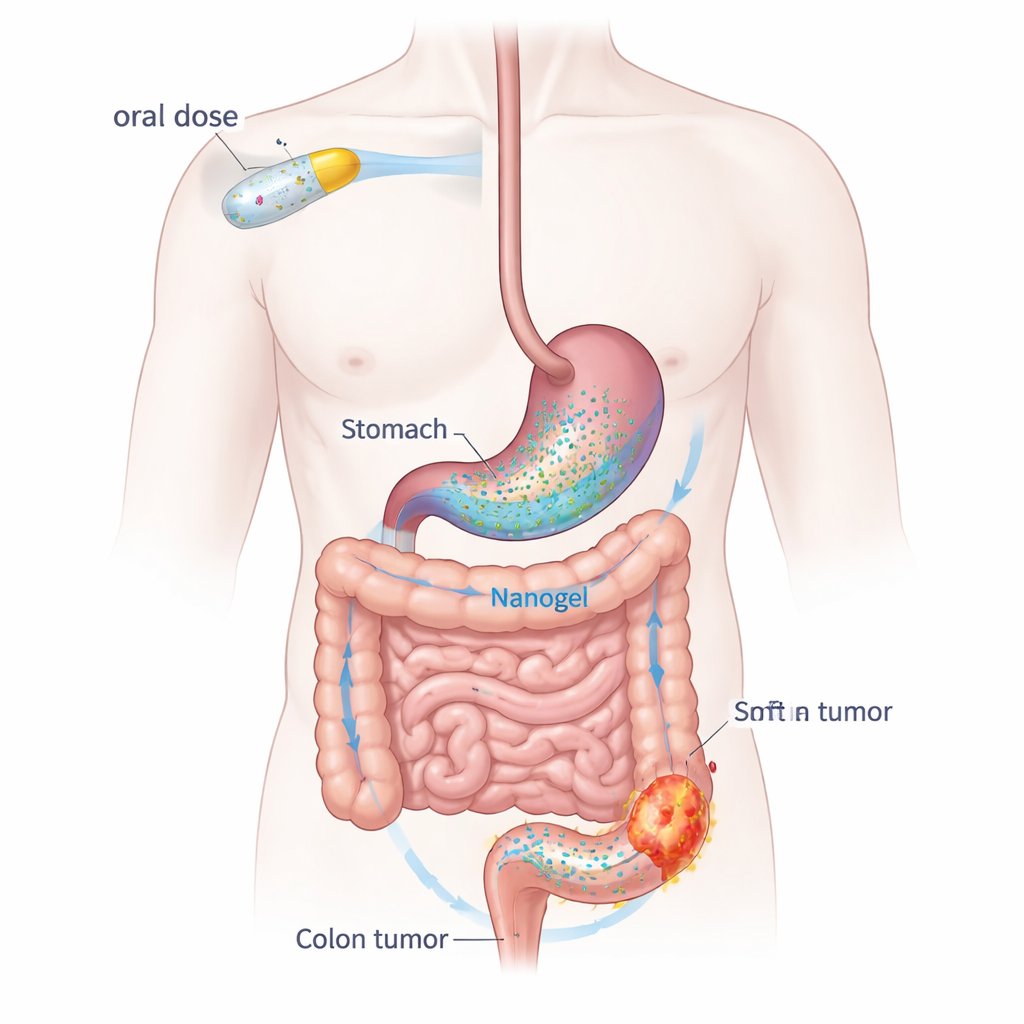
Een alledaagse pil omvormen tot een kankerrichtend laadvermogen
Dapagliflozine werkt normaal gesproken in de nieren om de bloedsuiker te verlagen, maar het vermindert ook ontsteking en remt celgroei — twee processen waarop kankers vertrouwen. Op zichzelf lost het middel echter slecht op in water en wordt het vrij snel uit het lichaam verwijderd. Om dit te overwinnen bouwde het team een “nanogel”-afgiftesysteem met twee voedselachtige polymeren: natriumalginaat, gewonnen uit zeewier, en polyvinylalcohol, een veelgebruikt, biocompatibel verdikkingsmiddel. Het middel zit opgesloten in deeltjes die ongeveer één tienduizendste van een millimeter breed zijn. Wanneer deze deeltjes het maagzuur tegenkomen, zakken ze neer en verknopen ze zich tot een zachte hydrogelmassa die blijft liggen en het middel geleidelijk vrijgeeft terwijl het naar de dikke darm beweegt.
Het middel beter oplosbaar maken en langzamer laten uitspoelen
De wetenschappers optimaliseerden eerst hoe de deeltjes werden gemaakt en verfijnden de verhouding van de twee polymeren zodat de nanodeeltjes klein, gelijkmatig van grootte en stabiel in vloeistof bleven. Ze bevestigden dat het middel goed in het polymeernetwerk was ingebed en gedeeltelijk was getransformeerd van een kristallijne naar een meer amorfe vorm, die doorgaans beter oplost. In testvloeistoffen die maag- en darmsappen nabootsen, verhoogde de nanogelformulering de schijnbare oplosbaarheid van dapagliflozine met ongeveer 1,7–1,8 keer vergeleken met het ruwe middel. Toen ze onderzochten hoe snel het middel eruit lekte, liet de nanogel een geleidelijk “langzaam-afgifte”-profiel over enkele uren zien, in plaats van de snelle piek die bij het gewone middel werd waargenomen. Eén recept, genaamd F2, vormde een compacte, duurzame gel die bij zure omstandigheden minstens twee uur intact bleef terwijl het geneesmiddel gelijkmatig werd vrijgegeven.
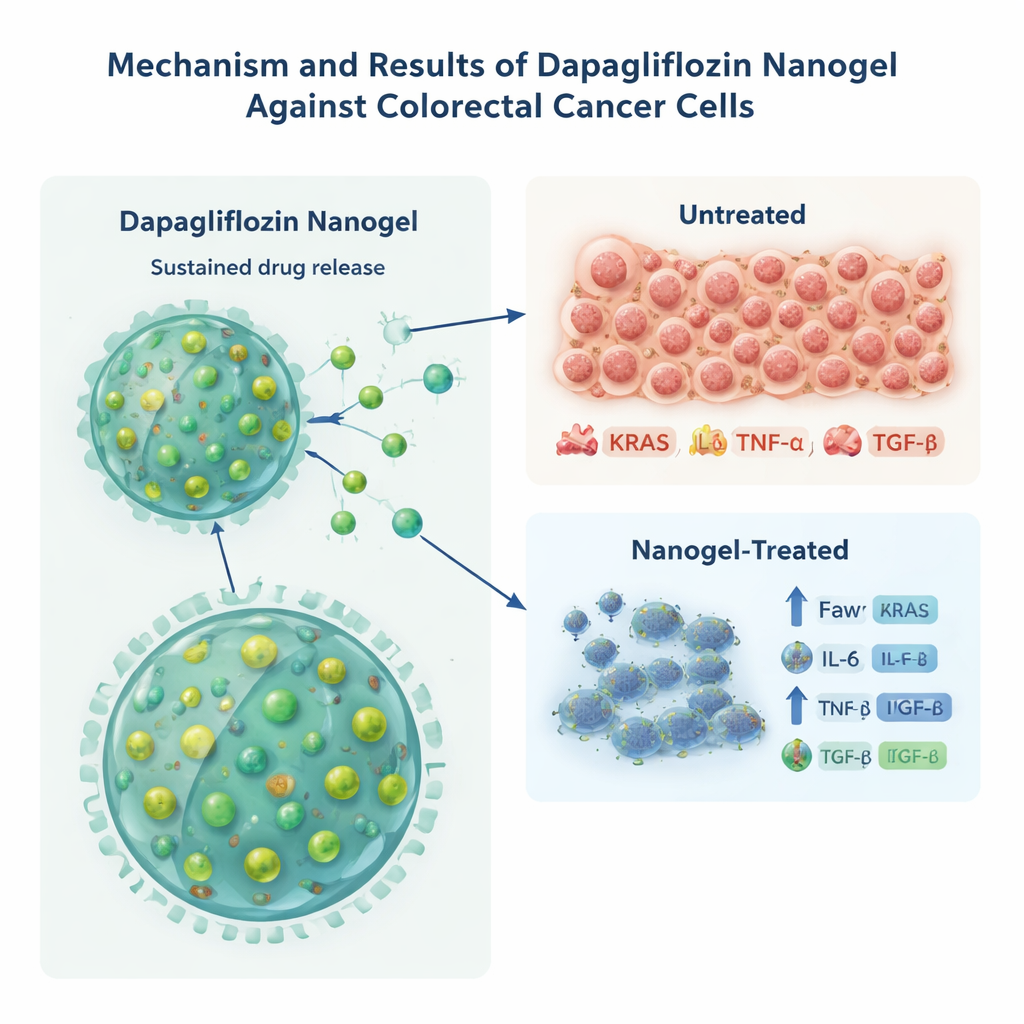
Kankercellen onder stress zetten in het laboratorium
Om te onderzoeken of deze nieuwe vorm van dapagliflozine daadwerkelijk kankercellen kon beschadigen, testte het team het op HCT-116 colorectale kankercellen gekweekt in petrisal. Vergeleken met dezelfde hoeveelheid vrij middel doodde de nanogelversie kankercellen bij lagere concentraties, waardoor de dosis om de celgroei te halveren met ongeveer een derde afnam. De onderzoekers bekeken vervolgens moleculen die verbonden zijn met agressief tumorgedrag en chronische ontsteking, waaronder KRAS (een belangrijk kankerbevorderend eiwit) en de signaaleiwitten IL-6, TNF-α en TGF-β. Cellen behandeld met het middelgeladen nanogel toonden veel lagere niveaus van al deze merkers dan cellen behandeld met het vrije middel of met lege deeltjes, wat suggereert dat de aanhoudende blootstelling door de nanodeeltjes effectiever de kanker- en ontstekingsgerelateerde signalen dempte. Omdat de cellijn al een vaste KRAS-mutatie draagt, waarschuwen de auteurs dat deze daling in KRAS-eiwit stressreacties kan weerspiegelen in plaats van directe genetische correctie, maar het ondersteunt nog steeds een sterke biologische impact.
Veranderingen in hoe het lichaam het geneesmiddel verwerkt
Het team ging vervolgens over naar dierstudies en gaf ratten ofwel een eenvoudige suspensie van dapagliflozinepoeder of de geoptimaliseerde nanogel, beide oraal en in dezelfde dosis. In de nanogelgroep verschenen de piekniveaus van het middel in het bloed later en waren ze lager, maar het middel bleef langer in circulatie. De totale blootstelling (gemeten als area under the curve) steeg licht met ongeveer 7%, en de schijnbare halfwaardetijd verdubbelde ruwweg. Deze veranderingen betekenen dat het lichaam het middel als een gelijkmatiger, langer durende dosis ervaart in plaats van een scherpe piek en snelle daling. Dat gedrag komt overeen met wat de onderzoekers met de gel wilden bereiken: het middel in de darm vasthouden, het langzaam vrijgeven en mogelijk hogere concentraties in het onderste darmkanaal en de dikke darm behouden, waar tumoren ontstaan.
Wat dit kan betekenen voor toekomstige kankerzorg
In gewone bewoordingen neemt deze studie een bekend diabetesmiddel en kleedt het uit met een nieuw “afgiftepak” zodat het beter colongezwellen kan bereiken en nabij kan blijven. De nanogel maakt het middel makkelijker oplosbaar, vertraagt de ontsnapping uit de darm en lijkt het toxischer te maken voor colorectale kankercellen terwijl belangrijke ontstekings- en groeisignalen worden geremd. Bij ratten spreidt het de aanwezigheid van het middel in het bloed zachtjes uit zonder de totale dosis drastisch te verhogen. Het werk bevindt zich nog in een vroeg stadium — beperkt tot één kankercellijn en kortdurende dierproeven — en heeft nog geen directe tumorkrimping in levende dieren of mensen aangetoond. Desalniettemin vormt het een gedetailleerde basis voor het herbestemmen van dapagliflozine als onderdeel van toekomstige behandelingen voor colorectale kanker, met behulp van slimme orale nanogels om een bekend pilletje om te vormen tot een meer gericht antikankerinstrument.
Bronvermelding: Abdullah, S., Thiab, S., Altamimi, A.A. et al. A repurposing Dapagliflozin via polymeric nanogels for colorectal cancer therapy. Sci Rep 16, 5625 (2026). https://doi.org/10.1038/s41598-026-36232-8
Trefwoorden: colorectale kanker, herbestemming van geneesmiddelen, nanodeeltjes, orale toediening van geneesmiddelen, dapagliflozine