Clear Sky Science · nl
Nationwide genomic surveillance of carbapenem- and colistin-resistant Klebsiella pneumoniae bloodstream isolates in Thailand (2020–2024)
Deadly Blood Infections on the Rise
Ziekenhuizen wereldwijd worden geconfronteerd met een verontrustende ontwikkeling: gewone bacteriën die vroeger nog gevoelig waren voor onze sterkste antibiotica worden vrijwel onbehandelbaar. Deze studie richt zich op Klebsiella pneumoniae, een micro-organisme dat de bloedbaan kan binnendringen en levensbedreigende infecties kan veroorzaken, en volgt hoe het zich in heel Thailand heeft ontwikkeld om zelfs middelen van laatste redmiddel te weerstaan. Begrijpen waar deze superbugs zich verspreiden en hoe ze medicijnen omzeilen is cruciaal om patiënten te beschermen, artsen te ondersteunen bij behandelingskeuzes en het volksgezondheidsbeleid te vormen.
Tracking a Hospital Superbug Across a Nation
De onderzoekers analyseerden 227 Klebsiella pneumoniae-monsters afkomstig uit het bloed van patiënten in ziekenhuizen door heel Thailand tussen 2020 en 2024. Deze monsters kwamen uit een landelijk surveillancenetwerk dat routinematig gegevens verzamelt over resistente infecties. Laboratoriumtests toonden aan dat meer dan 93% van deze bloedisolaten resistent was tegen carbapenems, een krachtige klasse antibiotica die vaak wordt ingezet wanneer andere middelen falen. Zorgelijk was dat bijna een derde van de carbapenemresistente stammen ook resistent bleek tegen colistine, een van de laatste opties waar artsen op terugvallen als niets anders werkt. Door standaard gevoeligheidstests te combineren met whole-genome sequencing kon het team niet alleen zien welke middelen faalden, maar ook welke genetische trucs de bacteriën gebruikten om te overleven.
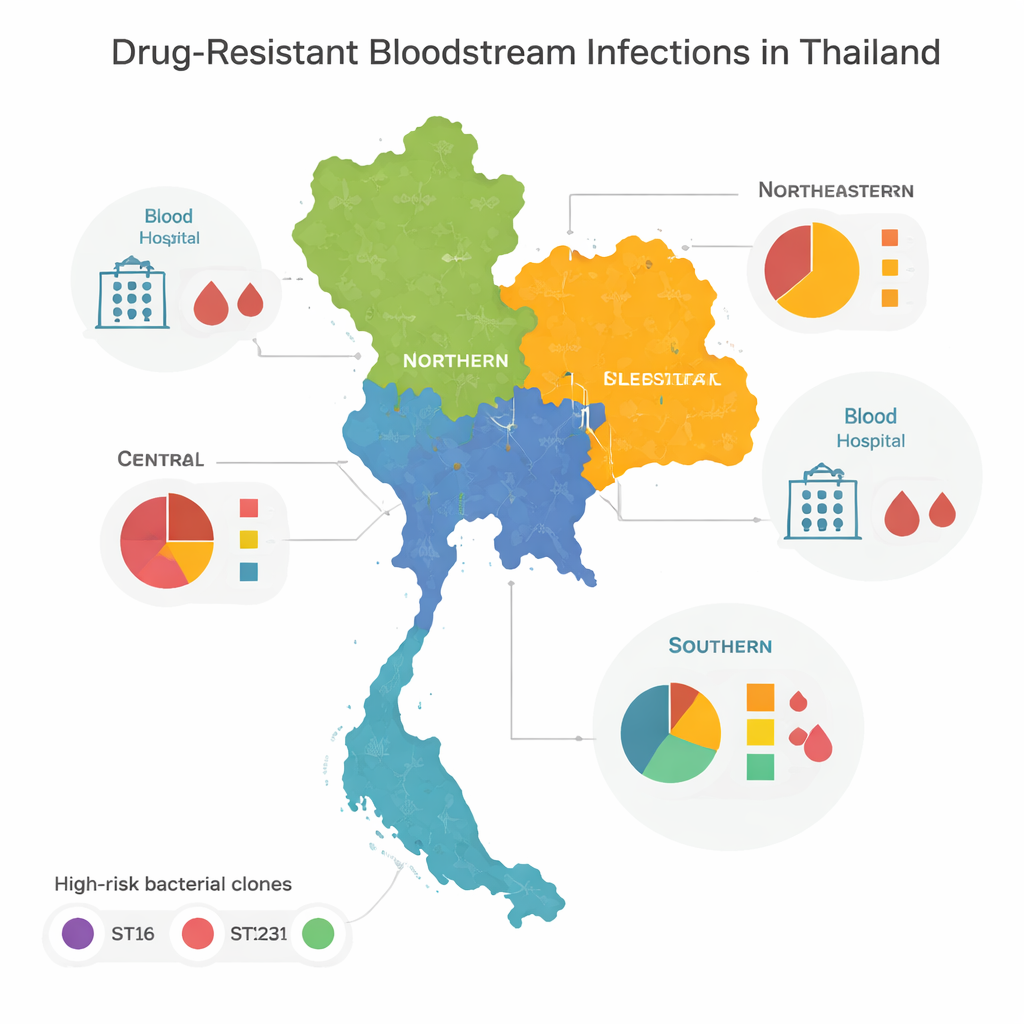
High-Risk Clones and Regional Patterns
Bij vergelijking van de genomen ontdekte het team dat de meeste resistente bacteriën tot een paar "high-risk" families, of clones, behoorden die wereldwijd bekendstaan om ziekenhuisuitbraken. Drie in het bijzonder — ST16, ST147 en ST231 — domineerden in centraal, noordelijk en noordoostelijk Thailand. Deze clones waren breed verspreid over regio’s, wat wijst op veelvuldig verkeer van patiënten, personeel of bacteriën tussen ziekenhuizen. Het zuiden van het land verschilde: daar werd niet één of enkele types gedomineerd, maar was er een grote variëteit aan lijnages, waarvan veel slechts éénmaal werden aangetroffen. Die diversiteit duidt op een complexere mix van lokale uitbraken, omgevingsbronnen en grensoverschrijdende bewegingen in plaats van één of twee dominante clones.
How the Bacteria Outsmart Antibiotics
De studie liet zien hoe deze bacteriën meerdere resistentiemechanismen combineren. Veel ST16- en ST231-stammen droegen genen zoals blaNDM en blaOXA, die enzymen produceren die carbapenemantibiotica afbreken voordat ze kunnen werken. Sommige hadden daarnaast veranderingen in hun buitenmembraan die de binnendringing van medicijnen verminderen, wat samen resulteert in zeer sterke resistentie. ST231-stammen droegen vaak het extra gen rmtF1, dat een belangrijke groep geneesmiddelen, de aminoglycosiden, blokkeert en zo de behandelopties verder verkleint. ST147 viel op door zijn genetische flexibiliteit: deze clone wisselde verschillende resistentiegenen en plasmiden — kleine mobiele DNA-cirkels — uit, waardoor het een potentieel knooppunt is voor het verspreiden van resistentiekenmerken naar andere bacteriën.
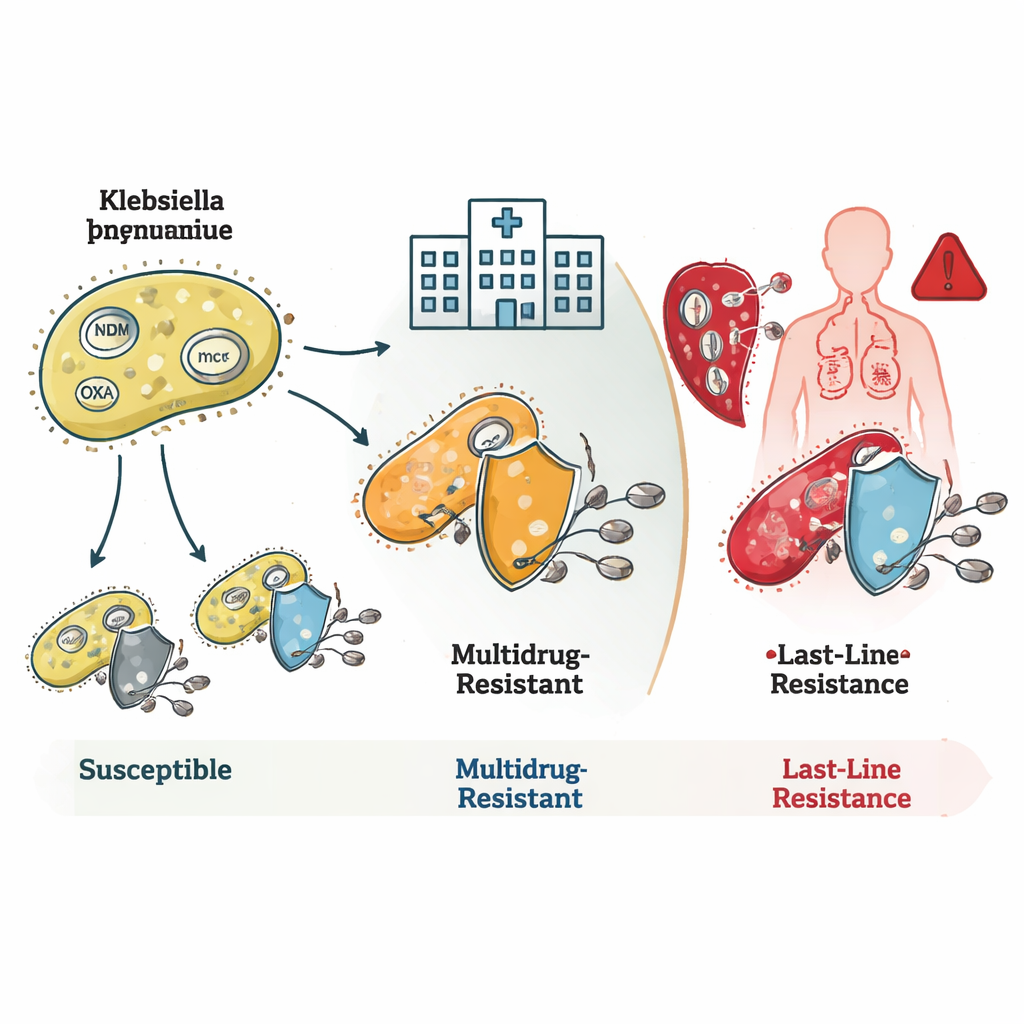
Last-Line Failures and Hidden Dangers
De meest alarmerende bevinding betrof resistentie tegen colistine, een medicijn dat artsen reserveren voor noodsituaties. Sommige zeldzame bacteriefamilies droegen mcr-genen, die via plasmiden tussen soorten kunnen springen en direct colistineresistentie veroorzaken. Andere stammen, met name binnen de ST16-clone, waren resistent tegen colistine terwijl ze geen bekende resistentiegenen of mutaties bezaten. Dit suggereert dat wetenschappers nog niet alle manieren in kaart hebben gebracht waarop bacteriën dit laatste middel kunnen neutraliseren. Het team identificeerde ook hypervirulente stammen — bacteriën die bijzonder goed ernstige ziekte kunnen veroorzaken — waaronder één lijn die hoge virulentie combineerde met resistentie tegen alle geteste carbapenems, een bijzonder gevaarlijke combinatie.
Why Genomic Surveillance Matters
Om te begrijpen hoe genetische veranderingen zich vertaalden naar echte faalresultaten in het laboratorium, gebruikten de onderzoekers statistische modellen om specifieke resistentiegenen te koppelen aan testuitslagen. Genen zoals blaNDM-1 en nauwe verwanten toonden zeer sterke associaties met carbapenemresistentie, waarmee hun centrale rol in behandeluitval werd bevestigd. Voor colistine hadden de meeste resistente bacteriën echter geen herkenbare resistentiemarkers, wat wijst op verborgen mechanismen die nog ontdekt moeten worden. De auteurs betogen dat routinematig gebruik van whole-genome sequencing in ziekenhuis surveillance kan werken als een vroegwaarschuwingssysteem: het detecteert opkomende high-risk clones, volgt hun bewegingen over regio’s en grenzen en kan snelle infectiecontroleacties sturen.
What This Means for Patients and Policy
Voor leken is de boodschap scherp maar helder: sommige bloedbaaninfecties in Thailand worden nu veroorzaakt door bacteriën die vrijwel elk middel waarover artsen beschikken, weerstaan, en een paar gevaarlijke families van deze microben verspreiden zich wijd. Tegelijk laat de studie zien dat met de juiste instrumenten — landelijke bemonstering, genetische analyse en snelle gegevensdeling — zorgsystemen deze dreigingen kunnen zien aankomen en zich kunnen aanpassen. Uitbreiding van genomische surveillance, ontwikkeling van snelle moleculaire tests en aanscherping van infectiepreventie kunnen helpen de opmars van deze superbugs te vertragen en tijd te winnen voor de ontwikkeling van nieuwe behandelingen en vaccins.
Bronvermelding: Krobanan, K., Kamjumphol, W., Leethongdee, P. et al. Nationwide genomic surveillance of carbapenem- and colistin-resistant Klebsiella pneumoniae bloodstream isolates in Thailand (2020–2024). Sci Rep 16, 5853 (2026). https://doi.org/10.1038/s41598-026-36228-4
Trefwoorden: antimicrobial resistance, Klebsiella pneumoniae, bloodstream infection, genomic surveillance, Thailand healthcare