Clear Sky Science · nl
Pyridinium- en broom-gesubstitueerde distyryl-BODIPY-kleurstoffen voor mitochondriën-gerichte photodynamische therapie
Cellen van binnenuit doen oplichten
Photodynamische therapie is een kankerbehandeling die speciale licht-geactiveerde medicijnen gebruikt om tumorcellen te doden, terwijl gezond weefsel grotendeels wordt gespaard. Deze studie onderzoekt een nieuwe familie fluorescerende kleurstoffen die zijn ontworpen om zich te richten op de energiecentrales van de cel—de mitochondriën—en, wanneer belicht met dieprood licht, reactieve zuurstofsoorten te genereren die kankercellen kunnen vernietigen. Het onderzoek laat zowel de belofte als de valkuilen zien van het moleculair ontwerpen van zulke kleurstoffen.
Waarom de energiecentrales van de cel targeten?
Mitochondriën zijn cruciaal voor energieproductie en helpen bepalen of een cel overleeft of sterft. Kankercellen hebben vaak een sterker geladen mitochondriale membraan dan normale cellen, waardoor zij positief geladen moleculen veel sterker aantrekken. De onderzoekers maakten hiervan gebruik door een positief geladen pyridiniumgroep aan een bekend fluorescerend kleurstofskelet genaamd BODIPY te koppelen. Dit ontwerp helpt de kleurstoffen naar mitochondriën te sturen, waar licht-geïnitieerde chemische reacties maximale schade aan kankercellen kunnen toebrengen met beperkt effect elders.
Slimmere licht-geactiveerde kleurstoffen ontwerpen
Het team maakte drie nauwe verwante kleurstoffen, PyBHI, PyBMI en PyBBrI, die voornamelijk verschillen in het aantal broomatomen dat ze dragen (geen, één of twee). Alle drie delen ze een langgerekte structuur die hun lichtabsorptie en -emissie naar het nabij-infrarode gebied verschuift—een nuttig venster waar licht dieper door weefsel kan dringen. In theorie zouden deze kleurstoffen twee interne routes kunnen gebruiken om een “triplet” geëxciteerde toestand te bereiken die reactieve singletzuurstof produceert: één aangedreven door de zware broomatomen en een andere door een tijdelijke verschuiving van elektrische lading binnen het molecuul. 
Wanneer theorie experimentele realiteit ontmoet
Ondanks het elegante ontwerp lieten gedetailleerde tests zien dat de kleurstoffen niet zo efficiënt singletzuurstof genereerden als gehoopt. Met behulp van chemische probes die hun kleur verliezen bij reactie met singletzuurstof, maten de onderzoekers zeer lage zuurstofgeneratie-opbrengsten voor alle drie de kleurstoffen, met slechts een bescheiden verbetering naarmate er meer broomatomen werden toegevoegd. Ultrafast laserexperimenten toonden waarom: na lichtabsorptie komen de kleurstoffen snel in lading-verschoofde toestanden terecht die meestal onschadelijk als warmte ontspannen in plaats van om te zetten naar de gewenste triplettoestand. In de gebromineerde versies openen de zware atomen weliswaar een route naar de triplettoestand, maar deze route is veel langzamer dan het concurrerende energieverlies, waardoor de algehele efficiëntie beperkt blijft.
Richting tumor-mitochondriën in levende cellen
Het verhaal verandert in een biologische omgeving. In gekweekte menselijke borstkanker- (MCF-7) en baarmoederhalskanker- (HeLa) cellen toonden confocale microscopie aan dat alle drie de kleurstoffen sterk in mitochondriën accumuleren en colocaliseren met een standaard mitochondriale kleurstof. Toxiciteitstesten in het donker wezen uit dat de kleurstoffen grotendeels onschadelijk zijn zonder licht. Onder roodlichtbestraling veroorzaakte de di-bromineerde kleurstof PyBBrI echter aanzienlijke kankerceldood, waarbij lage nanomolaire doses de levensvatbaarheid van cellen halveerden. De andere twee kleurstoffen waren veel minder effectief. 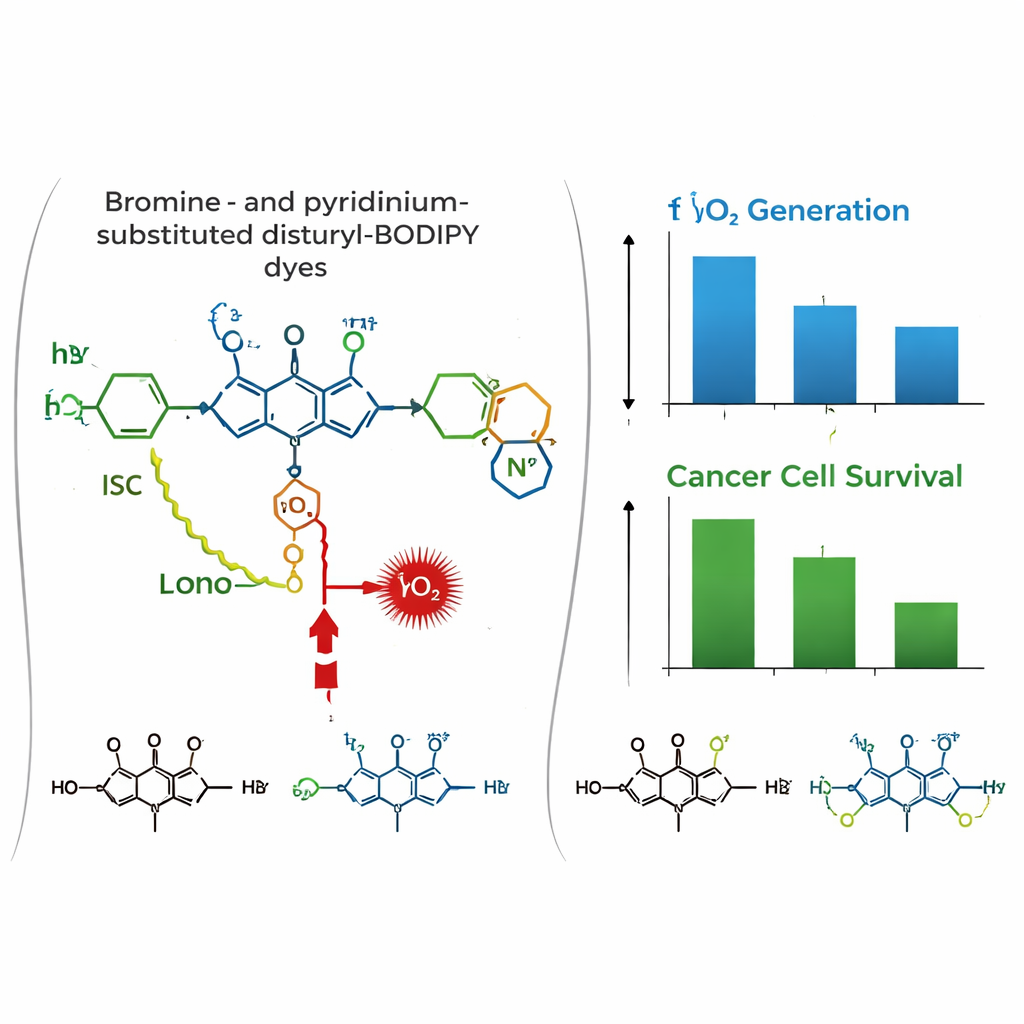
Wat dit betekent voor toekomstige kankertherapieën
Voor niet-specialisten is de kernboodschap dat kleine chemische aanpassingen het gedrag van licht-geactiveerde kankerdrugs drastisch kunnen veranderen, en dat hun prestaties in echte cellen beter—of slechter—kunnen zijn dan voorspeld op basis van basismetingen. In dit geval toonde de meest sterk gemodificeerde kleurstof, PyBBrI, in een reageerbuis slechts beperkte productie van reactief zuurstof, maar bleek zeer krachtig tegen kankercellen zodra zij hun mitochondriën bereikte. Het werk benadrukt zowel het belang van het richten van medicijnen op kwetsbare structuren binnen kankercellen als de complexiteit van het voorspellen van photodynamische efficiëntie. Het wijst de weg naar de volgende generatie mitochondriën-gerichte therapieën die nabij-infrarood licht gebruiken om cel-dodende chemie precies daar "aan" te zetten waar het nodig is.
Bronvermelding: Kim, C., Badon, I.W., Jo, J. et al. Pyridinium- and bromine-substituted distyryl-BODIPY dyes for mitochondria-targeted photodynamic therapy. Sci Rep 16, 6789 (2026). https://doi.org/10.1038/s41598-026-36213-x
Trefwoorden: photodynamische therapie, mitochondriën-gerichte kleurstoffen, BODIPY, singletzuurstof, kankercellen