Clear Sky Science · nl
γ-straling veroorzaakt regiogebonden subcellulaire veranderingen in markers voor amyotrofe laterale sclerose en frontotemporale dementie in varkenshersenen
Waarom kleine stralingsdoses en varkenshersenen ertoe doen
De meeste mensen zien straling vooral als schadelijk, vooral voor de hersenen. Toch is onze omgeving doordrongen van lage niveaus straling door medische scans, vliegreizen en de omgeving. Tegelijkertijd blijven wetenschappers zoeken naar de oorzaken van amyotrofische laterale sclerose (ALS), de dodelijke ziekte die honkbalheld Lou Gehrig verlamde, en zijn nauwe verwant, frontotemporale dementie (FTD), die gedrag en persoonlijkheid aantast. Deze studie stelt een verrassend hoopvolle vraag: kan een enkele, bescheiden dosis gammastraling de hersenchemie subtiel heroriënteren op manieren die niet louter schadelijk zijn, en mogelijk zelfs bescherming bieden tegen moleculaire veranderingen die met ALS en FTD geassocieerd worden?
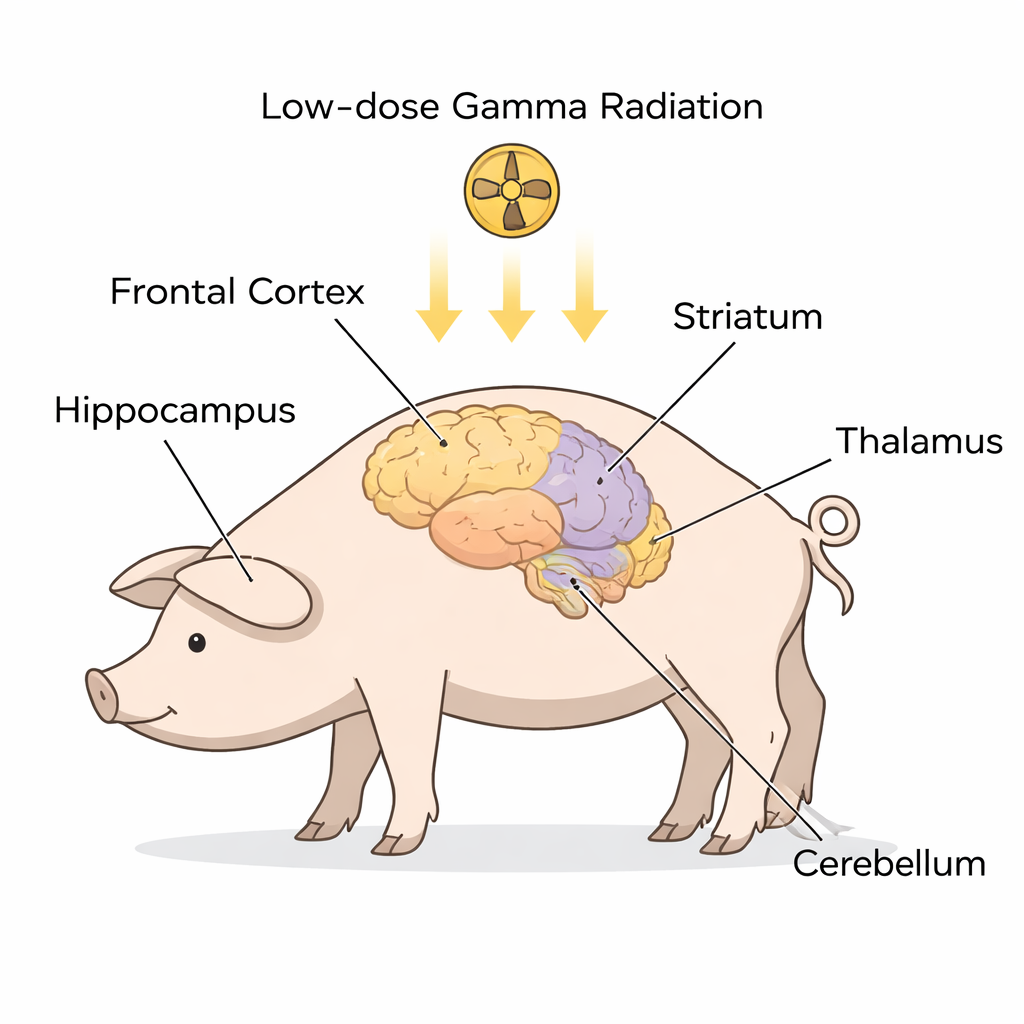
Een nadere blik op waarschuwingssignalen van ALS in de hersenen
In plaats van patiënten met bestaande ALS te bestuderen, werkten de onderzoekers met gezonde Göttingen-minivarkens, waarvan de hersenen anatomisch op die van ons lijken. Negen dieren kregen een eenmalige, gehele-lichaam blootstelling aan lage-dosis gammastraling, terwijl zes verdoofd maar niet bestraald werden en als controles dienden. Ongeveer een maand later disseceerden de wetenschappers vijf belangrijke hersengebieden die vaak bij ALS en FTD betrokken zijn — de frontale cortex, hippocampus, striatum, thalamus/hypothalamus en cerebellum. In elk gebied scheidden ze de celinhoud in twee hoofdcompartimenten: het cytoplasma (de vloeibare binnenkant van de cel) en de kern (het compartiment met het DNA). Met een techniek genaamd Western blotting maten ze de niveaus van verschillende eiwitten die sterk aan ALS en ALS‑FTD gerelateerd zijn, waaronder SOD1, FUS, C9orf72, STMN2, ubiquitine, TDP‑43 en een gewijzigde vorm genaamd gefosforyleerd TDP‑43.
Straling laat sommige markers ongewijzigd — en verplaatst andere
Een geruststellende bevinding was dat de totale niveaus van SOD1, een eiwit waarvan mutaties sommige erfelijke vormen van ALS veroorzaken, in geen enkel gebied veranderden na straling. Evenmin veranderden de belangrijkste vormen van TDP‑43 — het eiwit dat het vaakst in ALS-gerelateerde klompjes in de hersenen wordt gevonden — in zowel de kern als het cytoplasma in alle onderzochte gebieden. Maar niet alles bleef statisch. Het team zag regiogebonden en compartimentgebonden verschuivingen in verschillende andere eiwitten. Zo nam FUS, een eiwit dat normaal in de kern voorkomt maar in ALS kan ontsporen en samenklonteren, af in het cytoplasma van de thalamus/hypothalamus na straling, terwijl de kernniveaus in de frontale cortex stegen en in de hippocampus daalden. Het ALS-geassocieerde eiwit C9orf72 veranderde niet in het celvocht maar toonde een daling binnen hippocampale kernen. STMN2, een eiwit belangrijk voor het behoud van zenuwvezels, nam ook af in de hippocampale kernen, wat wijst op een gecoördineerde respons tussen deze twee moleculen in dat geheugen-gerelateerde gebied.
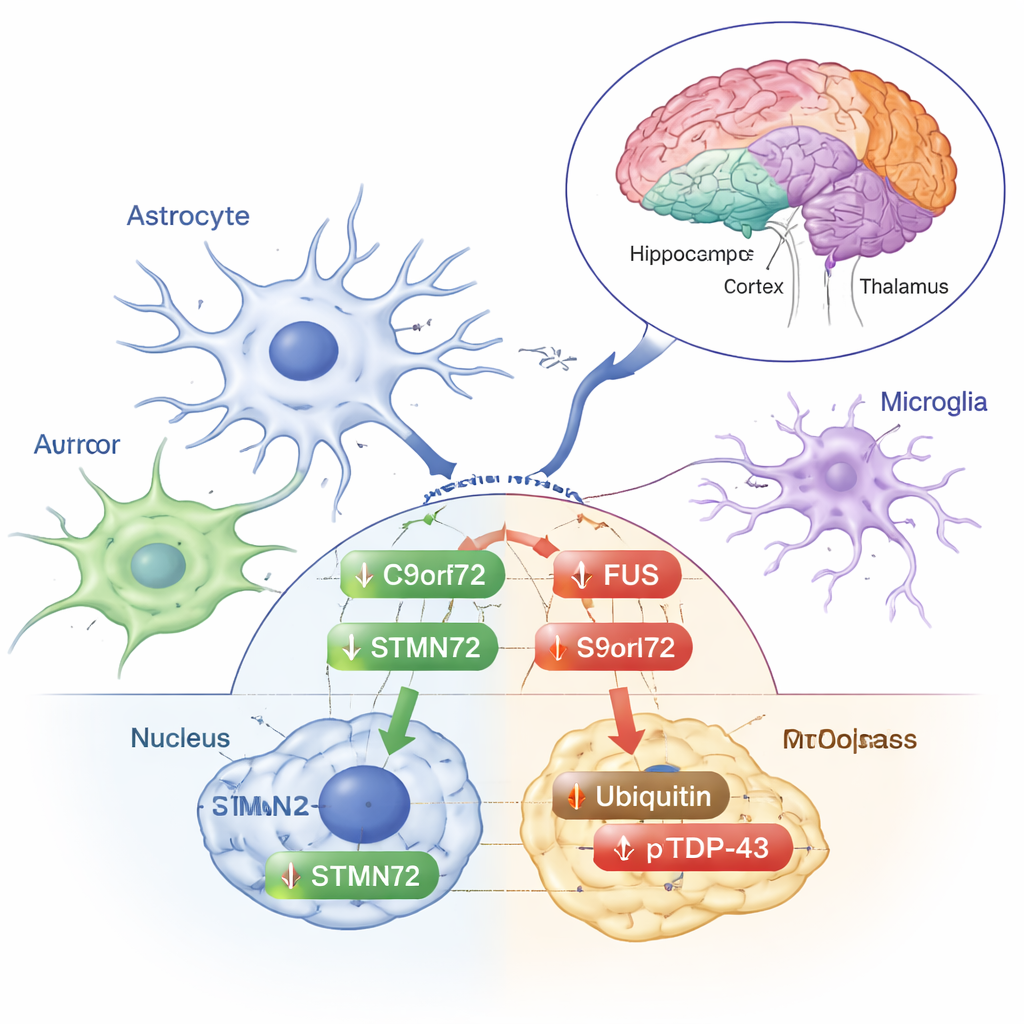
Stresssignalen of vroege bescherming?
Andere veranderingen leken meer op klassieke stressreacties. Ubiquitine — het kleine labeltje dat de cel gebruikt om beschadigde eiwitten te markeren voor opruiming — nam toe in de cytoplasmatische fractie van de frontale cortex. De gefosforyleerde vorm van TDP‑43, die vaak verrijkt is in de abnormale afzettingen gezien bij ALS en FTD, steeg in het cytoplasma van de frontale cortex, het striatum en de thalamus/hypothalamus, ook al veranderde het totale TDP‑43 zelf niet. Deze verschuivingen suggereren dat lage-dosis straling het eiwithandling‑apparaat van de hersenen lichtjes aanstuurt zonder de volledige patronen van verkeerd vouwen en aggregatie te ontketenen die de ziekte kenmerken. De auteurs benadrukken dat deze reacties per hersengebied en per subcellulair compartiment verschillen, wat onderstreept hoe fijn afgestemd de hersenreactie op stress kan zijn.
Wat dit zou kunnen betekenen voor ALS‑risico — en mogelijke voordelen
Betekent dit dat lage-dosis straling ALS veroorzaakt? De gegevens pleiten tegen een eenvoudig ja. De onderzoekers zagen niet de kenmerkende mislokalisatie of ophoping van de belangrijkste ALS-eiwitten, en veel veranderingen wezen op gewijzigde regulatie in plaats van directe schade. Intrigerend genoeg passen deze resultaten bij eerder werk van dezelfde groep en anderen waaruit blijkt dat kleine hoeveelheden straling soms hormese kunnen opwekken — een fenomeen waarbij milde stress reparatiepaden activeert en schadelijke eiwitten vermindert, zoals die geassocieerd met de ziekte van Alzheimer of Parkinson in diermodellen. De huidige studie suggereert dat, althans op korte termijn, een enkele lage dosis gammastraling ALS‑gerelateerde markers op manieren herverdeelt die adaptief in plaats van destructief kunnen zijn.
Grote vragen en behoedzame hoop
Voor niet‑specialisten is de belangrijkste conclusie dat de relatie tussen straling en hersengezondheid genuanceerder is dan “alle straling is slecht”. In dit groot‑diermodel veroorzaakte blootstelling aan lage‑dosis gamma subtiele, regiogebonden verschuivingen in eiwitten die met ALS en FTD geassocieerd zijn, zonder de schadelijke patronen te reproduceren die in patiëntenhersenen worden gezien. Deze veranderingen kunnen het proberen van de hersenen weerspiegelen om met stress om te gaan en zich te herstellen, en in sommige gevallen zelfs nuttig blijken. De studie keek echter slechts één maand na een enkele blootstelling en alleen naar de hersenen (niet naar het ruggenmerg, waar ALS het zwaarst toeslaat). Langetermijn- en herhaalde-dosisstudies zijn nodig voordat men zulke bevindingen op mensen zou overwegen. Desalniettemin opent dit werk een nieuw venster op hoe alledaagse hoeveelheid straling interacteert met de moleculen die ten grondslag liggen aan verwoestende neurodegeneratieve ziekten — en werpt het de mogelijkheid op dat, onder zorgvuldig gecontroleerde omstandigheden, kleine doses ooit gebruikt zouden kunnen worden om de eigen verdedigingsmechanismen van de hersenen subtiel te stimuleren.
Bronvermelding: Iacono, D., Murphy, E.K., Perl, D.P. et al. γ-Radiation induces region-specific subcellular alterations of amyotrophic lateral sclerosis and frontotemporal dementia markers in swine brain. Sci Rep 16, 5627 (2026). https://doi.org/10.1038/s41598-026-36208-8
Trefwoorden: amyotrofische laterale sclerose, frontotemporale dementie, lage-dosis straling, hersenproteïnen, minivarkenmodel