Clear Sky Science · nl
Verlies van leukocytentelomeren na bestraling bij prostaatkanker: een prospectieve studie
Waarom dit onderzoek belangrijk is voor kankeroverlevenden
Mensen leven langer na kanker, maar veel overlevenden ervaren problemen die voelen als versnelde veroudering — vermoeidheid, kwetsbaarheid en andere chronische aandoeningen die te vroeg lijken te verschijnen. Deze studie stelt een eenvoudige maar belangrijke vraag: laat bestraling voor prostaatkanker een blijvend spoor achter op de fundamentele verouderingsklok van het lichaam, verborgen in onze chromosomen?
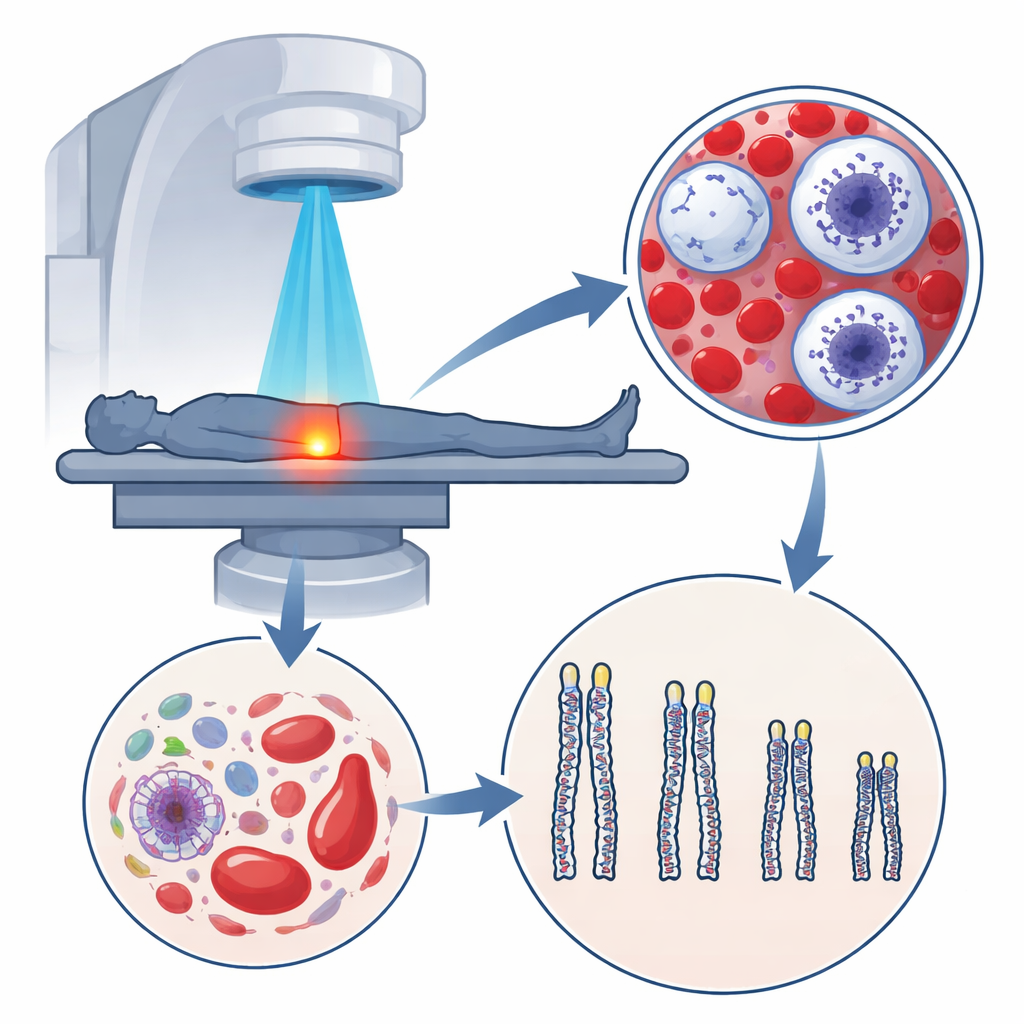
De kleine dopjes die ons DNA beschermen
Aan het uiteinde van onze chromosomen zitten telomeren, kleine stukjes DNA die werken als de plastic uiteinden van schoenveters en voorkomen dat genetisch materiaal rafelt. Elke keer dat een cel zich deelt, worden deze dopjes iets korter. Wanneer ze te kort worden, wordt de cel in een stilstand gezet of sterft ze, een proces dat samenhangt met natuurlijke veroudering. Omdat witte bloedcellen gemakkelijk uit bloed te bemonsteren zijn en weerspiegelen wat in veel weefsels gebeurt, wordt hun telomerlengte vaak gebruikt als maat voor "biologische leeftijd", die kan afwijken van het aantal jaren dat iemand heeft geleefd.
Nader bekeken tijdens en na de behandeling
Om te onderzoeken hoe moderne bestraling van de prostaat deze verouderingsmaat zou kunnen beïnvloeden, volgden onderzoekers 314 mannen van 65 jaar en ouder die curatieve bestraling ondergingen in één medisch centrum. Bloedmonsters werden vier keer afgenomen: vóór de behandeling, aan het einde van de meerdere weken durende bestraling, en vervolgens 3 maanden en 15 maanden later. In elk monster mat het team de gemiddelde relatieve lengte van telomeren in witte bloedcellen met een gevoelige DNA-test. Dit ontwerp stelde hen in staat om te volgen hoe ieders telomeren in de loop van de tijd veranderden, in plaats van alleen verschillende mensen op één moment te vergelijken.
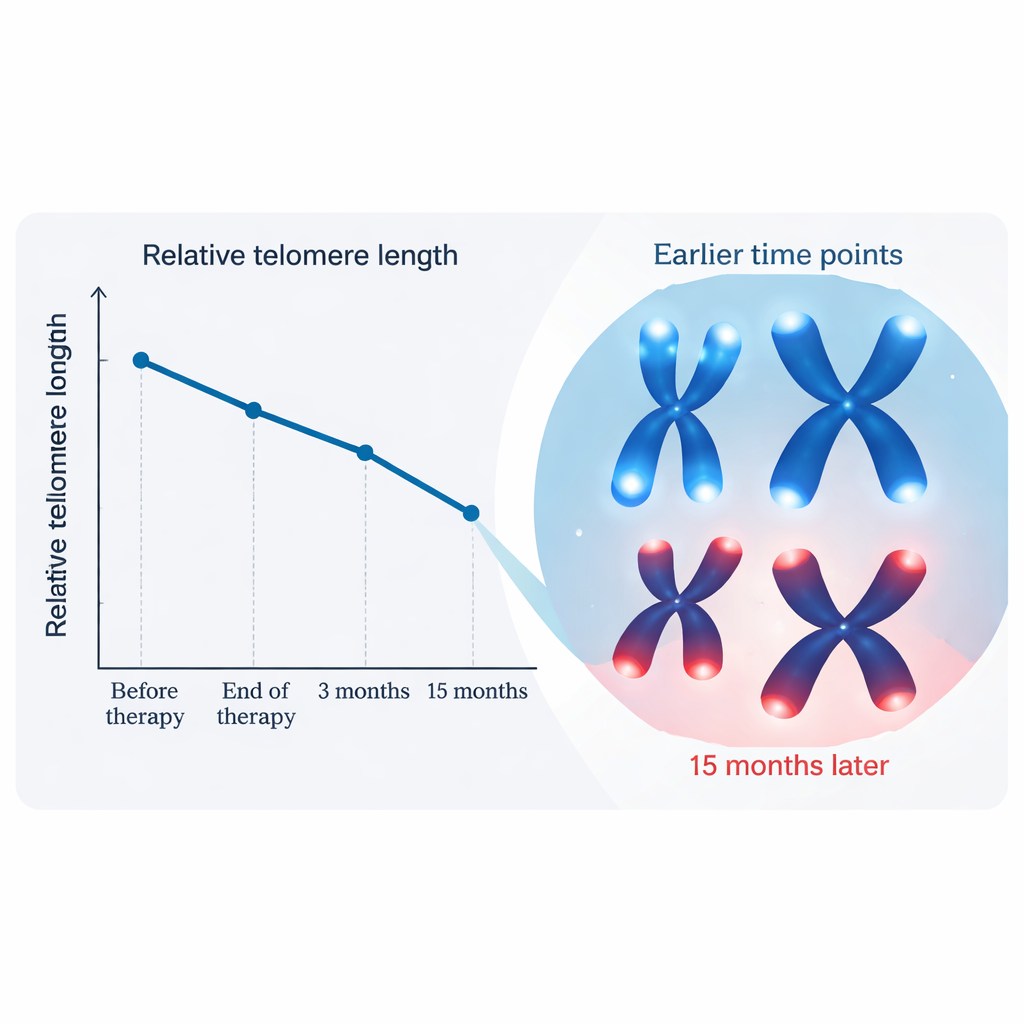
Wat er met telomeren in de tijd gebeurde
De telomerlengte bleef grotendeels vergelijkbaar van vóór de behandeling tot het einde van de bestraling en ook bij de controle na 3 maanden, met kleine schommelingen die statistisch niet betekenisvol waren. De opvallende verandering deed zich voor bij het 15-maandenmoment: gemiddeld waren de telomeren ongeveer 15 procent korter dan bij aanvang, een daling veel groter dan verwacht zou worden bij normale veroudering over iets meer dan een jaar bij oudere volwassenen. Dit patroon suggereert dat de lange termijn biologische impact van bestraling op het bloed langzaam kan optreden, lang nadat zichtbare bijwerkingen zijn verdwenen. De onderzoekers onderzochten ook of factoren zoals leeftijd, hoge bloeddruk, roken, behandelingsdetails of bestraling van nabijgelegen lymfeklieren deze veranderingen zouden beïnvloeden. Leeftijd en hoge bloeddruk lieten bescheiden verbanden zien met de mate van inkorting, terwijl de meeste behandelvariaties in deze groep geen duidelijk effect hadden op de uitkomst.
Hoe bestraling cellulaire slijtage kan versnellen
Waarom zou een lokale bestraling van de prostaat telomeren in circulerende bloedcellen beïnvloeden? De auteurs wijzen op twee verbonden processen. Ten eerste genereert ioniserende straling reactieve zuurstofmoleculen die DNA kunnen beschadigen, en telomeren zijn bijzonder kwetsbaar voor dit soort schade en worden minder efficiënt gerepareerd dan andere regio's. Ten tweede kan radiotherapie een aanhoudende ontstekingsreactie in het lichaam opwekken, waardoor witte bloedcellen vaker gaan delen en er meer schadelijke zuurstofbijproducten vrijkomen. Beide mechanismen zouden de geleidelijke erosie van telomeren kunnen versnellen, waardoor cellen in de richting van senescentie worden geduwd — een onomkeerbare "oude" toestand waarin ze niet meer delen maar wel invloed blijven uitoefenen op omliggende weefsels.
Wat dit voor patiënten zou kunnen betekenen
Voor de mannen in deze studie bleef prostaatbestraling een curatieve behandeling, maar ze was ook geassocieerd met tekenen van versnelde biologische veroudering in hun bloedcellen een jaar na therapie. Kortere telomeren bewijzen op zichzelf niet dat iemand kwetsbaar of ziek zal worden, maar ze hangen samen met een hoger risico op leeftijdsgerelateerde problemen zoals hartziekten, diabetes en cognitieve achteruitgang. De bevindingen benadrukken dat succesvolle kankerbehandeling verborgen langetermijnkosten kan hebben en onderstrepen de noodzaak van nazorg die rekening houdt met verouderingsgerelateerde gezondheid, niet alleen met tumorcontrole. De auteurs betogen dat grotere, langere studies — inclusief vergelijkingen met mensen die geen bestraling krijgen — nodig zijn om deze resultaten te bevestigen en om beschermende benaderingen te testen, zoals het richten op ontsteking of oxidatieve stress, die patiënten zouden kunnen helpen hun biologische veerkracht na therapie te behouden.
Bronvermelding: Langsenlehner, T., Paal, K., Thurner, E.M. et al. Leukocyte telomere attrition following radiotherapy in prostate cancer: a prospective study. Sci Rep 16, 5905 (2026). https://doi.org/10.1038/s41598-026-36205-x
Trefwoorden: prostaatkanker, bestraling, telomeren, biologische veroudering, cellulaire veroudering