Clear Sky Science · nl
FcIgG-GE11-Melittin als nieuw EGFR-gericht peptibody met krachtige cytotoxische werking tegen kankercellen
Bijengif ontmoet precisiemalige kankertherapie
Veel veelbelovende kankergeneesmiddelen zijn simpelweg te schadelijk voor de rest van het lichaam om veilig te kunnen worden gebruikt. Een opvallend voorbeeld is melittine, het belangrijkste toxine in bijengif: het kan kankercellen doen uiteenvallen, maar kan ook rode bloedcellen en gezond weefsel beschadigen. Deze studie onderzoekt een slimme omweg: het bouwen van een "geleide raket" die melittine rechtstreeks naar tumorcellen brengt die een specifiek oppervlaktemarker tonen, terwijl normale cellen grotendeels onaangetast blijven.
Waarom een veelvoorkomende kankerschakel richten
Een belangrijke speler in veel tumoren is een molecuul genaamd epidermale groeifactorreceptor, of EGFR. Deze receptor zit op het celoppervlak en helpt de groei en het overleven te regelen. In verschillende kankers—waaronder long-, colorectale, prostaat- en sommige hoofd-hals- en nierkankers—is EGFR overgeproduceerd, wat ongecontroleerde celdeling stimuleert. Daarom zijn geneesmiddelen die zich aan EGFR hechten een belangrijke klasse van gerichte therapieën geworden. Bestaande EGFR-middelen blokkeren echter voornamelijk signalen; ze maken niet actief gaten in kankercellen. De onderzoekers vroegen zich af of ze de krachtige cel-lyserende eigenschap van melittine konden benutten en deze selectief konden afleveren aan EGFR-rijke tumorcellen.
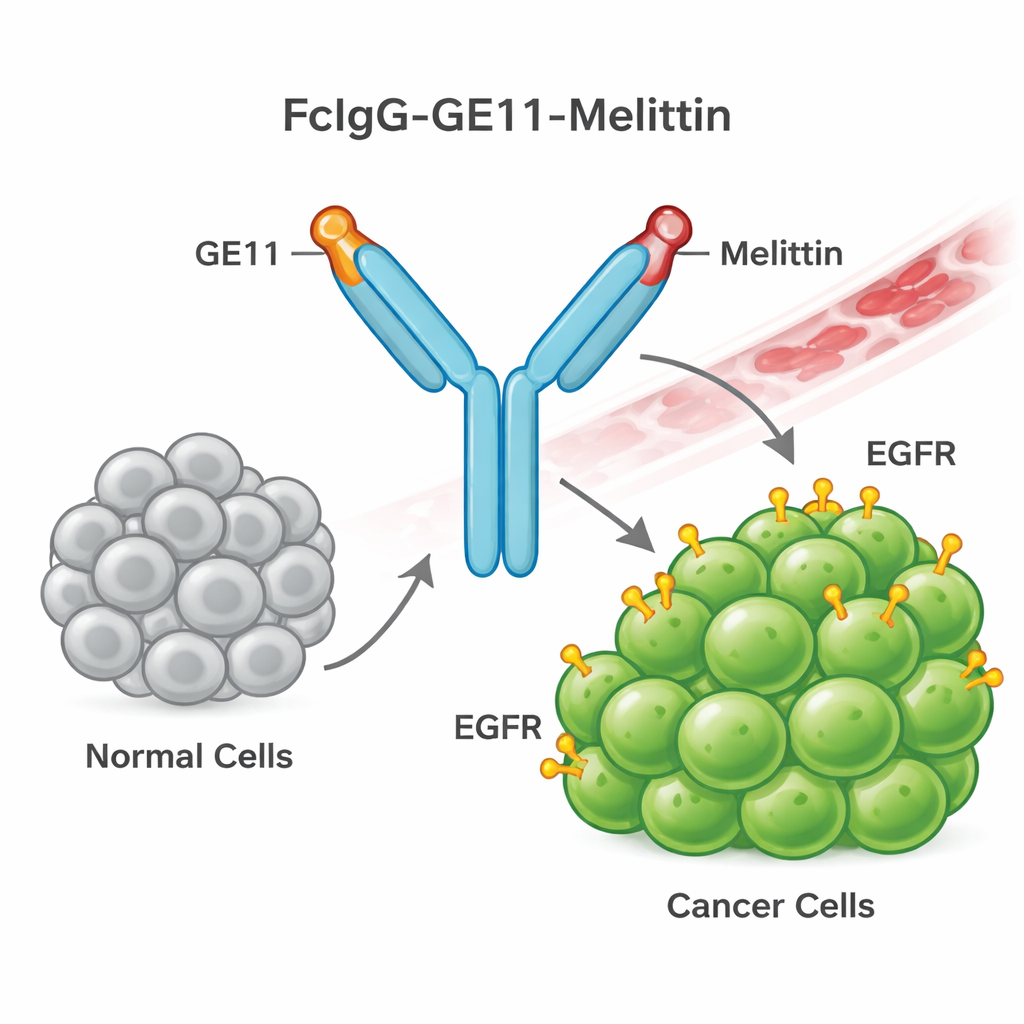
Een geleid wapen van bijengif bouwen
Daartoe ontwierp het team een nieuw fusie-eiwit dat ze FcIgG-GE11-Melittin noemen. Het combineert drie onderdelen: een antistof-"staart" (het Fc-gedeelte van menselijke IgG) die de stabiliteit in de bloedbaan verbetert en zuivering vergemakkelijkt; een kort geleidend peptide genaamd GE11 dat EGFR op kankercellen herkent en bindt; en melittine, het bijengifpeptide dat celmembranen kan doen scheuren. Bacteriën werden genetisch aangepast om dit fusie-eiwit in grote hoeveelheden te produceren. Het eiwit werd vervolgens opnieuw gevouwen en gezuiverd, en laboratoriumtests bevestigden dat het de verwachte dimerische vorm aannam en het menselijke antistoftag droeg, wat aantoont dat het construct correct was opgebouwd.
Zich vasthechten aan tumorcellen, niet aan willekeurige cellen
De volgende vraag was of dit ontworpen molecuul daadwerkelijk EGFR-rijke kankercellen vindt en eraan blijft zitten. Met flowcytometrie testten de auteurs binding aan A549-longkankercellen, die bekend staan om hun overexpressie van EGFR. Cellen behandeld met FcIgG-GE11-Melittin toonden een sterke toename van fluorescentie, wat aangeeft dat veel fusie-moleculen zich aan hun oppervlak hadden gehecht. Een niet-gerelateerd peptibody, Romiplostim, toonde bijna geen binding en diende als negatieve controle. Het bindingsprofiel van het nieuwe construct kwam sterk overeen met dat van Cetuximab, een bekende EGFR-antistof, wat de gedachte ondersteunt dat het GE11-deel het fusie-eiwit correct naar zijn doel begeleidt.
Kankercellen doden terwijl bloedcellen gespaard blijven
Vervolgens testte het team hoe goed het fusie-eiwit verschillende kankercellijnen in kweek kon doden. Vrije melittine alleen was extreem krachtig maar niet discriminerend en verminderde de overleving scherp zelfs bij lage doses in long- (A549), prostaat- (DU145) en colorectale (SW480) kankercellen. Daarentegen toonde FcIgG-GE11-Melittin dosisafhankelijke doding die het sterkst was in EGFR-positieve cellen, terwijl een EGFR-arme borstkankerlijn (MDA-MB-453) relatief resistent was. Dit patroon suggereert dat de aanval van het fusieconstruct afhankelijk is van EGFR-richting in plaats van willekeurige membraanschade. Het belangrijkste is dat vrije melittine in experimenten met menselijke rode bloedcellen bijna volledige hemolyse veroorzaakte bij bescheiden doses, terwijl het fusie-eiwit minder dan 5% hemolyse produceerde, zelfs bij zeer hoge concentraties. Met andere woorden, het vastmaken van melittine aan de EGFR-zoekende drager verminderde sterk de neiging om rode bloedcellen te laten barsten.
Wat dit kan betekenen voor toekomstige kankerzorg
Al met al laat dit werk zien dat het koppelen van een krachtig membraan-verstorend toxine zoals melittine aan een precies richtsysteem het kan omvormen van een breed toxische stof tot een meer tumorselectief wapen. FcIgG-GE11-Melittin hecht sterk aan EGFR-overexpressende kankercellen, doodt ze op een gecontroleerde, dosisafhankelijke manier en veroorzaakt minimale schade aan rode bloedcellen in het laboratorium. Hoewel verdere dierstudies en veiligheidstests nodig zijn vóór eventueel gebruik bij patiënten, illustreert deze benadering hoe het herontwerpen van natuurlijke toxines tot geleide therapieën nieuwe wegen kan openen voor de behandeling van EGFR-positieve kankers, effectiever en met minder bijwerkingen.
Bronvermelding: Hallaji, M., Fayaz, S., Allahyari, M. et al. FcIgG-GE11-Melittin as a novel EGFR targeted peptibody with potent cytotoxic activity against cancer cells. Sci Rep 16, 7047 (2026). https://doi.org/10.1038/s41598-026-36167-0
Trefwoorden: gerichte kankertherapie, EGFR, bijengif melittine, peptibody, tumorselectieve toxines