Clear Sky Science · nl
Cytoplasmatisch TDP-43 veroorzaakt vroege gedragsstoornissen zonder neurodegeneratie in een serotonerg neuron-specifiek C. elegans-model
Waarom kleine wormen van belang zijn voor grote hersenziektes
Aandoeningen zoals amyotrofische laterale sclerose (ALS) en frontotemporale dementie (FTD) berooven mensen geleidelijk van beweging, spraak en persoonlijkheid. Een belangrijke verdachte in deze ziekten is een eiwit genaamd TDP-43, dat zich op de verkeerde plaats in zenuwcellen ophoopt. In deze studie gebruiken onderzoekers een klein wormpje, Caenorhabditis elegans, om te observeren wat er gebeurt in levende dieren wanneer TDP-43 zijn normale locatie verlaat en in het cytoplasma van de cel terechtkomt. Door zich te concentreren op een klein, goed begrepen groepje serotonineproducerende neuronen, laten de onderzoekers zien hoe gedrag al vroeg kan ontsporen, lang voordat neuronen zichtbaar afsterven — wat een venster biedt op de vroegste, meest behandelbare stadia van de ziekte. 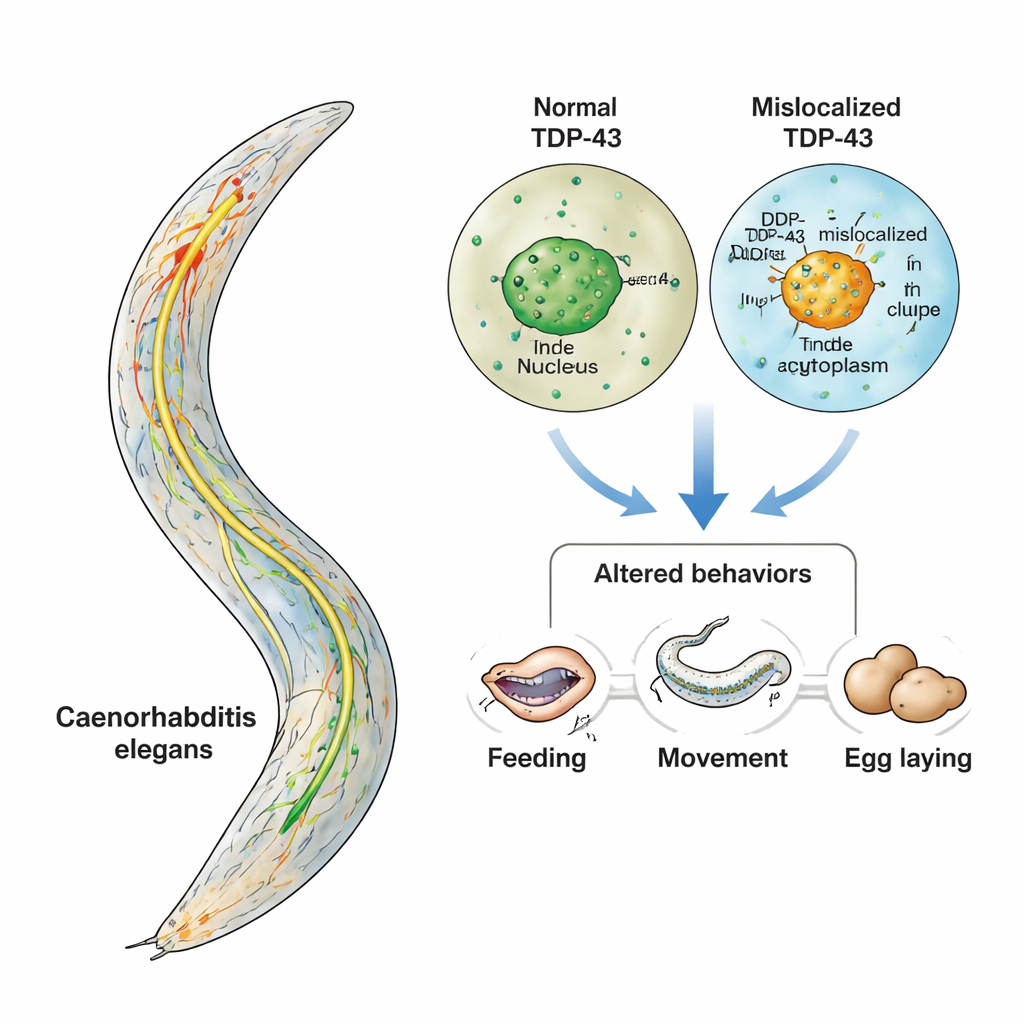
Een klonterend eiwit en een chemische boodschapper
TDP-43 bevindt zich normaal in de kern, waar het helpt bij het beheren van RNA, de werkende kopieën van genetische instructies in de cel. Bij ALS en FTD verlaat TDP-43 echter vaak de kern, hoopt het zich op in het cytoplasma en vormt het plakkerige aggregaten. Tegelijkertijd wijzen gegevens uit patiëntstudies en muismodellen erop dat serotonine, een boodschapper die vooral bekend is vanwege zijn rol in stemming, ook verstoord raakt bij deze ziekten. Omdat serotonine veel gedragingen beïnvloedt — van voeden tot bewegingscontrole — stelden de auteurs een gerichte vraag: als TDP-43 specifiek verkeerd gelokaliseerd is in serotonineproducerende neuronen, functioneren die neuronen dan zodanig anders dat het gedrag verandert, zelfs voordat ze degenereren?
Hertakeling van een eenvoudig zenuwstelsel
Het team wendde zich tot C. elegans, een microscopische worm waarvan het volledige zenuwstelsel van 302 neuronen nauwkeurig in kaart is gebracht. Slechts drie paren van deze neuronen produceren serotonine, en elk paar regelt een duidelijk omschreven gedrag: voeden (faryngeale pomping), vertragen bij het vinden van voedsel en het leggen van eieren. Met genetische middelen maakten de onderzoekers wormen zo dat alleen deze serotonerge neuronen menselijk TDP-43 produceerden. Eén stam maakte de normale, in de kern gelokaliseerde vorm; een andere maakte een gemuteerde versie zonder het nucleaire "adreslabel", waardoor TDP-43 in het cytoplasma ophoopte. Omdat alle andere neuronen onaangetast bleven, konden gedragsveranderingen direct worden herleid tot problemen in dit ene, kleine circuit.
Gedrag faalt voordat neuronen sterven
In meerdere testen gedroegen de gewijzigde wormen zich abnormaal op manieren die sterk leken op gedeeltelijk of ernstig verlies van serotonine. Wormen met de cytoplasmatische versie van TDP-43 vertoonden langzamere ritmische pompbewegingen van hun voedingsorgaan, een zwakkere neiging om te vertragen wanneer ze na vasten voedsel tegenkwamen, en verminderde ei-legging. Wormen die de normale, nucleaire TDP-43 tot expressie brachten, presteerden ook slechter dan ongewijzigde dieren, maar niet zo erg als die met cytoplasmatisch TDP-43, wat een duidelijk gradueel verlies aan functie laat zien. Cruciaal was dat dezelfde dieren, getest in een context waarin serotonine niet nodig is — zwemmen in vloeistof — normaal bewogen. Dit toonde aan dat de kernapparatuur voor locomotie intact was en dat de defecten specifiek waren voor serotonine-afhankelijke gedragingen in plaats van een algemene achteruitgang van de gezondheid. 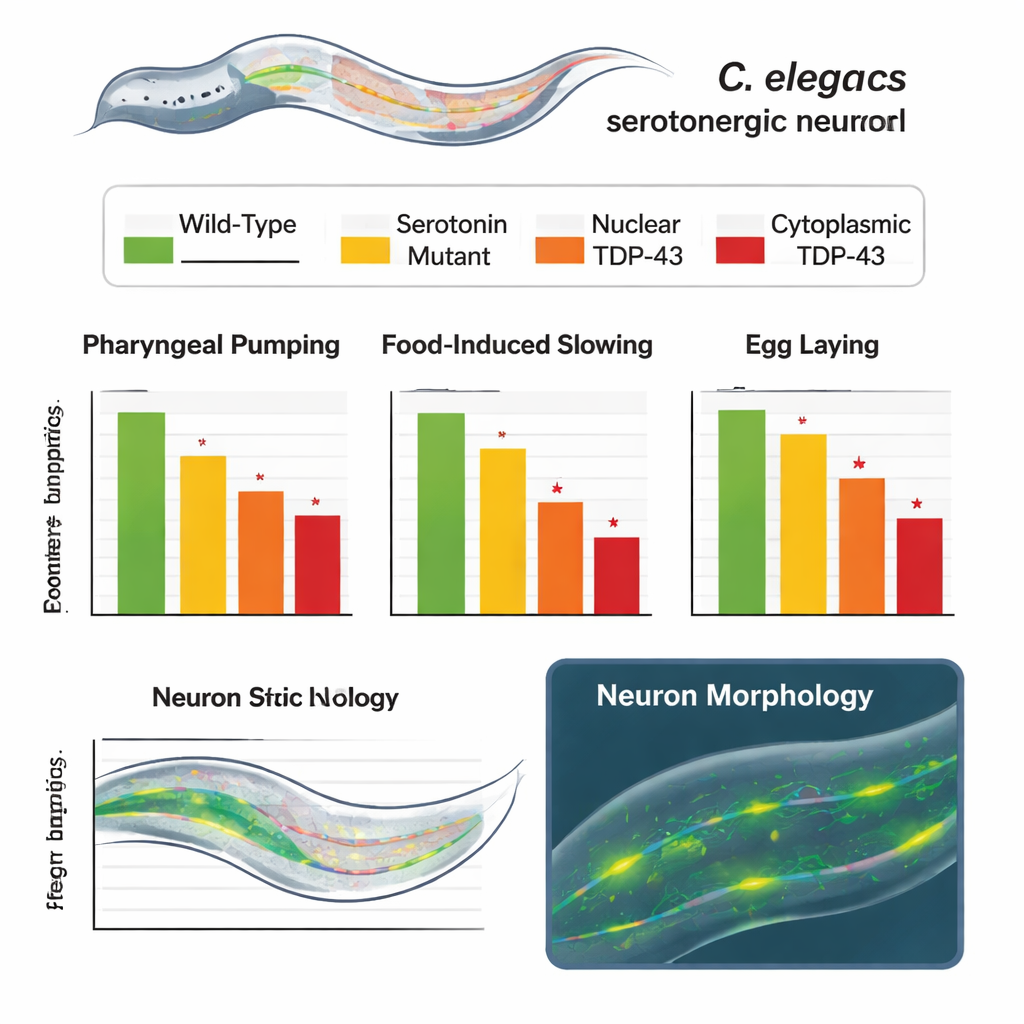
Verborgen schade onthuld door een medicijntest
Om te achterhalen of de getroffen neuronen nog leefden en functioneel waren, gebruikten de onderzoekers fluoxetine, beter bekend als Prozac, een middel dat de serotoninesignalering versterkt. Bij normale wormen verhoogt fluoxetine sterk de ei-legging. Bij de genetisch gemodificeerde wormen nam de ei-legging ook toe na toediening van het medicijn, maar de respons was afgezwakt — vooral bij degenen met cytoplasmatisch TDP-43. Dit patroon suggereert dat de serotonerge neuronen nog signalen konden afgeven, maar minder effectief. Microscopische beeldvorming vertelde een vergelijkbaar verhaal: de serotonineproducerende neuronen zagen er structureel normaal uit, zonder verlies van cellichamen of grote vervormingen van hun vertakkingen, en hun totale fluorescentie — een proxy voor celgezondheid — kwam overeen met die van controledieren.
Vroege waarschuwingssignalen en nieuwe kansen
Gezamenlijk schetsen de bevindingen een beeld waarin verkeerd gelocaliseerd TDP-43 de werking van serotonerge neuronen aanzienlijk kan verstoren terwijl die neuronen ogenschijnlijk intact blijven. Bij de wormen raakt het gedrag verstoord — voeden, beweegaanpassing en voortplanting — voordat er zichtbare neuronale sterfte optreedt. Dit weerspiegelt klinische observaties dat subtiele gedrags- en stemmingsveranderingen vaak voorafgaan aan duidelijke hersenatrofie bij menselijke neurodegeneratieve ziekten. Door een eenvoudig, genetisch manipuleerbaar systeem te bieden waarin vroege, circuitspecifieke defecten nauwkeurig kunnen worden gemeten, kan dit wormmodel wetenschappers helpen te onderzoeken hoe TDP-43 de neuronfunctie verstoort en therapieën te testen die gericht zijn op het redden van neuronen tijdens dit kwetsbare, predegeneratieve venster.
Bronvermelding: Lacour, A., Vassallu, F., Romussi, S. et al. Cytoplasmic TDP-43 leads to early behavioral impairments without neurodegeneration in a serotonergic neuron-specific C. elegans model. Sci Rep 16, 6068 (2026). https://doi.org/10.1038/s41598-026-36138-5
Trefwoorden: TDP-43, serotonine-neuronen, C. elegans, ALS en FTD, neurodegeneratie