Clear Sky Science · nl
ONCOPLEX: een door oncologie geïnspireerd hypergrafmodel dat diverse biologische kennis integreert voor voorspelling van kanker-drivergenen
Waarom dit onderzoek ertoe doet
Kanker wordt aangestuurd door een klein aantal krachtige genetische veranderingen die verscholen liggen tussen duizenden onschuldige varianten. Het vinden van die werkelijk gevaarlijke “driver”-genen is essentieel voor betere diagnose en gerichte behandelingen, maar het is als het signaleren van een paar kopstukken in een uitgestrekte, rumoerige menigte. Deze studie introduceert ONCOPLEX, een nieuw kunstmatig-intelligentieframework dat naar genen kijkt niet één voor één, maar in de context van de biologische paden waarin ze samen werken, en zo een scherper middel biedt om de genen te identificeren die tumoren daadwerkelijk aanstuwen.
Kankergenen zien in hun biologische omgeving
De meeste huidige methoden doorzoeken kankergenomen op mutaties die ongewoon vaak voorkomen of die opvallen in eenvoudige genennetwerken. Die benaderingen helpen, maar biologie is zelden zo eenvoudig. Genen werken meestal in groepen binnen paden die celgroei, DNA-herstel en veel andere processen regelen. ONCOPLEX omarmt deze complexiteit door genen te representeren als knopen en paden als grotere, overlappende groepen die meerdere genen tegelijk kunnen bevatten. Dit soort structuur, bekend als een hypergraf, stelt het model in staat om relaties tussen meerdere genen direct te beschouwen in plaats van ze op te splitsen in veel afzonderlijke paren.
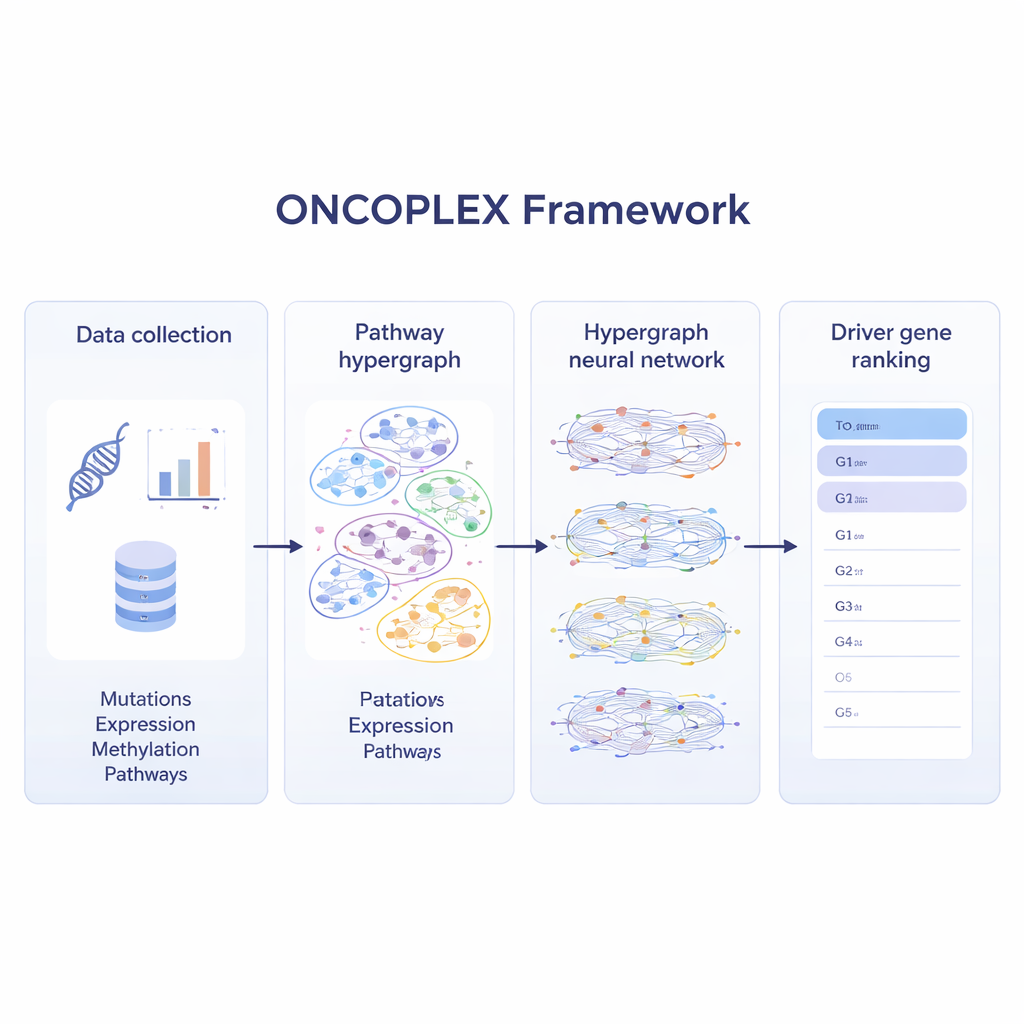
Verschillende lagen kankergegevens combineren
Om het beste uit moderne kankerdatasets te halen, combineert ONCOPLEX meerdere soorten informatie over elk gen. Het gebruikt mutatiefrequenties, veranderingen in genactiviteit, chemische labels op DNA (methylatie) en een rijke set biologische kenmerken zoals evolutionaire conservatie en functionele annotaties. Deze kenmerken worden aan elk gen in de hypergraf gekoppeld. Een gespecialiseerd neuraal netwerk geeft vervolgens informatie door de paden heen, waardoor de representatie van elk gen zowel door zijn eigen gegevens als door het gedrag van de genen waarmee het samenwerkt kan worden gevormd. Het model wordt getraind met genen die al als kankerdri ver bekend zijn, terwijl het ook leert van vele niet-geëtiketteerde genen die belangrijk kunnen zijn maar nog niet erkend zijn.
Beter dan bestaande tools bij veel kankers
De onderzoekers testten ONCOPLEX op data van The Cancer Genome Atlas, zowel door veel tumortypen samen te brengen als door 11 afzonderlijke kankers te onderzoeken, waaronder borst-, long-, lever-, blaaskanker en hoofd- en halstumoren. Ze vergeleken het met verschillende toonaangevende graf- en hypergrafgebaseerde methoden. Over de hele linie was ONCOPLEX beter in het onderscheiden van bekende drivergenen van de veel vaker voorkomende non-drivers en in het hoog ranken van waarschijnlijke drivers. Het voordeel was vooral duidelijk bij de hoogst gerangschikte genen, waar nauwkeurige identificatie het meest waardevol is voor vervolgexperimenten en klinische vertaling.
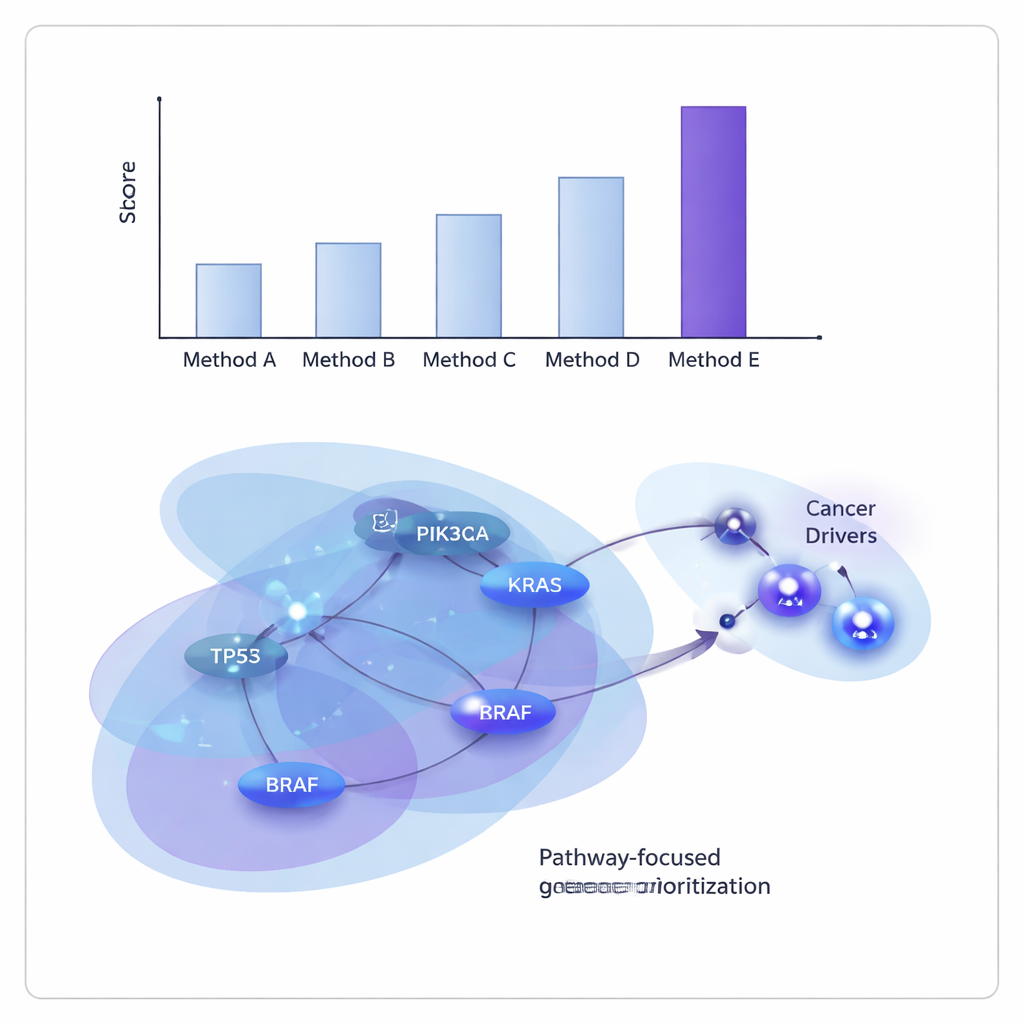
Gedeelde en kankerspecifieke boosdoeners onthullen
Voorbij de ruwe prestatiecijfers brachten de gerangschikte genlijsten van ONCOPLEX veel bekende kankergen naar voren, zoals KRAS, BRAF en leden van het PI3K–AKT-signaleringstraject, wat bevestigt dat het model gevestigde biologie vastlegt. Het benadrukte ook veelbelovende kandidaten die nog niet stevig erkend zijn als drivers in bepaalde kankertypes, waaronder genen zoals GRB2 en MAPK3 bij borstkanker en SHC1 bij maagkanker. Toen het team de hoogst gerangschikte genen onderzocht met pathway-enrichmentsanalyse, vonden ze sterke signaturen van goed bekende kankerpaden, waaronder ErbB-signalisatie en PI3K–AKT–mTOR, evenals immuungerelateerde paden, wat suggereert dat ONCOPLEX zich richt op netwerken die klinisch relevant zijn.
Sterktes, beperkingen en wat hierna komt
Door aan te tonen dat rijkere biologische kenmerken zijn voorspellingen gestaag verbeteren, laat ONCOPLEX de waarde zien van het samenvoegen van veel gegevensbronnen binnen een padgerichte benadering. Tegelijk onthult de studie een beperking: omdat veel kankers een groot aantal paden delen, geeft het model soms de voorkeur aan wijdverspreide “pan-cancer” genen boven genen die werkelijk specifiek zijn voor één tumortype. De auteurs stellen voor dat toekomstig werk moet verfijnen hoe padinformatie wordt gebruikt, zodat gemeenschappelijke en kankerspecifieke signalen duidelijker van elkaar te scheiden zijn.
Wat dit betekent voor patiënten en clinici
Voor niet-specialisten is de belangrijkste conclusie dat ONCOPLEX een meer biologisch realistische manier biedt om te zoeken naar de genen die kanker aansturen. Door naar genen te kijken in het gezelschap waarin ze verkeren—binnen paden in plaats van geïsoleerd—verbetert het onze mogelijkheid om zowel bekende als eerder over het hoofd geziene drivers op te sporen, zelfs in kankers waar weinig over bekend is. Dit soort hulpmiddel kan onderzoekers helpen prioriteiten te stellen voor welke genen in het laboratorium bestudeerd moeten worden, de zoektocht naar nieuwe medicijntargets sturen en uiteindelijk meer precieze, padbewuste behandelstrategieën in de oncologie ondersteunen.
Bronvermelding: Alotaibi, E.M., Alkhnbashi, O.S. & Tran, V.D. ONCOPLEX: an oncology-inspired hypergraph model integrating diverse biological knowledge for cancer driver gene prediction. Sci Rep 16, 5164 (2026). https://doi.org/10.1038/s41598-026-36127-8
Trefwoorden: kanker-drivergenen, hypergraf neurale netwerken, multi-omics integratie, padway-analyse, precisie-oncologie