Clear Sky Science · nl
Omvattende beoordeling van door goudnanostaafjes veroorzaakte genotoxiciteit met behulp van multimodale biologische systemen
Waarom kleine gouden staafjes van belang zijn voor ons DNA
Goud roept misschien sieraden of financiën op, maar in de moderne geneeskunde wordt het ook gevormd tot piepkleine staafjes die duizenden malen dunner zijn dan een menselijke haar. Deze “goudnanostaafjes” kunnen artsen helpen tumoren duidelijker zichtbaar te maken, kankercellen te verhitten en te doden, en medicijnen zeer gericht af te leveren. Tegelijkertijd roepen dezelfde bijzondere eigenschappen die deze deeltjes zo krachtig maken een cruciale vraag op: beschadigen ze het genetisch materiaal in onze cellen? Deze studie kijkt breed, over bacteriën, gist en menselijke leverkankercellen, om te onderzoeken hoe goudnanostaafjes met DNA interactie aangaan en wat dat kan betekenen voor zowel medische behandelingen als veiligheidsregelgeving. 
Van reageerbuizen naar levende cellen
Om de risico’s en voordelen van goudnanostaafjes te onderzoeken, bereidden de onderzoekers eerst uniforme, staafvormige deeltjes van ongeveer 50 nanometer lengte—veel te klein om met het blote oog te zien, maar gemakkelijk in staat om cellen binnen te dringen. Ze testten deze deeltjes vervolgens in meerdere biologische systemen die samen een soort “toxiciteitspijplijn” vormen. Twee veelvoorkomende bacteriën, Salmonella typhimurium en Escherichia coli, werden gebruikt als snelle, eenvoudige sensoren voor DNA-schade. Speciaal geconstrueerde giststammen, die elk één gen misten dat gelinkt is aan stressreacties of celdood, boden een meer mensachtig model omdat gist veel kernroutes met ons deelt. Ten slotte werden menselijke leverkankercellen (HepG2), die veel gebruikt worden om geneesmiddelen en chemicaliën te testen, blootgesteld aan goudnanostaafjes zodat het team veranderingen in sleutelgenen die bij kanker betrokken zijn kon volgen.
DNA zien uitlopen in komeetstaarten
Bij zowel bacteriën als gist gebruikten de wetenschappers een gevoelige techniek genaamd de komeetassay om DNA‑schade per cel ‘zichtbaar’ te maken. Bij deze methode worden cellen in gel ingebed, voorzichtig opengebroken en in een elektrisch veld geplaatst. Intact DNA blijft grotendeels op zijn plaats, maar gebroken strengen stromen eruit en vormen een vorm die lijkt op een komeet met een helder kopje en een uitlopende staart. Door te meten hoe lang en hoe helder die staart is, kunnen onderzoekers de omvang van de genetische schade inschatten. In zowel Salmonella als E. coli veroorzaakten goudnanostaafjes duidelijke, dosisafhankelijke toename in alle komeetparameters: meer cellen met staarten, langere staarten en een hoger percentage DNA dat in de staart werd getrokken. Gist-knockoutstammen vertoonden hetzelfde patroon, waarbij sommige stammen—vooral die met uitschakelingen in genen gerelateerd aan stress en mitochondriale functie—aanzienlijk meer DNA‑fragmentatie lieten zien dan normale gist. 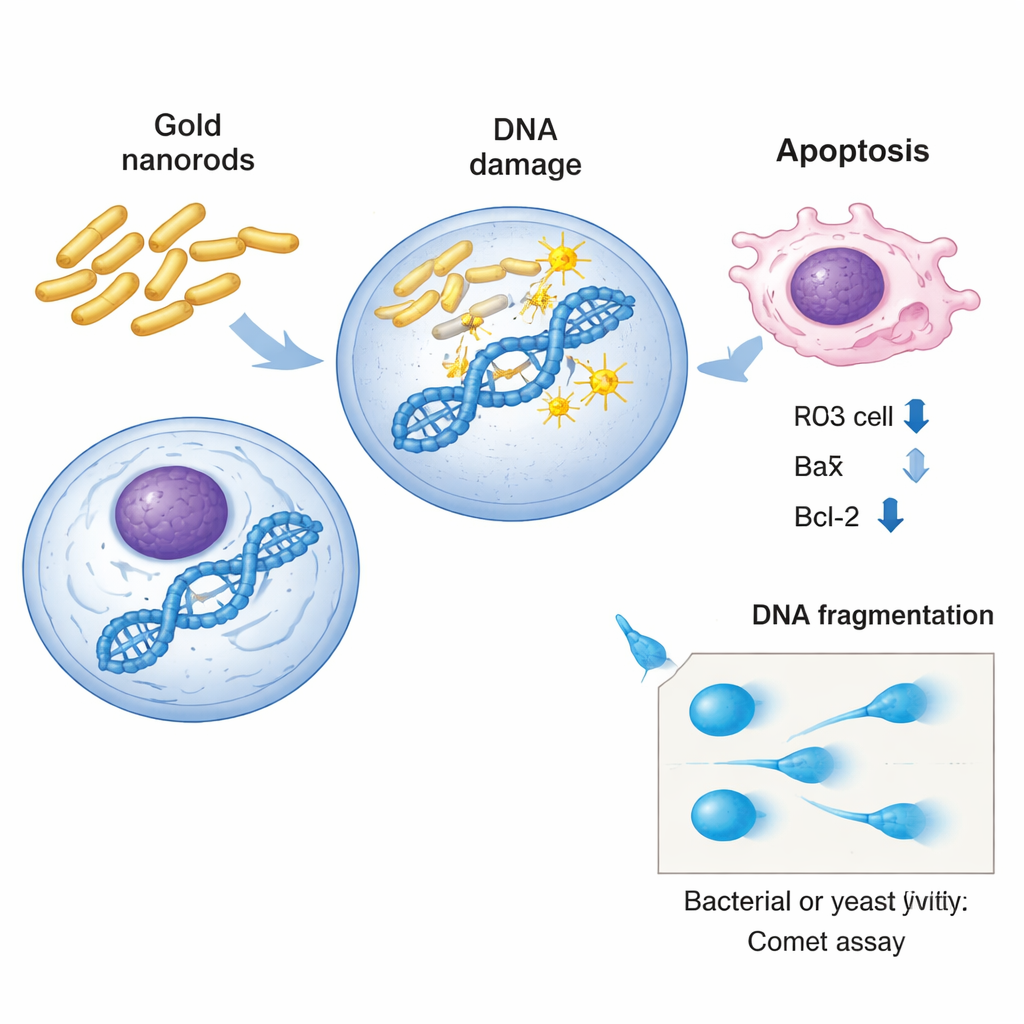
Genetwerkn en doodsignalen in menselijke cellen
In menselijke leverkankercellen keek het team dieper, voorbij fysieke breuken in het DNA, om te zien hoe de interne controlesystemen van de cellen reageerden. Met realtime PCR maten ze de activiteit van drie veelbekende bewakers en uitvoerders van celdoorslag: p53 en Bax, die celdood bevorderen wanneer schade wordt gedetecteerd, en Bcl-2, dat cellen helpt te overleven. Na blootstelling aan halfsterke toxische doses goudnanostaafjes stegen p53- en Bax-niveaus, terwijl Bcl-2-niveaus daalden—een moleculair signaal van geprogrammeerde celdood (apoptose). Met andere woorden: de nanostaafjes beschadigden niet alleen het DNA maar duwden ook kankercellen richting zelfvernietiging. Om de gistresultaten met de menselijke biologie te verbinden, gebruikten de onderzoekers het GeneMANIA-platform om interactienetwerken rond de verwijderde gistgenen in kaart te brengen. Deze analyse toonde dicht geweven netwerken van fysieke en genetische interacties gerelateerd aan stressrespons, DNA-reparatie en mitochondriale functie, wat het idee versterkt dat dezelfde soorten routes kwetsbaar zijn in zowel gist als menselijke cellen.
De medische belofte afwegen tegen genetisch risico
Samen genomen schetsen deze experimenten een genuanceerd beeld van goudnanostaafjes. Enerzijds kunnen ze duidelijk DNA beschadigen in zeer verschillende organismen, en neemt de schade toe met de dosis. Bepaalde genetische achtergronden, zoals giststammen zonder specifieke stress- of mitochondriale genen, zijn bijzonder gevoelig, wat suggereert dat mensen met bepaalde genetische eigenschappen ook anders kunnen reageren. Anderzijds kan in menselijke leverkankercellen deze DNA‑schade en de daaropvolgende activering van doodspaden precies zijn wat artsen willen bij het richten op tumoren. Voor een lezer is de kernboodschap dat goudnanostaafjes krachtige instrumenten zijn die zowel kunnen helpen als schaden: ze kunnen kankercellen doden, maar ze kunnen ook genetische risico’s vormen voor andere cellen en voor het milieu. De studie betoogt dat toekomstige medische toepassingen van deze deeltjes zorgvuldig dosis, gerichte afgifte en patiëntgenen moeten afwegen om hun voordelen te benutten en hun genotoxische potentieel onder controle te houden.
Bronvermelding: Rashad, S.E., Haggran, A.A. & Abdoon, A.S.S. Comprehensive assessment of gold nanorod-induced genotoxicity using multi-model biological systems. Sci Rep 16, 5429 (2026). https://doi.org/10.1038/s41598-026-36119-8
Trefwoorden: goudnanostaafjes, DNA-schade, nanotoxicologie, kankertherapie, genotoxiciteitstests