Clear Sky Science · nl
R5- en R7-posities op fluoroquinolon-skeletten veroorzaken verstoring van F-actinefilamenten
Antibiotica als mogelijke helper in de hersenen
Veel voorkomende hersenaandoeningen, van de ziekte van Alzheimer tot de ziekte van Parkinson, delen een verborgen schuldige: kleine structurele staafjes in zenuwcellen die na verloop van tijd vastlopen en star worden. Deze staafjes bestaan uit het eiwit actine, normaal een flexibele component van het inwendige cellulaire geraamte. Deze studie onderzoekt een verrassende mogelijkheid — dat een goed bekende klasse antibiotica, fluoroquinolonen, kan worden herontworpen om deze schadelijke actinebundels voorzichtig uit elkaar te halen en zo mogelijk de hersenen te beschermen.
Wanneer het cellulaire geraamte misgaat
Gezonde hersencellen hervormen voortdurend hun interne skelet om verbindingen te vormen en aan te passen. Actinefilamenten staan centraal in dit proces: ze ontstaan en lossen weer op wanneer dat nodig is. Onder stress kan actine echter vergrendelen tot hardnekkige, staafachtige aggregaten die de cel verstoppen, het transport van belangrijke ladingen verstoren en de ophoping van ziektegerelateerde eiwitten zoals amyloïde en tau bevorderen. In de loop der jaren kunnen deze staafjes uitgroeien tot dichte structuren, bekend als Hirano-lichamen, die vaak worden aangetroffen in de hersenen van mensen met verschillende neurodegeneratieve aandoeningen. Omdat bestaande actine-gerichte geneesmiddelen vaak extreem toxisch zijn, zijn onderzoekers op zoek naar veiligere kleine moleculen die deze aggregaten kunnen losmaken zonder cellen te schaden.
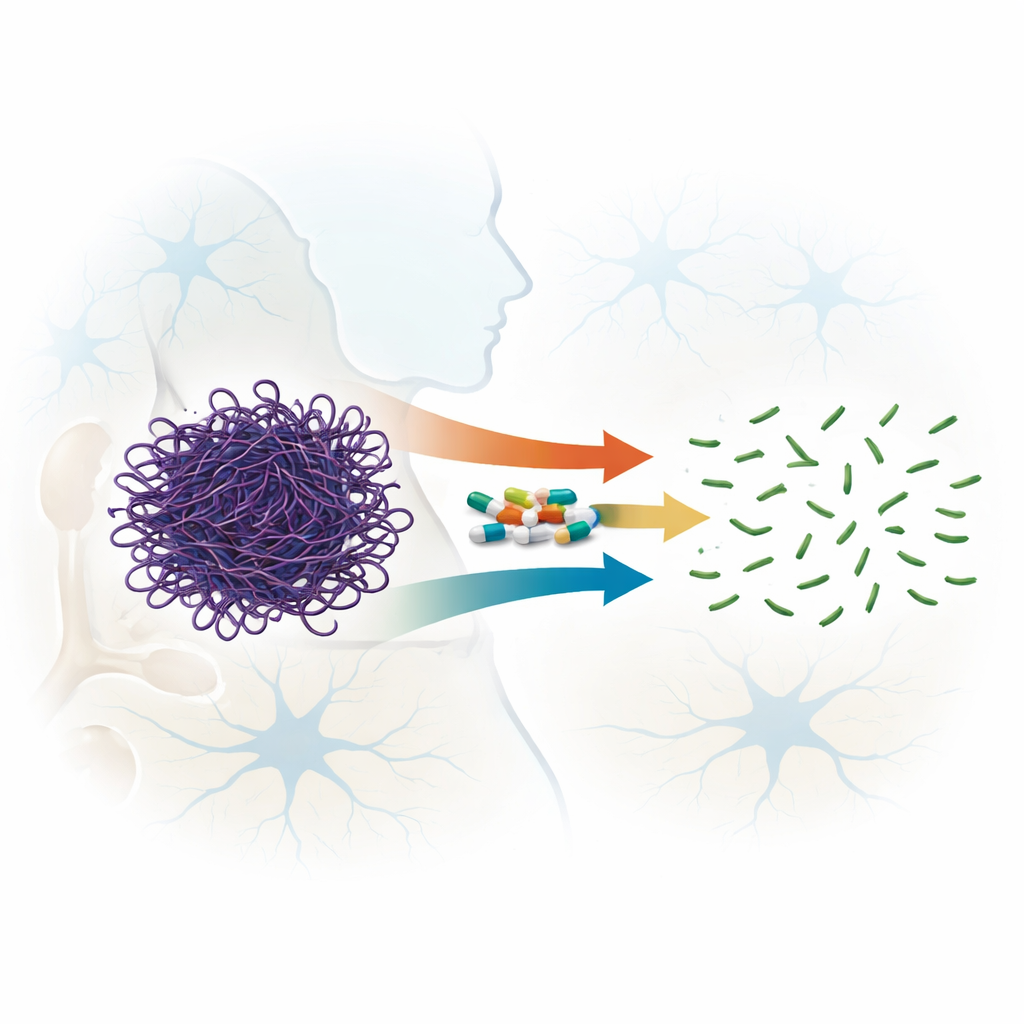
Een onverwachte eigenschap van bekende medicijnen
Fluoroquinolonen zijn breedspectrumantibiotica die wereldwijd worden gebruikt en waarvan sommige nieuwere leden de bloed-hersenbarrière kunnen passeren. Eerdere aanwijzingen suggereerden dat bepaalde fluoroquinolonen actinefilamenten konden destabiliseren. In dit werk vergeleken de auteurs systematisch zeven verwante verbindingen, verspreid over vier generaties van de geneesmiddelfamilie, om te zien hoe goed ze voorgevormde actinefilamenten uiteenrijten in plaats van alleen te verhinderen dat ze zich vormen. Met lichtverstrooiingsmetingen, elektronenmicroscopie en gel-filtratie toonden ze aan dat alle geteste middelen actinefilamenten konden verstoren, maar met zeer verschillende sterktes. Twee middelen, sparfloxacine (een middel van de derde generatie) en moxifloxacine (vierde generatie), sprongen eruit doordat ze lange filamenten snel en onomkeerbaar in veel kleinere stukken hakten, zelfs bij relatief lage medicijn-tot-eiwitverhoudingen.
Filamenten zien uiteenvallen
Hoge-resolutiebeelden en biofysische tests onthulden hoe de filamenten veranderen onder medicijnbehandeling. Elektronenmicroscopie toonde aan dat onbehandeld actine lange, continue strengen vormt, terwijl effectieve fluoroquinolonen deze omzetten in korte, verspreide fragmenten. Minder krachtige leden produceerden geknikte en gebogen filamenten maar braken deze niet volledig. Warmtegebaseerde metingen van eiwitstabiliteit bevestigden deze fysieke verstoring: eenmaal behandeld gedroeg actine zich meer als zijn vrije, niet-geassembleerde vorm, met lagere smelttemperaturen, terwijl de basale bouwsteenstructuur vrijwel ongewijzigd bleef. Dit suggereert dat de middelen actine zelf niet ontvouwen of beschadigen — ze wrikken vooral los hoe de subunits aan elkaar kleven in filamenten.
Inzoomen op de moleculaire greep
Om te begrijpen waarom sommige fluoroquinolonen beter werken dan andere, combineerde het team geavanceerde kernspinresonantie-experimenten met computersimulaties van medicijn–eiwitinteracties. Ze vonden dat alle verbindingen leunen op een gedeelde ringvormige “kern” om contact te maken met actine, vooral op twee posities van die kern die herhaaldelijk het filament aanraken. Extra chemische groepen die op specifieke plaatsen zijn aangebracht — aangeduid als R5 en R7 — beïnvloeden echter sterk hoe stevig en waar elk molecuul bindt. Bij de meest effectieve verstorende middelen dragen deze posities een aminogroep en omvangrijke ringsystemen die reiken naar een klein pocket aan de interface tussen aangrenzende actinestrengen. Daar verstoren ze sleutelstabiliserende contacten, waaronder een belangrijke zoutbrug die normaal helpt filamenten bij elkaar te houden.
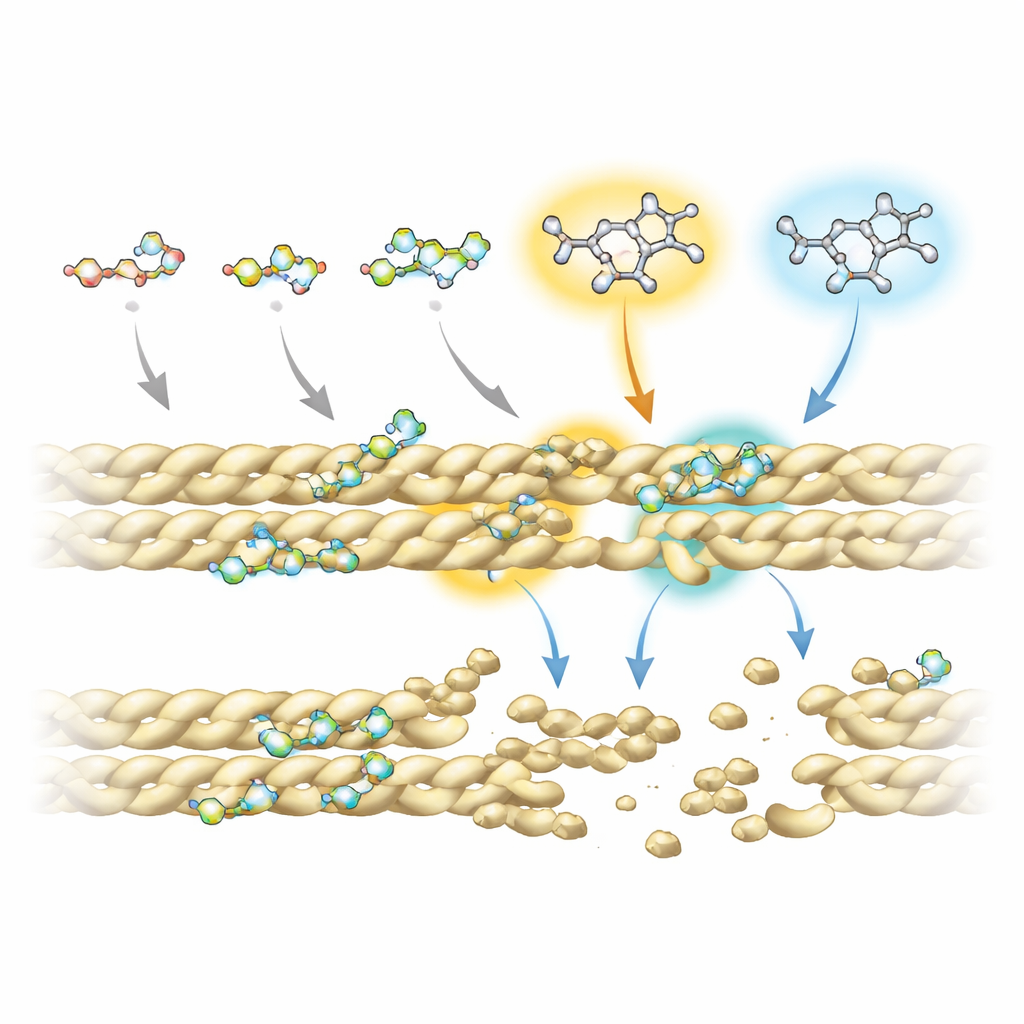
Van gistcellen naar toekomstige therapieën
De onderzoekers testten de middelen ook in een giststam die van nature actinebundels ophoopt, waarmee aspecten van zieke cellen werden nagebootst. Onder de microscoop toonden onbehandelde gistcellen grote, heldere actineklonten, terwijl cellen die werden blootgesteld aan fluoroquinolonen — met name sparfloxacine, moxifloxacine en, bij hogere doses, nalidixinezuur — veel diffuzere, puntige patronen vertoonden, wat aangeeft dat de bundels waren afgebroken. Belangrijk is dat de werking van de middelen relatief mild leek: ze verzwakten de filamentverpakking zonder de onderliggende vorm van actine grofweg te vervormen, en hun binding was zwakker dan die van klassieke actinetoxines, wat mogelijk het risico op ernstige bijwerkingen vermindert.
Slimmere actine-gerichte geneesmiddelen ontwerpen
Samenvattend laat deze studie zien dat kleine aanpassingen aan bekende antibiotica drastisch kunnen veranderen hoe ze interageren met het interne cellulaire geraamte. Door de R5- en R7-posities te identificeren als sleutel-"knoppen" voor zowel actineverstoring als hersenpenetratie, schetsen de auteurs een blauwdruk voor het creëren van nieuwe, door fluoroquinolonen geïnspireerde moleculen die selectief schadelijke actineaggregaten ontmantelen. Hoewel deze bevindingen een vroeg, laboratoriumstadium proof-of-principle zijn, roepen ze de mogelijkheid op dat toekomstige geneesmiddelen afgeleid van vertrouwde antibiotica toxisch geraamte in zenuwcellen zouden kunnen opruimen en zo sommige vormen van neurodegeneratie kunnen vertragen of voorkomen.
Bronvermelding: Gupta, R.J., Nair, H., Sarhadi, T.R. et al. R5 and R7 positions on fluoroquinolone scaffolds drive F-actin filament disruption. Sci Rep 16, 9517 (2026). https://doi.org/10.1038/s41598-026-36089-x
Trefwoorden: actine-aggregaten, fluoroquinolon-antibiotica, neurodegeneratieve ziekte, drug repurposing, cytoskelet